สารออกฤทธิ์: เซฟตาซิดิม
Glazidim 250 มก. ผงสำหรับสารละลายสำหรับฉีด
Glazidim 500 มก. ผงสำหรับสารละลายสำหรับฉีด
Glazidim 1 g ผงสำหรับสารละลายสำหรับฉีด
Glazidim 1 g ผงสำหรับสารละลายสำหรับฉีดหรือแช่
Glazidim 2 g powder สำหรับฉีดหรือแช่
Glazidim 1 g ผงสำหรับสารละลายสำหรับแช่
Glazidim 2 g ผงสำหรับสารละลายสำหรับแช่
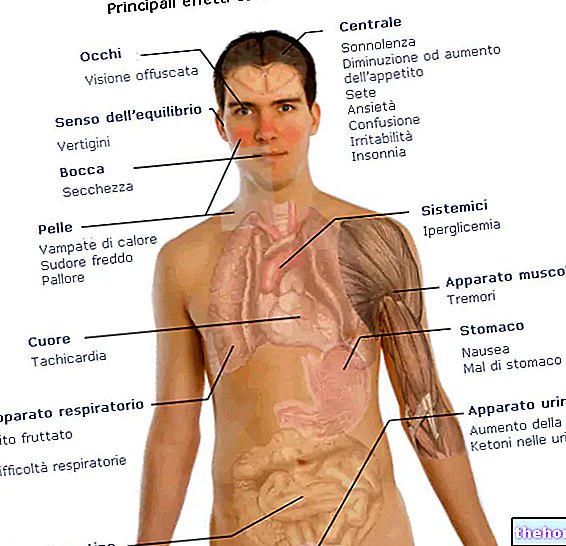
ทำไมจึงใช้กลาซิดิม? มีไว้เพื่ออะไร?
Glazidim เป็นยาปฏิชีวนะที่ใช้ในผู้ใหญ่และเด็ก (รวมถึงทารกแรกเกิด) มันทำงานโดยการฆ่าเชื้อแบคทีเรียที่ทำให้เกิดการติดเชื้อและอยู่ในกลุ่มของยาที่เรียกว่าเซฟาโลสปอริน
Glazidim ใช้รักษาการติดเชื้อแบคทีเรียที่รุนแรงของ:
- ปอดหรือหน้าอก
- ปอดและหลอดลมในผู้ป่วยโรคซิสติก ไฟโบรซิส
- สมอง (เยื่อหุ้มสมองอักเสบ)
- หู
- ทางเดินปัสสาวะ
- ผิวหนังและเนื้อเยื่ออ่อน
- ช่องท้องและผนังช่องท้อง (เยื่อบุช่องท้องอักเสบ)
- กระดูกและข้อต่อ
Glazidim ยังสามารถใช้ได้:
- เพื่อป้องกันการติดเชื้อระหว่างการผ่าตัดต่อมลูกหมากในผู้ชาย
- เพื่อรักษาผู้ป่วยที่มีจำนวนเม็ดเลือดขาวต่ำ (neutropenia) ที่มีไข้เนื่องจาก 'การติดเชื้อแบคทีเรีย'
ข้อห้าม เมื่อไม่ควรใช้ Glazidim
คุณไม่ควรได้รับ Gladizim:
- หากคุณแพ้เซฟาซิดิมหรือส่วนประกอบอื่นๆ ของยานี้ (ระบุไว้ในหัวข้อ 6)
- หากคุณมีอาการแพ้อย่างรุนแรงต่อยาปฏิชีวนะชนิดอื่น (เพนิซิลลิน โมโนแบคแทม และคาร์บาเพเนม) เนื่องจากคุณอาจแพ้กลาซิดิมด้วย
แจ้งให้แพทย์ทราบก่อนเริ่มใช้ Glazidim หากคุณคิดว่าสิ่งนี้ใช้ได้กับคุณ คุณต้องไม่รับกลาซิดิม
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนรับประทาน Glazidim
ดูแลเป็นพิเศษกับกลาซิดิม
ระวังอาการบางอย่าง เช่น อาการแพ้ ความผิดปกติของระบบประสาท และความผิดปกติของระบบทางเดินอาหาร เช่น ท้องร่วง ขณะรับการรักษาด้วยกลาซิดิม ซึ่งจะช่วยลดความเสี่ยงของปัญหาที่อาจเกิดขึ้น ดู (เงื่อนไขที่คุณต้องระวัง) ในหัวข้อ 4 หากคุณมีอาการแพ้ยาปฏิชีวนะอื่น ๆ คุณอาจแพ้ Glazidim
หากคุณต้องการตรวจเลือดหรือปัสสาวะ
Glazidim อาจส่งผลต่อผลการทดสอบน้ำตาลในปัสสาวะและการตรวจเลือดที่เรียกว่าการทดสอบ Coombs หากคุณมีการทดสอบเหล่านี้:
บอกผู้ที่เก็บตัวอย่างว่าคุณกำลังรับการรักษาด้วยกลาซิดิม
ปฏิกิริยา ยาหรืออาหารชนิดใดที่สามารถปรับเปลี่ยนผลของกลาซิดิมได้
แจ้งให้แพทย์ประจำตัวของคุณทราบหากคุณกำลังรับประทาน เพิ่งกำลังรับประทาน หรืออาจกำลังใช้ยาอื่นอยู่ รวมถึงยาที่ไม่มีใบสั่งยาด้วย
คุณไม่ควรให้ Glazidim โดยไม่ปรึกษาแพทย์หากคุณกำลังใช้:
- ยาปฏิชีวนะที่เรียกว่าคลอแรมเฟนิคอล
- ยาปฏิชีวนะชนิดหนึ่งที่เรียกว่า aminoglycosides เช่น gentamicin, tobramycin
- ยาเม็ดขับปัสสาวะที่เรียกว่า furosemide
แจ้งให้แพทย์ทราบหากสิ่งนี้ใช้ได้กับคุณ
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
การตั้งครรภ์ ให้นมบุตร และภาวะเจริญพันธุ์
ปรึกษาแพทย์เพื่อขอคำแนะนำก่อนที่คุณจะได้รับ Glazidim:
- หากคุณกำลังตั้งครรภ์ สงสัย หรือกำลังวางแผนที่จะตั้งครรภ์
- หากคุณกำลังให้นมบุตร
แพทย์ของคุณจะชั่งน้ำหนักประโยชน์ของการรักษาด้วย Glazidim ต่อความเสี่ยงต่อทารก
การขับรถและการใช้เครื่องจักร
Glazidim อาจทำให้เกิดผลข้างเคียงที่ส่งผลต่อความสามารถในการขับรถเช่นอาการวิงเวียนศีรษะ ห้ามขับรถหรือใช้เครื่องจักรเว้นแต่คุณจะแน่ใจว่าไม่ได้รับผลกระทบใดๆ
Glazidim มีโซเดียม
คุณต้องคำนึงถึงสิ่งต่อไปนี้หากคุณควบคุมอาหารโซเดียม
ปริมาณ วิธีการ และระยะเวลาในการบริหาร วิธีใช้ Glazidim: Posology
Glazidim ได้รับอย่างไร?
Glazidim มักจะได้รับจากแพทย์หรือพยาบาล สามารถให้ในรูปแบบ "การฉีดเข้าเส้นเลือดดำหรือฉีด" เข้าเส้นเลือดหรือกล้ามเนื้อโดยตรง
Glazidim จัดทำโดยแพทย์ เภสัชกร หรือพยาบาลโดยใช้น้ำฉีดหรือของเหลวในการให้ยาที่เหมาะสม
ปริมาณที่แนะนำ
ปริมาณที่เหมาะสมของกลาซิดิมจะถูกกำหนดโดยแพทย์ของคุณ และขึ้นอยู่กับ: ความรุนแรงและประเภทของการติดเชื้อ หากคุณกำลังรับการรักษาด้วยยาปฏิชีวนะชนิดอื่น น้ำหนักตัวและอายุของคุณ สภาพของไตของคุณ
ทารกแรกเกิด (0-2 เดือน)
สำหรับน้ำหนักตัวเด็กแต่ละกิโลกรัม ยากลาซิดิม 25 ถึง 60 มก. ต่อวันจะได้รับในสองโดส
ทารก (อายุเกิน 2 เดือน) และทารกที่มีน้ำหนักน้อยกว่า 40 กก.
สำหรับน้ำหนักตัวของทารกหรือเด็กแต่ละกิโลกรัม ยากลาซิดิม 100 ถึง 150 มก. จะได้รับต่อวันโดยแบ่งเป็นสามขนาด ปริมาณสูงสุดคือ 6 กรัมต่อวัน
ผู้ใหญ่และวัยรุ่นที่มีน้ำหนักตั้งแต่ 40 กก. ขึ้นไป
Glazidim 1 ถึง 2 กรัมสามครั้งต่อวัน ปริมาณสูงสุดคือ 9 กรัมต่อวัน
ผู้ป่วยที่อายุเกิน 65
ปริมาณรายวันโดยทั่วไปไม่ควรเกิน 3 กรัมต่อวัน โดยเฉพาะอย่างยิ่งถ้าคุณอายุมากกว่า 80 ปี
ผู้ป่วยโรคไต
คุณอาจได้รับยาที่แตกต่างจากปกติ แพทย์หรือพยาบาลของคุณจะเป็นผู้ตัดสินว่าคุณต้องการกลาซิดิมมากน้อยเพียงใดโดยพิจารณาจากความรุนแรงของโรคไต แพทย์ของคุณจะติดตามคุณอย่างใกล้ชิดและอาจมีการทดสอบการทำงานของไตเป็นระยะๆ
ยาเกินขนาด จะทำอย่างไรถ้าคุณกิน Glazidim มากเกินไป
หากคุณได้รับกลาซิดิมมากกว่าที่ควร
หากคุณใช้ยาเกินขนาดที่กำหนดโดยไม่ได้ตั้งใจ ให้ติดต่อแพทย์หรือโรงพยาบาลที่ใกล้ที่สุดทันที
หากคุณลืมใช้ Glazidim
ถ้าลืมฉีดยา ต้องรีบฉีดยา ห้ามกิน 2 ครั้ง (ฉีด 2 ครั้งพร้อมกัน) เพื่อชดเชยการลืมยา ให้กินยาในเข็มต่อไปตามเวลาปกติ
อย่าหยุดทานกลาซิดิม
อย่าหยุดทานกลาซิดิมเว้นแต่แพทย์จะสั่ง หากคุณมีคำถามเพิ่มเติมเกี่ยวกับการใช้ยานี้ โปรดสอบถามแพทย์หรือพยาบาลของคุณ
ผลข้างเคียงของ Glazidim
เช่นเดียวกับยาอื่น ๆ ยานี้อาจทำให้เกิดผลข้างเคียงได้ แม้ว่าจะไม่ใช่ทุกคนที่ได้รับก็ตาม
เงื่อนไขที่ต้องให้ความสนใจ
ผลข้างเคียงที่ร้ายแรงต่อไปนี้เกิดขึ้นในคนจำนวนน้อย แต่ไม่ทราบความถี่ที่แน่นอน:
- ปฏิกิริยาการแพ้อย่างรุนแรง อาการต่างๆ ได้แก่ ผื่นขึ้น ผื่นขึ้น บวมบางครั้งที่ใบหน้าหรือปากทำให้หายใจลำบาก
- ผื่นที่มีลักษณะเป็นพุพองเล็กๆ คล้ายเป้าหมาย (จุดมืดตรงกลางล้อมรอบด้วย "บริเวณสว่างที่มีวงแหวนสีดำรอบขอบ)
- ผื่นขึ้นเป็นวงกว้างด้วยแผลพุพองและการลอกของผิวหนัง (สิ่งเหล่านี้อาจเป็นสัญญาณของ Stevens-Johnson syndrome หรือ toxic epidermal necrolysis)
- ความผิดปกติของระบบประสาท: อาการสั่น อาการชัก และในบางกรณี อาการโคม่า สิ่งเหล่านี้เกิดขึ้นในผู้ที่มีขนาดยาสูงเกินไป โดยเฉพาะอย่างยิ่งในผู้ที่เป็นโรคไต
ติดต่อแพทย์หรือพยาบาลของคุณโดยด่วน หากคุณมีอาการเหล่านี้
ผลข้างเคียงที่พบบ่อย
สิ่งเหล่านี้อาจส่งผลกระทบต่อผู้ป่วยมากถึง 1 ใน 10:
- ท้องเสีย
- บวมและแดงตามเส้นเลือด
- เกิดผื่นแดงที่อาจคัน
- ปวด แสบร้อน บวมหรืออักเสบบริเวณที่ฉีด
บอกแพทย์หากเงื่อนไขใด ๆ เหล่านี้ทำให้คุณกังวล
ผลข้างเคียงที่อาจปรากฏในการตรวจเลือด ได้แก่
- การเพิ่มขึ้นของเซลล์เม็ดเลือดขาว (eosinophilia)
- เพิ่มจำนวนเซลล์ที่ช่วยให้ลิ่มเลือด
- การเพิ่มขึ้นของเอนไซม์ตับ
ผลข้างเคียงที่ไม่ธรรมดา
สิ่งเหล่านี้อาจส่งผลกระทบต่อผู้ป่วยมากถึง 1 ใน 100:
- การอักเสบของลำไส้ซึ่งอาจทำให้เกิดอาการปวดหรือท้องเสียซึ่งอาจมีเลือด
- candidiasis - การติดเชื้อราในปากหรือช่องคลอด
- ปวดหัว
- อาการวิงเวียนศีรษะ
- อาการปวดท้อง
- คลื่นไส้หรืออาเจียน
- ไข้และหนาวสั่น
บอกแพทย์หากคุณมีอาการเหล่านี้
ผลข้างเคียงที่อาจปรากฏในการตรวจเลือด ได้แก่
- ทำให้จำนวนเม็ดเลือดขาวลดลง
- ลดจำนวนเกล็ดเลือด (เซลล์ที่ช่วยให้ลิ่มเลือด)
- การเพิ่มขึ้นของระดับเลือดของยูเรีย BUN หรือซีรั่ม creatinine
ผลข้างเคียงที่หายากมาก
สิ่งเหล่านี้อาจส่งผลกระทบมากถึง 1 ใน 10,000 ผู้ป่วย:
- การอักเสบหรือไตวาย
ผลข้างเคียงอื่นๆ
ผลข้างเคียงอื่น ๆ เกิดขึ้นในคนจำนวนน้อย แต่ไม่ทราบความถี่ที่แน่นอน:
- ความรู้สึกของเข็มและหมุด
- รสชาติที่ไม่พึงประสงค์ในปาก
- สีเหลืองของตาขาวหรือผิวหนัง
ผลข้างเคียงอื่น ๆ ที่อาจปรากฏในการตรวจเลือดคือ:
- การทำลายเซลล์เม็ดเลือดแดงเร็วเกินไป
- การเพิ่มขึ้นของเซลล์เม็ดเลือดขาวบางชนิด
- จำนวนเม็ดเลือดขาวลดลงอย่างรุนแรง
การรายงานผลข้างเคียง
หากคุณได้รับผลข้างเคียง ให้ปรึกษาแพทย์หรือเภสัชกร ซึ่งรวมถึงผลข้างเคียงที่อาจเกิดขึ้นซึ่งไม่ได้ระบุไว้ในเอกสารฉบับนี้ คุณยังสามารถรายงานผลข้างเคียงได้โดยตรงผ่านระบบการรายงานที่: http://www.agenziafarmaco.gov.it/it/responsabiliโดยการรายงานผลข้างเคียง คุณสามารถช่วยให้ข้อมูลเพิ่มเติมเกี่ยวกับความปลอดภัยของยานี้ได้
การหมดอายุและการเก็บรักษา
เก็บยานี้ให้พ้นสายตาและมือเด็ก
ก่อนทำการสร้างใหม่ ให้เก็บขวดที่ป้องกันแสงไว้
ผลิตภัณฑ์ในสารละลาย หลังจากคืนสภาพด้วยน้ำ p.p.i. o กับของเหลวที่ให้ยาที่เข้ากันได้ (เช่น น้ำเกลือ กลูโคส หรือสารละลายโซเดียมแลคเตท) โดยปกติควรใช้ภายใน 18 ชั่วโมงหากเก็บไว้ที่อุณหภูมิปกติ และภายใน 7 วันหากเก็บไว้ที่ 4 ° C
องค์ประกอบและรูปแบบยา
กลาซิดิมมีอะไรบ้าง
สารออกฤทธิ์คือเซฟตาซิดิม (ในรูปของเซฟตาซิดิมเพนตาไฮเดรต)
Glazidim 250 มก. ผงสำหรับฉีดประกอบด้วย 250 มก. ceftazidime
Glazidim 500 มก. ผงสำหรับฉีดมีเซฟตาซิดิม 500 มก
Glazidim 1 g ผงสำหรับฉีดประกอบด้วย 1 g ceftazidime
Glazidim 1 g ผงสำหรับฉีดหรือแช่ประกอบด้วย 1 g ของ ceftazidime
Glazidim 2 g ผงสำหรับสารละลายสำหรับฉีดหรือแช่ประกอบด้วย ceftazidime 2 g
Glazidim 1 g ผงสำหรับการแก้ปัญหาสำหรับการแช่มี 1 g ของ ceftazidime
Glazidim 2 g ผงสำหรับการแก้ปัญหาสำหรับการแช่มี 2 g ของ ceftazidime
สารเพิ่มปริมาณคือ:
ขวดผง: ปราศจากโซเดียมคาร์บอเนต
หลอดตัวทำละลาย: น้ำสำหรับฉีด
ถุงแช่ประกอบด้วย:
เกลือแกง
น้ำฉีด
Glazidim หน้าตาเป็นอย่างไรและเนื้อหาของแพ็คเกจ
Glazidim บรรจุในขวดแก้วไร้สีประเภทที่ 3 พร้อมฝาอีลาสโตเมอร์และฝาอะลูมิเนียม ตัวทำละลายในขวดแก้วไร้สีประเภทที่ 1
Glazidim 250 มก. ผงสำหรับสารละลายสำหรับฉีด:
- ผง 1 ขวด + หลอดตัวทำละลาย 1 มล.
Glazidim 500 มก. ผงสำหรับสารละลายสำหรับฉีด:
- ผง 1 ขวด + หลอดตัวทำละลาย 1.5 มล.
Glazidim 1 g ผงสำหรับสารละลายสำหรับฉีด:
- ผง 1 ขวด + หลอดตัวทำละลาย 3 มล.
- ผง 1 ขวด + หลอดตัวทำละลาย 10 มล.
Glazidim 1 g ผงสำหรับฉีดหรือแช่:
- แป้ง 10 ขวด
- แป้ง 25 ขวด
Glazidim 2 g ผงสำหรับฉีดสำหรับสารละลายสำหรับการแช่:
- แป้งฝุ่น 1 ขวด
Glazidim 1 g และ 2 g ผงสำหรับสารละลายสำหรับการแช่บรรจุในขวดแก้วไร้สีประเภท I พร้อมกับอุปกรณ์ที่ได้รับการจดสิทธิบัตรพิเศษ - MONOVIAL - สำหรับการเตรียมสารละลายแช่ ถุงแช่ที่มีสารละลายทางสรีรวิทยามีความจุ 100 มล.
Glazidim 1 g ผงสำหรับสารละลายสำหรับการแช่:
- ผงแป้ง 1 ขวดพร้อมอุปกรณ์ MONOVIAL
- แป้ง 1 ขวดพร้อมอุปกรณ์ MONOVIAL + ถุงแช่ 100 มล.
Glazidim 2 g ผงสำหรับสารละลายสำหรับการแช่:
- ผงแป้ง 1 ขวดพร้อมอุปกรณ์ MONOVIAL
- แป้ง 1 ขวดพร้อมอุปกรณ์ MONOVIAL + ถุงแช่ 100 มล.
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่นำเสนออาจไม่ใช่ข้อมูลล่าสุด
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
กลาซิดิม
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
Glazidim 250 มก. ผงสำหรับสารละลายสำหรับฉีด
ขวดแต่ละขวดมีเซฟตาซิดิม 250 มก. (ในรูปของเซฟตาซิดิม เพนตาไฮเดรต)
Glazidim 500 มก. ผงสำหรับสารละลายสำหรับฉีด
แต่ละขวดมีเซฟตาซิดิม 500 มก. (ในรูปของเซฟตาซิดิม เพนตาไฮเดรต)
Glazidim 1 g ผงสำหรับสารละลายสำหรับฉีด
แต่ละขวดมีเซฟตาซิดิม 1 กรัม (ในรูปของเซฟตาซิดิม เพนตาไฮเดรต)
Glazidim 1 g ผงสำหรับสารละลายสำหรับฉีดหรือแช่
แต่ละขวดมีเซฟตาซิดิม 1 กรัม (ในรูปของเซฟตาซิดิม เพนตาไฮเดรต)
Glazidim 2 g powder สำหรับฉีดหรือแช่
ขวดแต่ละขวดมีเซฟตาซิดิม 2 กรัม (ในรูปของเซฟตาซิดิมเพนตาไฮเดรต)
Glazidim 1 g ผงสำหรับสารละลายสำหรับแช่
แต่ละขวดมีเซฟตาซิดิม 1 กรัม (ในรูปของเซฟตาซิดิม เพนตาไฮเดรต)
Glazidim 2 g ผงสำหรับสารละลายสำหรับแช่
ขวดแต่ละขวดมีเซฟตาซิดิม 2 กรัม (ในรูปของเซฟตาซิดิมเพนตาไฮเดรต)
สำหรับรายการสารปรุงแต่งทั้งหมด โปรดดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
250 mg, 500 mg 1 g ผงสำหรับฉีด
ผงสำหรับฉีด
1 g, 2 g ผงสำหรับสารละลายสำหรับฉีดหรือแช่
ผงสำหรับฉีดหรือแช่
1 ก., ผง 2 ก. สำหรับสารละลายสำหรับแช่ (พร้อมอุปกรณ์ Monovial)
ผงสำหรับสารละลายสำหรับแช่
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
Glazidim มีไว้สำหรับการรักษาโรคติดเชื้อตามรายการด้านล่างในผู้ใหญ่และเด็กรวมถึงทารกแรกเกิด (ตั้งแต่แรกเกิด)
• โรคปอดบวมในโรงพยาบาล
• การติดเชื้อในปอดในโรคซิสติก ไฟโบรซิส
• เยื่อหุ้มสมองอักเสบจากแบคทีเรีย
• หูชั้นกลางอักเสบที่เป็นหนองเรื้อรัง
• โรคหูน้ำหนวกภายนอกที่เป็นมะเร็ง
• การติดเชื้อทางเดินปัสสาวะที่ซับซ้อน
• การติดเชื้อที่ผิวหนังและเนื้อเยื่ออ่อนที่ซับซ้อน
• การติดเชื้อในช่องท้องที่ซับซ้อน
• การติดเชื้อที่กระดูกและข้อ
• เยื่อบุช่องท้องอักเสบที่เกี่ยวข้องกับการฟอกไตในผู้ป่วยที่มีการล้างไตทางช่องท้องอย่างต่อเนื่อง (การล้างไตทางช่องท้องอย่างต่อเนื่อง-CAPD)
การรักษาผู้ป่วยที่มีภาวะแบคทีเรียที่เกิดขึ้นหรือสงสัยว่าเกี่ยวข้องกับการติดเชื้อใด ๆ ที่ระบุไว้ข้างต้น
เซฟตาซิดิมสามารถใช้ในการจัดการผู้ป่วยนิวโทรพีนิกที่มีไข้ที่สงสัยว่าจะเกิดจาก "การติดเชื้อแบคทีเรีย"
เซฟตาซิดิมสามารถใช้ในการป้องกันการติดเชื้อทางเดินปัสสาวะของผู้ป่วยในระหว่างการผ่าตัดต่อมลูกหมาก (การผ่าตัดผ่านท่อปัสสาวะของต่อมลูกหมาก-ทูอาร์พี).
การเลือกใช้ยาเซฟตาซิดิมต้องคำนึงถึงสเปกตรัมต้านแบคทีเรียซึ่งจำกัดเฉพาะแบคทีเรียแอโรบิกแกรมลบเป็นหลัก (ดูหัวข้อ 4.4 และ 5.1)
ต้องให้ยาเซฟตาซิดิมร่วมกับสารต้านแบคทีเรียอื่น ๆ เมื่อใดก็ตามที่แบคทีเรียที่พิจารณาว่ามีส่วนในการติดเชื้ออยู่นอกขอบเขตของกิจกรรม
ควรพิจารณาแนวทางที่เป็นทางการเกี่ยวกับการใช้สารต้านแบคทีเรียอย่างเหมาะสม
04.2 วิทยาและวิธีการบริหาร
ปริมาณ
ตารางที่ 1: ผู้ใหญ่และเด็ก ≥ 40 กก.
ตารางที่ 2: เด็ก
ประชากรเด็ก
ความปลอดภัยและประสิทธิภาพของ Glazidim ที่ฉีดอย่างต่อเนื่องในทารกและเด็กอายุ ≤ 2 เดือนยังไม่ได้รับการจัดตั้งขึ้น
พลเมืองอาวุโส
ในแง่ของอายุที่ลดลงของ ceftazidime ในผู้ป่วยสูงอายุ ปริมาณรายวันไม่ควรเกิน 3 กรัมในผู้ป่วยที่มีอายุมากกว่า 80 ปี
การด้อยค่าของตับ
ข้อมูลที่มีอยู่ไม่ได้ระบุถึงความจำเป็นในการปรับขนาดยาสำหรับผู้ป่วยที่มีความบกพร่องของตับในระดับเล็กน้อยหรือปานกลาง ไม่มีข้อมูลจากการศึกษาในผู้ป่วยที่มีความบกพร่องทางตับอย่างรุนแรง (ดูหัวข้อ 5.2 เพิ่มเติม) แนะนำให้ติดตามทางคลินิกอย่างใกล้ชิดเพื่อความปลอดภัยและประสิทธิภาพ
การด้อยค่าของไต
Ceftazidime ถูกขับออกทางไตไม่เปลี่ยนแปลง ดังนั้น ในผู้ป่วยที่มีการทำงานของไตบกพร่อง ควรลดขนาดยาลง (ดูหัวข้อ 4.4 ด้วย)
ควรให้ขนาดยาเริ่มต้นที่ 1 กรัม ปริมาณการบำรุงรักษาควรขึ้นอยู่กับการกวาดล้างของ creatinine
ตารางที่ 3: ปริมาณการบำรุงรักษาที่แนะนำของ Glazidim ในการด้อยค่าของไต "" การแช่เป็นระยะ
ผู้ใหญ่และเด็ก ≥ 40 กก.
ในผู้ป่วยที่มีการติดเชื้อรุนแรง ควรเพิ่มขนาดยาต่อหน่วย 50% หรือเพิ่มความถี่ในการใช้ยา
ในเด็ก ควรคำนวณค่าประมาณการกวาดล้างของครีเอตินีนตามหน้าที่ของพื้นที่ผิวกายหรือมวลร่างกายที่ไม่ติดมัน
เด็ก
แนะนำให้ติดตามทางคลินิกอย่างใกล้ชิดเพื่อความปลอดภัยและประสิทธิภาพ
ตารางที่ 4: ปริมาณการบำรุงรักษาที่แนะนำของ Glazidim ในการด้อยค่าของไต "" การแช่อย่างต่อเนื่อง
ผู้ใหญ่และเด็ก ≥ 40 กก.
ควรใช้ความระมัดระวังในการเลือกขนาดยา แนะนำให้ติดตามทางคลินิกอย่างใกล้ชิดเพื่อความปลอดภัยและประสิทธิภาพ
เด็ก
ความปลอดภัยและประสิทธิภาพของ Glazidim เป็นยาอย่างต่อเนื่องในเด็กที่มีความบกพร่องทางไต
หากใช้ยาอย่างต่อเนื่องในเด็กที่มีความบกพร่องทางไต ควรคำนวณการกวาดล้างของ creatinine เป็นหน้าที่ของพื้นที่ผิวกายหรือมวลร่างกายติดมัน
การฟอกไต
ค่าครึ่งชีวิตในซีรั่มระหว่างการฟอกไตมีตั้งแต่ 3 ถึง 5 ชั่วโมง
หลังการฟอกไตแต่ละครั้ง ควรทำซ้ำขนาดยาเซฟาตาซิไดม์ที่แนะนำในตารางที่ 5 และ 6
การล้างไตทางช่องท้อง
เซฟทาซิไดม์สามารถใช้ในการล้างไตทางช่องท้องและการล้างไตทางช่องท้องแบบต่อเนื่อง (CAPD)
นอกจากการใช้ทางหลอดเลือดดำแล้ว ยาเซฟาตาซิดิมยังสามารถเติมลงในน้ำยาล้างไต (โดยปกติคือ 125 ถึง 250 มก. ต่อสารละลายฟอกไต 2 ลิตร)
สำหรับผู้ป่วยที่มีภาวะไตไม่เพียงพอในการฟอกเลือดด้วยหลอดเลือดแดงแบบต่อเนื่องหรือการกรองเลือดด้วยเลือดไหลสูงในหอผู้ป่วยหนัก: 1 กรัมต่อวัน รับประทานครั้งเดียวหรือแบ่งขนาด สำหรับการกรองเลือดที่มีการไหลต่ำ ให้ปฏิบัติตามปริมาณที่แนะนำในภาวะไตวาย
สำหรับผู้ป่วยในการกรองเลือดทางหลอดเลือดดำและการฟอกเลือดทางหลอดเลือดดำ ให้ปฏิบัติตามขนาดยาที่แนะนำในตารางที่ 5 และ 6 ด้านล่าง
ตารางที่ 5: แนวทางการให้ยาสำหรับการกรองเลือดในหลอดเลือดดำและหลอดเลือดดำอย่างต่อเนื่อง
ตารางที่ 6: แนวทางการให้ยาฟอกไตทางหลอดเลือดดำอย่างต่อเนื่อง
วิธีการบริหาร
ปริมาณขึ้นอยู่กับความรุนแรง ความไว ตำแหน่งและประเภทของการติดเชื้อ และอายุและการทำงานของไตของผู้ป่วย
Glazidim 500 มก. และ 250 มก. ควรได้รับการฉีดเข้าเส้นเลือดดำหรือโดยการฉีดเข้ากล้ามลึก บริเวณที่ฉีดเข้ากล้ามเนื้อที่แนะนำคือส่วนบนด้านนอกของ gluteus maximus หรือส่วนด้านข้างของต้นขา สารละลายกลาซิดิมสามารถฉีดเข้าเส้นเลือดได้โดยตรง เส้นทางการบริหารที่แนะนำมาตรฐานคือการฉีดเข้าเส้นเลือดดำเป็นระยะ ควรพิจารณาการบริหารกล้ามเนื้อเฉพาะเมื่อไม่สามารถให้ยาทางหลอดเลือดดำได้หรือไม่เหมาะสมสำหรับผู้ป่วย
Glazidim 1 กรัมควรได้รับการฉีดเข้าเส้นเลือดดำหรือโดยการฉีดหรือโดยการฉีดเข้ากล้ามลึก บริเวณที่ฉีดเข้ากล้ามเนื้อที่แนะนำคือส่วนบนด้านนอกของ gluteus maximus หรือส่วนด้านข้างของต้นขา สารละลายกลาซิดิมสามารถฉีดเข้าเส้นเลือดโดยตรงหรือฉีดผ่านชุดให้ยา หากผู้ป่วยได้รับของเหลวทางหลอดเลือด เส้นทางการบริหารที่แนะนำมาตรฐานคือการฉีดเข้าเส้นเลือดดำเป็นระยะ ๆ หรือการฉีดยาเข้าเส้นเลือดดำอย่างต่อเนื่อง ควรพิจารณาการบริหารกล้ามเนื้อเฉพาะเมื่อไม่สามารถให้ยาทางหลอดเลือดดำได้หรือไม่เหมาะสมสำหรับผู้ป่วย
Glazidim 2 g ควรได้รับการฉีดเข้าเส้นเลือดดำหรือฉีด สารละลายกลาซิดิมสามารถฉีดเข้าเส้นเลือดโดยตรงหรือฉีดผ่านชุดให้ยา หากผู้ป่วยได้รับของเหลวทางหลอดเลือด เส้นทางการบริหารที่แนะนำมาตรฐานคือการฉีดเข้าเส้นเลือดดำเป็นระยะ ๆ หรือการฉีดยาเข้าเส้นเลือดดำอย่างต่อเนื่อง
04.3 ข้อห้าม
แพ้เซฟาโลสปอรินอื่น ๆ หรือสารเพิ่มปริมาณใด ๆ ที่ระบุไว้ในหัวข้อ 6.1
ประวัติแพ้อย่างรุนแรง (เช่น ปฏิกิริยาแอนาไฟแล็กติก) กับสารต้านแบคทีเรียเบตา-แลคแทมชนิดอื่น (เพนิซิลลิน โมโนแบคแทม และคาร์บาเพนเนม)
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
เช่นเดียวกับสารต้านแบคทีเรียเบต้าแลคตัมทั้งหมด มีรายงานปฏิกิริยาภูมิไวเกินที่รุนแรงและถึงขั้นเสียชีวิตได้ในบางครั้ง ในกรณีที่เกิดปฏิกิริยาภูมิไวเกินอย่างรุนแรง ควรหยุดการรักษาด้วยเซฟตาซิไดม์ทันทีและใช้มาตรการฉุกเฉินที่เหมาะสม
ก่อนเริ่มการรักษาควรตรวจสอบให้แน่ใจว่าผู้ป่วยไม่มีประวัติอาการแพ้อย่างรุนแรงต่อ ceftazidime หรือ cephalosporins อื่น ๆ หรือสาร beta-lactam ชนิดอื่น ๆ ควรใช้ความระมัดระวังเป็นพิเศษหากให้ ceftazidime กับผู้ป่วยที่มี "ประวัติ" แพ้ง่ายไม่รุนแรงต่อสารเบต้า-แลกแทมอื่น ๆ
เซฟตาซิดิมมีฤทธิ์ต้านแบคทีเรียในวงจำกัด ไม่เหมาะที่จะใช้เป็นสารต้านแบคทีเรียเพียงชนิดเดียวในการรักษาโรคติดเชื้อบางประเภท เว้นแต่ว่าเชื้อโรคนั้นได้รับการบันทึกไว้แล้วและเป็นที่ทราบกันว่ามีความละเอียดอ่อน หรือมีข้อสงสัยสูงว่าเชื้อโรคที่มีแนวโน้มมากที่สุดอาจไวต่อการรักษาด้วยยาเซฟตาซิไดมโดยเฉพาะอย่างยิ่งเมื่อพิจารณาการรักษาผู้ป่วยที่มีภาวะแบคทีเรียและเมื่อรักษาเยื่อหุ้มสมองอักเสบจากแบคทีเรีย การติดเชื้อที่ผิวหนังและเนื้อเยื่ออ่อน และการติดเชื้อที่กระดูกและข้อ นอกจากนี้ เซฟทาซิไดมยังไวต่อการไฮโดรไลซิสของเบต้าแลคทาเมสในวงกว้างหลายชนิด (เบต้าแลคทาเมสขยายสเปกตรัม-ESBL) ดังนั้นควรพิจารณาข้อมูลเกี่ยวกับความชุกของสิ่งมีชีวิตที่ผลิต ESBL เมื่อเลือกการรักษาด้วยเซฟาซิดีน
มีรายงานเกี่ยวกับอาการลำไส้ใหญ่บวมที่สัมพันธ์กับสารต้านแบคทีเรียและอาการลำไส้ใหญ่อักเสบจากเยื่อหุ้มสมองเทียมกับสารต้านแบคทีเรียเกือบทั้งหมด รวมทั้งเซฟตาซิดิมและอาจมีความรุนแรงตั้งแต่เล็กน้อยจนถึงเป็นอันตรายถึงชีวิต ดังนั้นจึงเป็นสิ่งสำคัญที่จะต้องพิจารณาการวินิจฉัยนี้ในผู้ป่วยที่มีอาการท้องร่วงในระหว่างหรือหลังการให้ยาเซฟตาซิไดม์ (ดูหัวข้อ 4.8) การหยุดยาเซฟตาซิไดมและการให้การรักษาเฉพาะ คลอสทริเดียม ดิฟิไซล์ จะต้องนำมาพิจารณา ไม่ควรให้ผลิตภัณฑ์ยาที่ยับยั้งการบีบตัวของหลอดเลือด
การรักษาร่วมกับยาเซฟาโลสปอรินในปริมาณสูงและผลิตภัณฑ์ยาที่เป็นพิษต่อไต เช่น อะมิโนไกลโคไซด์หรือยาขับปัสสาวะที่มีศักยภาพ (เช่น ฟูโรเซไมด์) อาจส่งผลเสียต่อการทำงานของไต
ยาเซฟตาซิดิมถูกไตขับออก ดังนั้นควรลดขนาดยาตามระดับความบกพร่องของไต ผู้ป่วยที่มีความบกพร่องทางไตควรได้รับการตรวจสอบอย่างรอบคอบเพื่อประสิทธิภาพและความปลอดภัย มีการรายงานผลทางระบบประสาทเป็นครั้งคราวเมื่อไม่ได้ลดขนาดยาในผู้ป่วยที่มีความบกพร่องทางไต (ดูหัวข้อ 4.2 และ 4.8)
การใช้เป็นเวลานานอาจทำให้จุลินทรีย์ที่ไม่ไวต่อการเจริญมากเกินไป (เช่น Enterococci, เชื้อรา) ซึ่งอาจต้องหยุดการรักษาหรือมาตรการที่เหมาะสมอื่นๆ การตรวจสอบสภาพของผู้ป่วยซ้ำ ๆ เป็นสิ่งสำคัญ
เซฟทาซิดิมไม่รบกวนการทดสอบด้วยเอนไซม์สำหรับการตรวจวัดไกลโคซูเรีย แต่อาจมีการรบกวนเล็กน้อย (ผลบวกที่ผิดพลาด) กับวิธีการที่อิงตามการลดทองแดง (เบเนดิกต์, เฟห์ลิง, คลินิเทส)
เซฟทาซิดิมไม่รบกวนการทดสอบอัลคาไลน์พิกเรตสำหรับการตรวจวัดครีเอตินีน
การพัฒนาการทดสอบคูมบ์สในเชิงบวกที่เกี่ยวข้องกับการใช้เซฟตาซิดิมในผู้ป่วยประมาณ 5% อาจรบกวนการทดสอบความเข้ากันได้ของเลือด
ข้อมูลสำคัญเกี่ยวกับสารเพิ่มปริมาณของ Glazidim:
ผง 250 มก. สำหรับสารละลายสำหรับฉีด
Glazidim 250 มก. มีโซเดียม 13 มก. ต่อขวด
ผง 500 มก. สำหรับสารละลายสำหรับฉีด
Glazidim 500 มก. มีโซเดียม 26 มก. ต่อขวด
ผง 1 กรัมสำหรับสารละลายสำหรับฉีดหรือแช่, ผง 1 กรัมสำหรับสารละลายสำหรับแช่
Glazidim 1 g มีโซเดียม 52 มก. ต่อขวด
ผง 2 กรัมสำหรับสารละลายสำหรับฉีดหรือแช่, ผง 2 กรัมสำหรับสารละลายสำหรับการแช่
Glazidim 2 g มีโซเดียม 104 มก. ต่อขวด
สิ่งนี้ควรพิจารณาสำหรับผู้ป่วยที่ควบคุมอาหารโซเดียม
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
มีการศึกษาปฏิสัมพันธ์กับโพรเบเนซิดและฟูโรเซไมด์เท่านั้น
การใช้ปริมาณสูงร่วมกับผลิตภัณฑ์ยาที่เป็นพิษต่อไตอาจส่งผลเสียต่อการทำงานของไต (ดูหัวข้อ 4.4)
คลอแรมเฟนิคอลเป็นปฏิปักษ์ ในหลอดทดลอง เซฟตาซิดิมและเซฟาโลสปอรินอื่นๆ ความเกี่ยวข้องทางคลินิกของการสังเกตนี้ไม่เป็นที่ทราบแน่ชัด แต่ถ้ามีการใช้เซฟตาซิดิมและคลอแรมเฟนิคอลร่วมกัน ควรพิจารณาความเป็นไปได้ของการเป็นปรปักษ์กันระหว่างยาปฏิชีวนะทั้งสองชนิด
04.6 การตั้งครรภ์และให้นมบุตร
การตั้งครรภ์
มีข้อมูลจำนวนจำกัดเกี่ยวกับการใช้เซฟตาซิดิมในสตรีตั้งครรภ์ การศึกษาในสัตว์ทดลองไม่ได้ระบุถึงผลที่เป็นอันตรายโดยตรงหรือโดยอ้อมในส่วนที่เกี่ยวกับการตั้งครรภ์ การพัฒนาของตัวอ่อน/ทารกในครรภ์ การคลอด หรือพัฒนาการหลังคลอด (ดูหัวข้อ 5.3)
Glazidim ควรกำหนดให้กับสตรีมีครรภ์เท่านั้นหากผลประโยชน์มีมากกว่าความเสี่ยง
การตั้งครรภ์
เซฟทาซิดิมถูกขับออกมาในน้ำนมแม่ในปริมาณเล็กน้อย แต่ในขนาดยาที่ใช้รักษาของเซฟตาซิดิมไม่มีผลกระทบต่อทารกที่กินนมแม่ เซฟตาซิดิมสามารถใช้ได้ระหว่างให้นมลูก
ภาวะเจริญพันธุ์
ไม่มีข้อมูลที่สามารถใช้ได้.
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
ไม่มีการศึกษาเกี่ยวกับความสามารถในการขับขี่และการใช้เครื่องจักร อย่างไรก็ตาม อาจเกิดผลกระทบที่ไม่พึงประสงค์ (เช่น อาการวิงเวียนศีรษะ) ซึ่งอาจทำให้ความสามารถในการขับขี่หรือใช้เครื่องจักรลดลง (ดูหัวข้อ 4.8)
04.8 ผลกระทบที่ไม่พึงประสงค์
อาการไม่พึงประสงค์ที่พบบ่อยที่สุดคือ eosinophilia, thrombocytosis, phlebitis หรือ thrombophlebitis ด้วยการฉีดเข้าเส้นเลือดดำ, ท้องร่วง, การเพิ่มขึ้นของเอนไซม์ตับชั่วคราว, ผื่นตามผิวหนังหรือลมพิษ, ความเจ็บปวดและ / หรือการอักเสบหลังการฉีดเข้ากล้ามและการทดสอบ Coombs ในเชิงบวก
ข้อมูลจากการทดลองทางคลินิกที่ได้รับการสนับสนุนและไม่ได้รับการสนับสนุนถูกนำมาใช้เพื่อกำหนดความถี่ของผลข้างเคียงที่พบบ่อยและผิดปกติ ความถี่ที่กำหนดให้กับผลที่ไม่พึงประสงค์อื่น ๆ ทั้งหมดถูกกำหนดโดยพื้นฐานบนพื้นฐานของข้อมูลการเฝ้าระวังทางเภสัชวิทยาที่ตามมา
การตลาดและอ้างถึงความถี่ของการรายงานมากกว่าความถี่จริง ๆ ภายในแต่ละระดับความถี่ผลกระทบที่ไม่พึงประสงค์จะแสดงตามลำดับความรุนแรงที่ลดลง แบบแผนต่อไปนี้ถูกใช้สำหรับการจำแนกความถี่:
พบบ่อยมาก (≥ 1/10)
สามัญ (≥1 / 100 y
ผิดปกติ (≥1 / 1,000 y
หายาก (≥1 / 10,000 y
หายากมาก (
ไม่ทราบ (ไม่สามารถประมาณได้จากข้อมูลที่มีอยู่)
1 มีรายงานเกี่ยวกับผลที่ตามมาของระบบประสาท ได้แก่ อาการสั่น กล้ามเนื้อกระตุกในกล้ามเนื้อ อาการชัก โรคไข้สมองอักเสบ และอาการโคม่าในผู้ป่วยที่มีความบกพร่องทางไตซึ่งไม่ได้ลดขนาดยา Glazidim อย่างเหมาะสม
2 อาการท้องร่วงและอาการลำไส้ใหญ่บวมอาจสัมพันธ์กับการปรากฏตัวของ คลอสทริเดียม ดิฟิไซล์ และอยู่ในรูปแบบของอาการลำไส้ใหญ่บวมปลอม
3 ALT (SGPT), AST (SOGT), LHD, GGT, อัลคาไลน์ฟอสฟาเตส
4 การทดสอบคูมบ์สในเชิงบวกเกิดขึ้นในผู้ป่วยประมาณ 5% และอาจรบกวนการทดสอบความเข้ากันได้ของเลือด
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยซึ่งเกิดขึ้นหลังจากการอนุมัติผลิตภัณฑ์ยามีความสำคัญเนื่องจากช่วยให้สามารถตรวจสอบความสมดุลของผลประโยชน์/ความเสี่ยงของผลิตภัณฑ์ยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านสุขภาพรายงานอาการไม่พึงประสงค์ที่น่าสงสัยผ่านระบบการรายงานระดับประเทศ "ที่อยู่: http ://www.agenziafarmaco.gov.it/it/responsabili.
04.9 ใช้ยาเกินขนาด
การให้ยาเกินขนาดสามารถนำไปสู่ผลที่ตามมาของระบบประสาท รวมทั้งโรคไข้สมองอักเสบ อาการชัก และโคม่า
อาการของยาเกินขนาดอาจเกิดขึ้นได้หากลดขนาดยาลงอย่างเหมาะสมในผู้ป่วยที่มีความบกพร่องทางไต (ดูหัวข้อ 4.2 และ 4.4)
ระดับเซฟทาซิไดม์ในซีรัมสามารถลดลงได้โดยการฟอกไตหรือการฟอกไตทางช่องท้อง
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
กลุ่มเภสัชบำบัด: ยาต้านแบคทีเรียสำหรับการใช้อย่างเป็นระบบ เซฟาโลสปอรินรุ่นที่สาม - รหัส ATC: J01DD02
กลไกการออกฤทธิ์
เซฟตาซิดิมยับยั้งการสังเคราะห์ผนังเซลล์ของแบคทีเรียหลังจากการยึดเกาะกับโปรตีนที่จับกับเพนิซิลลิน (โปรตีนที่จับกับเพนิซิลลิน - ป.ป.ช.) สิ่งนี้เกี่ยวข้องกับการหยุดชะงักของการสังเคราะห์ทางชีวภาพของผนังเซลล์ (peptidoglycan) ซึ่งนำไปสู่การสลายเซลล์แบคทีเรียและความตาย
ความสัมพันธ์ทางเภสัชจลนศาสตร์ / เภสัชพลศาสตร์
สำหรับเซฟาโลสปอริน ดัชนีเภสัชจลนศาสตร์-เภสัชพลศาสตร์ที่สำคัญที่สุดมีความสัมพันธ์กับประสิทธิภาพ ในร่างกาย แสดงให้เห็นว่าเป็นเปอร์เซ็นต์ของเวลาภายในช่วงขนาดยาในระหว่างที่ความเข้มข้นของยาที่จับกับที่ไม่ใช่โปรตีนยังคงสูงกว่าความเข้มข้นที่ยับยั้งขั้นต่ำ (MIC) ของเซฟตาซิดิมสำหรับสายพันธุ์แบคทีเรียเป้าหมายแต่ละชนิด (เช่น T% > MIC)
กลไกต้านทาน
ความต้านทานต่อแบคทีเรียต่อเซฟตาซิดิมอาจเกิดจากกลไกต่อไปนี้อย่างน้อยหนึ่งอย่าง:
• ไฮโดรไลซิสโดยเบต้าแลคทาเมส เซฟทาซิดิมสามารถไฮโดรไลซ์ได้อย่างมีประสิทธิภาพโดยเบต้าแลคทาเมสในวงกว้าง (เบต้าแลคทาเมสขยายสเปกตรัม-ESBLs) รวมถึงตระกูล SHV ของ ESBLs และเอนไซม์ AmpC ซึ่งสามารถเหนี่ยวนำหรือยับยั้งได้อย่างเสถียรในแบคทีเรียแกรมลบบางสายพันธุ์
• ลดความสัมพันธ์ของโปรตีนที่จับกับเพนิซิลลินสำหรับเซฟทาซิไดม์
• การซึมผ่านไม่ได้ของเยื่อหุ้มชั้นนอกที่จำกัดการเข้าถึงเซฟตาซิไดม์ต่อโปรตีนที่จับกับเพนิซิลลินในสิ่งมีชีวิตแกรมลบ
• ปั๊มระบายแบคทีเรีย
เบรกพอยต์
จุดพักของความเข้มข้นการยับยั้งขั้นต่ำ (MIC) ที่จัดตั้งขึ้นโดยคณะกรรมการยุโรปว่าด้วยการทดสอบความไวต่อแบคทีเรีย (คณะกรรมการยุโรปว่าด้วยการทดสอบความไวต่อยาต้านจุลชีพ - EUCAST) มีดังต่อไปนี้:
S = อ่อนไหว, I = ปานกลาง, R = ต้านทาน
1 จุดพักที่เกี่ยวข้องกับการรักษาด้วยยาขนาดสูง (2 ก. x 3)
2 จุดพักที่ไม่เกี่ยวข้องกับชนิดส่วนใหญ่ถูกกำหนดโดยอิงตามข้อมูล PK / PD และเป็นอิสระจากการกระจาย MIC ของสปีชีส์เฉพาะ ใช้สำหรับสายพันธุ์ที่ไม่ได้ระบุไว้ในตารางหรือหมายเหตุด้านล่างเท่านั้น
ความไวทางจุลชีววิทยา
ความชุกของการดื้อยาที่ได้รับอาจแตกต่างกันไปตามภูมิศาสตร์และตามเวลาสำหรับสายพันธุ์ที่เลือก และข้อมูลในท้องถิ่นเกี่ยวกับการดื้อยาเป็นที่ต้องการ โดยเฉพาะอย่างยิ่งเมื่อรักษาการติดเชื้อรุนแรง ตามความจำเป็น เมื่อความชุกของการดื้อยาในท้องถิ่นนั้นเป็นที่น่าสงสัยถึงประโยชน์ของยาเซฟตาซิไดม์ในการติดเชื้อบางประเภท ควรขอคำแนะนำจากผู้เชี่ยวชาญ
แกะที่อ่อนไหวง่าย
แอโรบิกแกรมบวก:
Streptococcus pyogenes
Streptococcus agalactiae
แอโรบิกแกรมลบ:
ซิโตรแบคเตอร์ โคเซริ
ฮีโมฟีลัส อินฟลูเอนเซ
โมราเซลลา กาตาร์ราลิส
Neisseria เยื่อหุ้มสมองอักเสบ
Pasteurella multocida
โพรทูส มิราบิลิส
โพรทูส เอสพีพี (คนอื่น)
โพรวิเดนเซีย เอสพีพี
สายพันธุ์ที่ความแข็งแกร่งที่ได้รับอาจเป็นปัญหาได้
แอโรบิกแกรมลบ:
Acinetobacter baumannii £ +
Burkholderia เซปาเซีย
Citrobacter freundii
เอนเทอโรแบคเตอร์ แอโรจีเนส
Enterobacter cloacae
Escherichia coli
Klebsiella pneumoniae
Klebsiella เอสพีพี (คนอื่น)
Pseudomonas aeruginosa
Serratia เอสพีพี
Morganella morganii
แอโรบิกแกรมบวก:
Staphylococcus aureus £
Streptococcus pneumoniae ££
ไวริแดนส์ กรุ๊ป สเตรปโทคอกคัส
แกรมบวกแบบไม่ใช้ออกซิเจน:
คลอสทริเดียม เพอร์ฟรินเกนส์
เปปโตสเตรปโตคอคคัส เอสพีพี
แกรมลบแบบไม่ใช้ออกซิเจน:
ฟูโซแบคทีเรียม เอสพีพี
สิ่งมีชีวิตที่ต้านทานโดยเนื้อแท้
แอโรบิกแกรมบวก:
เอนเทอโรคอคคัส รวมอยู่ด้วย Enterococcus อุจจาระ และ เอนเทอโรคอคคัส ฟีเซียม
Listeria เอสพีพี
แกรมบวกแบบไม่ใช้ออกซิเจน:
คลอสทริเดียม ดิฟิไซล์
แกรมลบแบบไม่ใช้ออกซิเจน:
แบคทีเรีย เอสพีพี (หลายชนิดของ แบคทีเรียที่เปราะบาง มีภูมิต้านทาน)
คนอื่น:
หนองในเทียม เอสพีพี
มัยโคพลาสมา เอสพีพี
Legionella เอสพีพี
£ S. aureus ซึ่งไวต่อเมทิซิลลินถือว่ามีความไวต่ำโดยเนื้อแท้ต่อเซฟตาซิดิม ทั้งหมด S. aureus ทนต่อ methicillin สามารถทนต่อ ceftazidime
££ S. pneumoniae แสดงให้เห็นถึงความไวปานกลางหรือทนต่อ penicellin สามารถแสดงให้เห็นถึงความไวต่อ ceftazidime ที่ลดลงอย่างน้อย
+มีการสังเกตอัตราการต่อต้านที่สูงในพื้นที่ / ประเทศ / ภูมิภาคหนึ่งแห่งหรือมากกว่าในสหภาพยุโรป
05.2 คุณสมบัติทางเภสัชจลนศาสตร์
การดูดซึม
หลังจากได้รับ ceftazidime 500 มก. และ 1 กรัมในกล้ามเนื้อ ระดับสูงสุดของพลาสมาในพลาสมาที่ 18 และ 37 มก. / ล. ตามลำดับจะถึงอย่างรวดเร็ว ห้านาทีหลังจากให้ยาลูกกลอนทางหลอดเลือดดำ 500 มก. 1 กรัมหรือ 2 กรัมระดับพลาสม่าเท่ากับ 46, 87 และ 170 มก. / ล. ตามลำดับ จลนพลศาสตร์ของเซฟตาซิดิมเป็นเส้นตรงภายในช่วงขนาดยาครั้งเดียว 0.5 ถึง 2 กรัมหลังการให้ยาทางหลอดเลือดดำหรือทางกล้ามเนื้อ
การกระจาย
การจับโปรตีนในซีรั่มของเซฟาซิดิมอยู่ในระดับต่ำและประมาณ 10% ความเข้มข้นที่เกินจาก MIC สำหรับเชื้อโรคทั่วไปสามารถหาได้ในเนื้อเยื่อ เช่น กระดูก หัวใจ น้ำดี เสมหะ น้ำมูก ไขข้อ เยื่อหุ้มปอด และของเหลวในช่องท้อง Ceftaidime ข้ามรกอย่างรวดเร็วและถูกขับออกมาในน้ำนมแม่ การเจาะเข้าไปในเลือดที่ไม่บุบสลาย อุปสรรคของสมองไม่ดีส่งผลให้ระดับ ceftazidime ใน CSF ต่ำในกรณีที่ไม่มีการอักเสบ อย่างไรก็ตาม พบความเข้มข้น 4 ถึง 20 มก. / ล. หรือมากกว่าใน CSF เมื่อเยื่อหุ้มสมองอักเสบ
การเปลี่ยนแปลงทางชีวภาพ
เซฟตาซิดิมไม่ถูกเผาผลาญ
การกำจัด
ภายหลังการให้ยาทางหลอดเลือดแล้ว ระดับพลาสม่าจะลดลงด้วยครึ่งชีวิตประมาณ 2 ชั่วโมง Ceftaidime ถูกขับออกทางปัสสาวะโดยไม่เปลี่ยนแปลงโดยการกรองไต ประมาณ 80-90% ของขนาดยาจะฟื้นตัวในปัสสาวะภายใน 24 ชั่วโมง ขับออกทางน้ำดีน้อยกว่า 1%
ประชากรผู้ป่วยพิเศษ
การด้อยค่าของไต
การกำจัดเซฟตาซิไดม์จะลดลงในผู้ป่วยที่มีการทำงานของไตบกพร่อง และควรลดขนาดยาลง (ดูหัวข้อ 4.2)
การด้อยค่าของตับ
การปรากฏตัวของความผิดปกติของตับในระดับเล็กน้อยถึงปานกลางไม่มีผลต่อเภสัชจลนศาสตร์ของเซฟตาซิไดม์ในขนาดยาเดี่ยว 2 กรัมทางหลอดเลือดดำทุก 8 ชั่วโมงเป็นเวลา 5 วัน โดยที่การทำงานของไตจะไม่บกพร่อง (ดูหัวข้อ 4.2)
พลเมืองอาวุโส
การกวาดล้างที่ลดลงที่สังเกตได้ในผู้ป่วยสูงอายุส่วนใหญ่เกิดจากการลดลงของ ceftazidime ที่เกี่ยวข้องกับอายุ ค่าเฉลี่ยครึ่งชีวิตในการกำจัดอยู่ระหว่าง 3.5 ถึง 4 ชั่วโมงหลังการให้ครั้งเดียวหรือซ้ำเป็นเวลา 7 วัน 2 ครั้งต่อวัน 2 ก. โดยการฉีดเข้าเส้นเลือดดำ ในผู้ป่วยสูงอายุที่มีอายุ 80 ปีขึ้นไป
ประชากรเด็ก
ครึ่งชีวิตของเซฟตาซิดิมจะยืดเยื้อในทารกที่คลอดก่อนกำหนดและครบกำหนดจาก 4.5 ถึง 7.5 ชั่วโมงหลังจากให้ยา 25 ถึง 30 มก. / กก. อย่างไรก็ตามเมื่ออายุ 2 เดือนครึ่งชีวิตจะอยู่ในค่าสำหรับผู้ใหญ่ .
05.3 ข้อมูลความปลอดภัยพรีคลินิก
ข้อมูลที่ไม่ใช่ทางคลินิกเผยให้เห็นว่าไม่มีอันตรายเป็นพิเศษสำหรับมนุษย์จากการศึกษาทั่วไปของ เภสัชวิทยาความปลอดภัย, ความเป็นพิษเมื่อให้ยาซ้ำ, ความเป็นพิษต่อพันธุกรรม, ความเป็นพิษต่อระบบสืบพันธุ์ ยังไม่มีการศึกษาการก่อมะเร็งด้วยเซฟตาซิไดม์
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
ขวดผง: ปราศจากโซเดียมคาร์บอเนต
หลอดตัวทำละลาย: น้ำสำหรับฉีด
ถุงแช่ประกอบด้วย:
เกลือแกง
น้ำฉีด
06.2 ความเข้ากันไม่ได้
เซฟตาซิดิมสามารถเจือจางในของเหลวแช่ปกติ ยกเว้นสารละลายโซเดียมไบคาร์บอเนตที่มีความเสถียรน้อยกว่า นอกจากนี้ ยาเซฟตาซิดิมต้องไม่ผสมในชุดยาหรือหลอดฉีดยาเดียวกันกับอะมิโนไกลโคไซด์
มีการรายงานการก่อตัวของตะกอนโดยการเพิ่ม vancomycin ลงในสารละลายเซฟาซิดิม หากจำเป็นต้องให้ยาปฏิชีวนะสองตัวนี้ตามลำดับ ขอแนะนำให้ระบายของเหลวในช่องปากในปริมาณที่เพียงพอ เพื่อให้ได้ชุดการแช่ที่เพียงพอระหว่างการบริหารทั้งสองครั้ง
06.3 ระยะเวลาที่ใช้ได้
2 ปี
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
ก่อนทำการสร้างใหม่ ให้เก็บขวดที่ป้องกันแสงไว้
ผลิตภัณฑ์ในสารละลาย หลังจากคืนสภาพด้วยน้ำ p.p.i. o กับของเหลวที่ให้ยาที่เข้ากันได้ (เช่น น้ำเกลือ กลูโคส หรือสารละลายโซเดียมแลคเตท) โดยปกติควรใช้ภายใน 18 ชั่วโมงหากเก็บไว้ที่อุณหภูมิปกติ และภายใน 7 วันหากเก็บไว้ที่อุณหภูมิ 4 องศาเซลเซียส
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
Glazidim 250 มก. ผงสำหรับสารละลายสำหรับฉีด:
• ผง 1 ขวด + หลอดตัวทำละลาย 1 มล.
Glazidim 500 มก. ผงสำหรับสารละลายสำหรับฉีด:
• ผง 1 ขวด + หลอดตัวทำละลาย 1.5 มล.
Glazidim 1 g ผงสำหรับสารละลายสำหรับฉีด:
• ผง 1 ขวด + หลอดตัวทำละลาย 3 มล.
• ผง 1 ขวด + หลอดตัวทำละลาย 10 มล.
Glazidim 1 g ผงสำหรับฉีดหรือแช่:
• แป้ง 10 ขวด
• แป้ง 25 ขวด
Glazidim 2 g ผงสำหรับฉีดหรือแช่:
• แป้ง 1 ขวด
Glazidim บรรจุในขวดแก้วไร้สีประเภทที่ 3 พร้อมฝาอีลาสโตเมอร์และฝาอะลูมิเนียม ตัวทำละลายในขวดแก้วไร้สีประเภทที่ 1
Glazidim 1 g ผงสำหรับสารละลายสำหรับการแช่:
• แป้ง 1 ขวดพร้อมอุปกรณ์ MONOVIAL
• แป้ง 1 ขวดพร้อมอุปกรณ์ MONOVIAL + ถุงแช่ 100 มล.
Glazidim 2 g ผงสำหรับสารละลายสำหรับการแช่:
• แป้ง 1 ขวดพร้อมอุปกรณ์ MONOVIAL
• แป้ง 1 ขวดพร้อมอุปกรณ์ MONOVIAL + ถุงแช่ 100 มล.
Glazidim 1 g และ 2 g ผงสำหรับสารละลายสำหรับการแช่บรรจุในขวดแก้วไร้สีประเภท I พร้อมกับอุปกรณ์ที่ได้รับการจดสิทธิบัตรพิเศษ - MONOVIAL - สำหรับการเตรียมสารละลายแช่ ถุงแช่ที่มีสารละลายทางสรีรวิทยามีความจุ 100 มล.
06.6 คำแนะนำในการใช้งานและการจัดการ
ขวดยา Glazidim ทุกประเภทมีจำหน่ายภายใต้แรงดันที่ลดลง คาร์บอนไดออกไซด์จะถูกปลดปล่อยออกมาและเกิดแรงดันบวกขึ้น ฟองอากาศเล็กๆ ของคาร์บอนไดออกไซด์ในสารละลายที่สร้างขึ้นใหม่นั้นสามารถมองข้ามไปได้
คำแนะนำสำหรับการคืนสภาพ
ดูตารางสำหรับการเติมปริมาตรและความเข้มข้นของสารละลายซึ่งอาจเป็นประโยชน์หากจำเป็นต้องใช้ปริมาณที่เป็นเศษส่วน
* หมายเหตุ: การเพิ่มเติมต้องทำในสองขั้นตอน
สีของสารละลายสามารถเปลี่ยนแปลงได้ตั้งแต่สีเหลืองซีดไปจนถึงสีเหลืองอำพัน ขึ้นอยู่กับความเข้มข้น ชนิดของสารเจือจาง และสภาวะการเก็บรักษาที่ใช้ ภายในกรอบของคำแนะนำที่กำหนดไว้ กิจกรรมของผลิตภัณฑ์จะไม่ได้รับผลกระทบจากการเปลี่ยนแปลงของสีดังกล่าว
เซฟตาซิดิมที่ความเข้มข้น 1 มก. / มล. ถึง 40 มก. / มล. เข้ากันได้กับ:
• โซเดียมคลอไรด์ 9 มก. / มล. (0.9%) สำหรับฉีด
• โซเดียมแลคเตท M / 6 สำหรับฉีด
• โซเดียมแลคเตทคอมพาวนด์สำหรับฉีด (Hartmann's solution)
• เดกซ์โทรส 5% สำหรับฉีด
• โซเดียมคลอไรด์ 0.225% และเดกซ์โทรส 5% สำหรับการฉีด
• โซเดียมคลอไรด์ 0.45% และเดกซ์โทรส 5% สำหรับการฉีด
• โซเดียมคลอไรด์ 0.9% และเดกซ์โทรส 5% สำหรับการฉีด
• โซเดียมคลอไรด์ 0.18% และเดกซ์โทรส 4% สำหรับฉีด
• เดกซ์โทรส 10% สำหรับฉีด
• เดกซ์แทรน 40 10% สำหรับฉีดใน 0.9% โซเดียมคลอไรด์สำหรับฉีด
• เดกซ์ทราน 40 10% สำหรับการฉีด เดกซ์โทรส 5% สำหรับการฉีด
• Dextran 70 6% สำหรับการฉีดโซเดียมคลอไรด์ 0.9% สำหรับการฉีด
• Dextran 70 6% สำหรับการฉีดใน dextrose 5% สำหรับการฉีด
เซฟตาซิดิมที่ความเข้มข้นระหว่าง 0.05 มก. / มล. และ 0.25 มก. / มล. เข้ากันได้กับสารละลายแลคเตทสำหรับการฟอกไตในช่องท้อง
Ceftaidime สามารถสร้างขึ้นใหม่เพื่อใช้ในกล้ามเนื้อด้วย lidocaine hydrochloride 0.5% หรือ 1% สำหรับการฉีด
เนื้อหาของขวดเซฟตาซิดิมขนาด 500 มก. สำหรับฉีด ผสมน้ำ 1.5 มล. สำหรับฉีด สามารถเติมลงในสารละลายเมโทรนิดาโซล (500 มก. ใน 100 มล.) และทั้งสองยังคงออกฤทธิ์
250 มก., ผง 500 มก. สำหรับสารละลายสำหรับฉีด, 1 กรัม, ผง 2 กรัมสำหรับสารละลายสำหรับฉีดหรือแช่
การเตรียมสารละลายสำหรับการฉีดลูกกลอน
1. สอดเข็มฉีดยาผ่านฝาปิดขวดยาและฉีดสารเจือจางตามปริมาณที่แนะนำ การไม่มีอากาศอาจทำให้สารเจือจางเข้าได้ง่ายขึ้น ถอดเข็มฉีดยาออก
2. เขย่าให้ละลาย: ปล่อยก๊าซคาร์บอนไดออกไซด์และจะได้สารละลายที่ชัดเจนใน 1-2 นาที
3. หมุนขวด เมื่อลูกสูบของกระบอกฉีดยาลดระดับลงจนสุด สอดเข็มผ่านช่องเปิดขวดและดึงปริมาตรรวมของสารละลายลงในกระบอกฉีดยา (แรงดันในขวดอาจช่วยให้สำลักได้) ตรวจสอบให้แน่ใจว่าเข็มอยู่ข้างในสารละลายและไม่เข้าไปในช่องว่างด้านบน สารละลาย ที่สำลักอาจมีฟองคาร์บอนไดออกไซด์ขนาดเล็ก สิ่งเหล่านี้สามารถมองข้ามได้
สารละลายเหล่านี้สามารถฉีดเข้าเส้นเลือดโดยตรงหรือฉีดผ่านชุดให้ยา หากผู้ป่วยได้รับของเหลวทางหลอดเลือด เซฟตาซิดิมเข้ากันได้กับของเหลวแช่ที่ใช้บ่อยที่สุด
1 g, 2 g ผงสำหรับสารละลายสำหรับฉีดหรือแช่
การเตรียมสารละลายเซฟาซิดิมให้ทางหลอดเลือดดำสำหรับการฉีดในภาชนะมาตรฐาน (ถุงขนาดเล็กหรือชุดยาชนิดบิวเรตต์)
เตรียมสารละลายโดยใช้สารเจือจางที่เข้ากันได้ 50 มล. (สำหรับขวดขนาด 1 ก. และ 2 ก.) เติมลงใน 2 ขั้นตอนดังนี้
1. ใส่เข็มฉีดยาผ่านฝาปิดขวดและฉีดสารเจือจาง 10 มล. สำหรับขวดขนาด 1 ก. และ 2 ก.
2. ถอนเข็มและเขย่าขวดเพื่อให้สารละลายชัดเจน
3. ห้ามสอดเข็มเพื่อเอาแก๊สออกจนกว่าผลิตภัณฑ์จะละลาย ใส่เข็มเพื่อขจัดก๊าซผ่านฝาปิดขวดเพื่อขจัดแรงดันภายใน
4. ถ่ายสารละลายที่ทำขึ้นใหม่ไปยังอุปกรณ์การบริหารขั้นสุดท้าย (ถุงขนาดเล็กหรือชุดยาฉีดชนิดบิวเรตต์) โดยเตรียมปริมาตรรวมอย่างน้อย 50 มล. และให้ยาทางหลอดเลือดดำเป็นระยะเวลา 15 ถึง 30 นาที
หมายเหตุ: เพื่อรักษาความเป็นหมันของผลิตภัณฑ์ สิ่งสำคัญคือต้องไม่สอดเข็มสำหรับกำจัดแก๊สเข้าไปในช่องเปิดขวดก่อนที่ผลิตภัณฑ์จะละลาย
1 ก., ผง 2 ก. สำหรับสารละลายสำหรับแช่ (พร้อมอุปกรณ์ Monovial)
การเตรียมสารละลายสำหรับการฉีดยาเข้าเส้นเลือดดำ
เนื้อหาของ Monovial จะถูกเพิ่มลงในถุงแช่ขนาดเล็กที่มีโซเดียมคลอไรด์ 0.9% หรือสารละลายเดกซ์โทรส 5% หรือของเหลวแช่อื่นๆ ที่เข้ากันได้
Monovial ขนาด 2 กรัมต้องสร้างขึ้นใหม่โดยใช้ถุงแช่ขนาด 100 มล.
1. ลอกส่วนบนที่ถอดออกได้ของฉลากออกแล้วถอดฝาครอบป้องกันออก
2. ใส่เข็ม Monovial ลงในช่องรับของถุงแช่
3. เพื่อให้สามารถใช้ Monovial ได้ ให้กดที่ครอบเข็มพลาสติกลงไปที่ไหล่ของขวดยาจนกว่าคุณจะได้ยินเสียงคลิก
4. ถือขวดให้ตั้งตรงและเติมให้เต็มประมาณสองในสามโดยการบีบถุงหลายครั้ง
5.เขย่าขวดให้ผงละลาย
6. ฟองเล็กน้อยจะเกิดขึ้นในระหว่างการสร้างใหม่
7. ด้วยขวดที่ด้านบน โอนเซฟตาซิดิมที่ทำขึ้นใหม่ลงในถุงแช่โดยการบีบและปล่อยถุง
8. ทำซ้ำขั้นตอนที่ 4 ถึง 7 เพื่อล้างด้านในขวด ทิ้ง Monovial ที่ว่างเปล่าอย่างปลอดภัย ตรวจสอบให้แน่ใจว่าผงละลายแล้วและถุงไม่รั่วไหล
ยาที่ไม่ได้ใช้และของเสียที่ได้จากยานี้ต้องกำจัดตามระเบียบข้อบังคับของท้องถิ่น
07.0 ผู้ทรงอำนาจการตลาด
แกล็กโซสมิทไคลน์ เอส.พี.เอ. - Via A. Fleming 2, เวโรนา
08.0 หมายเลขอนุญาตการตลาด
GLAZIDIM 250 มก. ผงสำหรับสารละลายสำหรับฉีด
เอไอซี. : 025212010
GLAZIDIM 500 mg Powder สำหรับสารละลายสำหรับฉีด
เอไอซี.: 025212022
GLAZIDIM 1 g ผงสำหรับสารละลายสำหรับฉีด
เอไอซี.: 025212034
เอไอซี.: 025212046
GLAZIDIM 1 g Powder สำหรับสารละลายสำหรับฉีดหรือแช่
A.I.C. : 025212111 (แพ็ค 10 ขวด)
เอ.ไอ.ซี. : 025212123 (กล่อง 25 ขวด)
GLAZIDIM 2 g Powder สำหรับสารละลายสำหรับฉีดหรือแช่
เอไอซี.: 025212059
GLAZIDIM 1 g Powder สำหรับสารละลายสำหรับแช่ด้วยอุปกรณ์ MONOVIAL
เอไอซี.: 025212073
A.I.C. : 025212097 (พร้อมถุงแช่)
GLAZIDIM 2 g Powder สำหรับสารละลายสำหรับแช่ด้วยอุปกรณ์ MONOVIAL
เอไอซี.: 025212085
A.I.C. : 025212109 (พร้อมถุงแช่)
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
10 มีนาคม 2527 / มิถุนายน 2551
10 ธันวาคม 2539 / มิถุนายน 2551 (แพ็คพร้อมอุปกรณ์ MONOVIAL)
10.0 วันที่แก้ไขข้อความ
02 เมษายน 2558