สารออกฤทธิ์: Adalimumab
สารละลาย Humira 40 มก. / 0.8 มล. สำหรับฉีดสำหรับเด็ก
เม็ดมีดแพ็คเกจ Humira มีจำหน่ายสำหรับขนาดบรรจุภัณฑ์:- สารละลาย Humira 40 มก. / 0.8 มล. สำหรับฉีดสำหรับเด็ก
- สารละลาย Humira 40 มก. สำหรับฉีดในหลอดฉีดยาแบบเติมล่วงหน้า
- สารละลาย Humira 40 มก. สำหรับฉีดในกระบอกฉีดยาแบบเติมพร้อมอุปกรณ์ป้องกันเข็ม
- สารละลาย Humira 40 มก. สำหรับฉีดในปากกาที่เติมไว้ล่วงหน้า
ทำไมต้องใช้ Humira? มีไว้เพื่ออะไร?
Humira มีสารออกฤทธิ์ adalimumab ซึ่งเป็นสารกดภูมิคุ้มกันแบบเลือก Humira ได้รับการระบุในการรักษาโรคข้ออักเสบที่ไม่ทราบสาเหตุในเด็กและเยาวชน polyarticular ในเด็กอายุ 2-17 ปี, โรคไขข้ออักเสบที่เกี่ยวข้องกับโรคไขข้ออักเสบในเด็กอายุ 6-17 ปี, โรค Crohn ในเด็กอายุ 6-17 ปี 17 ปีและโรคสะเก็ดเงินจากคราบจุลินทรีย์ในเด็กอายุ 4 ถึง 4 ปี 17 ปี. เป็นยาที่ช่วยลดกระบวนการอักเสบของโรคเหล่านี้ สารออกฤทธิ์ adalimumab เป็นโมโนโคลนอลแอนติบอดีของมนุษย์ที่ผลิตโดยเซลล์เพาะเลี้ยง โมโนโคลนัลแอนติบอดีเป็นโปรตีนที่รับรู้และจับกับโปรตีนอื่นๆ Adalimumab จับกับโปรตีนเฉพาะ (tumor necrosis factor หรือ TNFα) ที่มีอยู่ในระดับสูงในโรคที่มีการอักเสบ เช่น โรคข้ออักเสบที่ไม่ทราบสาเหตุหลายข้อในเด็ก, โรคข้ออักเสบที่เกี่ยวข้องกับการอักเสบ, โรค Crohn และโรคสะเก็ดเงินจากคราบจุลินทรีย์
โรคข้ออักเสบไม่ทราบสาเหตุในเด็กและเยาวชนที่มีหลายข้อและโรคข้ออักเสบที่เกี่ยวข้องกับการอักเสบ
โรคข้ออักเสบไม่ทราบสาเหตุในเด็กและเยาวชนที่มีหลายข้อและโรคข้ออักเสบที่เกี่ยวข้องกับการอักเสบเป็นโรคที่เกิดจากการอักเสบ Humira ใช้ในการรักษาโรคไขข้ออักเสบที่ไม่ทราบสาเหตุเด็กและเยาวชน polyarticular และโรคข้ออักเสบที่เกี่ยวข้องกับการอักเสบ อาจให้ยาแก้ไขโรค เช่น methotrexate เมื่อวินิจฉัย หากการตอบสนองต่อยาเหล่านี้ไม่เพียงพอ เด็กจะได้รับ Humira เพื่อรักษาโรคข้ออักเสบที่ไม่ทราบสาเหตุในเด็กและเยาวชนที่มีหลายข้อหรือข้ออักเสบที่เกี่ยวข้องกับการอักเสบ
โรคโครห์นในเด็ก
โรคโครห์นเป็นโรคที่เกิดจากการอักเสบของระบบทางเดินอาหาร Humira ได้รับการระบุในการรักษาโรค Crohn ในเด็กอายุ 6 ถึง 17 ปี เด็กจะได้รับยาอื่นก่อน หากบุตรของท่านไม่ตอบสนองต่อยาเหล่านี้ได้ดีเพียงพอ เขาหรือเธอจะได้รับ Humira เพื่อลดอาการและอาการของโรคโครห์น
โรคสะเก็ดเงินจากคราบพลัคในเด็ก
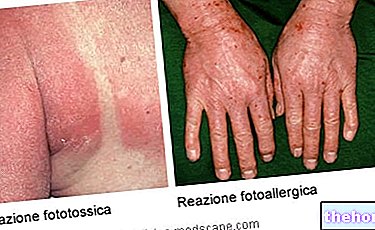
โรคสะเก็ดเงินจากคราบพลัคเป็นภาวะผิวหนังที่ทำให้เกิดรอยแดง เป็นสะเก็ด แข็งของผิวหนังที่ปกคลุมไปด้วยเกล็ดสีเงิน โรคสะเก็ดเงินเกิดจากปัญหาเกี่ยวกับระบบภูมิคุ้มกันของร่างกายซึ่งนำไปสู่การผลิตเซลล์ผิวหนังที่เพิ่มขึ้น Humira ใช้ในการรักษาโรคสะเก็ดเงินจากคราบพลัคที่รุนแรงในเด็กและวัยรุ่นอายุ 4 ถึง 17 ปีที่การบำบัดเฉพาะที่และการส่องไฟไม่ได้ผลอย่างเหมาะสมหรือไม่ได้ระบุไว้
ข้อห้าม เมื่อไม่ควรใช้ Humira
อย่าใช้ Humira
- หากบุตรของท่านแพ้ adalimumab หรือส่วนผสมอื่นใดของยานี้ (ระบุไว้ในหัวข้อ 6)
- หากคุณมี "การติดเชื้อรุนแรง รวมถึงวัณโรค (ดู" คำเตือนและข้อควรระวัง ") ควรแจ้งให้แพทย์ทราบหากบุตรของท่านมีอาการติดเชื้อ เช่น มีไข้ บาดแผล เหนื่อยล้า ปัญหาทางทันตกรรม
- ในภาวะหัวใจล้มเหลวในระดับปานกลางหรือรุนแรง สิ่งสำคัญคือต้องแจ้งให้แพทย์ทราบหากมีหรือมีอาการหัวใจวายร้ายแรง (ดู "คำเตือนและข้อควรระวัง")
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนใช้ Humira
พูดคุยกับแพทย์หรือเภสัชกรของบุตรของท่านก่อนใช้ Humira
- หากคุณมีอาการแพ้ใดๆ ที่มีอาการ เช่น แน่นหน้าอก หายใจมีเสียงหวีด เวียนศีรษะ บวม หรือผื่นขึ้น ให้หยุดให้ Humira และติดต่อแพทย์ของคุณทันที
- หากคุณมีการติดเชื้อ รวมถึงการติดเชื้อระยะยาวหรือเฉพาะที่ (เช่น แผลที่ขา) ให้ปรึกษาแพทย์ก่อนเริ่มการรักษาด้วย Humira หากคุณไม่แน่ใจ ให้ติดต่อแพทย์ของคุณ
- คุณสามารถติดเชื้อได้ง่ายขึ้นในขณะที่รับการรักษาด้วย Humira ความเสี่ยงนี้อาจเพิ่มขึ้นหากการทำงานของปอดของทารกบกพร่อง การติดเชื้อเหล่านี้อาจร้ายแรงและรวมถึงวัณโรค การติดเชื้อที่เกิดจากไวรัส เชื้อรา ปรสิตหรือแบคทีเรีย หรือการติดเชื้อฉวยโอกาสและภาวะติดเชื้อที่อาจเป็นอันตรายถึงชีวิตในบางกรณี สิ่งสำคัญคือต้องแจ้งให้แพทย์ทราบเกี่ยวกับอาการต่างๆ เช่น มีไข้ บาดแผล เหนื่อยล้า หรือมีปัญหาทางทันตกรรม แพทย์ของคุณอาจแนะนำให้หยุด Humira ชั่วคราว
- เนื่องจากมีกรณีของวัณโรคในผู้ป่วยที่ได้รับ Humira แพทย์จะต้องตรวจสอบว่าเด็กมีอาการทั่วไปหรือมีอาการของวัณโรคก่อนเริ่มการรักษาด้วย Humira หรือไม่ สิ่งนี้จะเกี่ยวข้องกับการรวบรวมการประเมินทางการแพทย์โดยละเอียดรวมถึงประวัติทางการแพทย์ของเด็กและการทดสอบทางคลินิกที่เหมาะสม (เช่น เอ็กซ์เรย์ทรวงอกและการทดสอบ tuberculin) ประสิทธิภาพและผลของการทดสอบดังกล่าวจะต้องบันทึกไว้ใน Alert Card สำหรับผู้ป่วย สิ่งสำคัญคือต้องบอกแพทย์ว่าเด็กเคยเป็นวัณโรคหรือเคยสัมผัสใกล้ชิดกับผู้ป่วยวัณโรคหรือไม่ วัณโรคสามารถเกิดขึ้นได้ระหว่างการรักษาแม้ว่าเด็กจะได้รับการรักษาเชิงป้องกันสำหรับวัณโรคก็ตาม ติดต่อแพทย์ของคุณทันทีหากมีอาการของวัณโรค (ไอเรื้อรัง น้ำหนักลด กระสับกระส่าย มีไข้ปานกลาง) หรือการติดเชื้ออื่นๆ ปรากฏขึ้นระหว่างหรือหลังการรักษา
- แจ้งให้แพทย์ทราบหากบุตรของท่านอาศัยอยู่ในหรือเดินทางไปยังบริเวณที่มีการติดเชื้อรา เช่น ฮิสโทพลาสโมซิส โรคบิดคอหรือบลาสโตไมโคซิส เป็นโรคเฉพาะถิ่น
- แจ้งให้แพทย์ทราบหากบุตรของท่านมีการติดเชื้อซ้ำหรือมีเงื่อนไขที่เพิ่มความเสี่ยงของการติดเชื้อ
- แจ้งให้แพทย์ทราบหากบุตรของท่านเป็นพาหะของไวรัสตับอักเสบบี (HBV) หากเขาติดเชื้อไวรัสตับอักเสบบีหรือหากคุณคิดว่าเขาอาจเสี่ยงต่อการติดเชื้อไวรัสตับอักเสบบี แพทย์ต้องทดสอบเด็กเพื่อหาโรคตับอักเสบ การติดเชื้อไวรัสบี การใช้ Humira อาจทำให้ไวรัสตับอักเสบบีกลับมาทำงานอีกครั้งในผู้ที่เป็นพาหะของไวรัสนี้ ในบางกรณีซึ่งพบไม่บ่อยนัก โดยเฉพาะอย่างยิ่งหากผู้ป่วยกำลังรับการรักษาด้วยยาอื่นๆ ที่กดภูมิคุ้มกัน การเปิดใช้งานไวรัสตับอักเสบบีอีกครั้งอาจเป็นอันตรายถึงชีวิตได้
- สิ่งสำคัญคือต้องแจ้งให้แพทย์ของบุตรของท่านทราบหากมีอาการติดเชื้อ เช่น มีไข้ บาดแผล เหนื่อยล้า หรือมีปัญหาทางทันตกรรม
- ก่อนการผ่าตัดหรือทำหัตถการทางทันตกรรม แจ้งแพทย์ว่าบุตรของท่านกำลังใช้ Humira แพทย์ของคุณอาจแนะนำให้ระงับชั่วคราว
- หากบุตรของท่านมีโรคทำลายล้าง เช่น โรคปลอกประสาทเสื่อมแข็ง แพทย์จะเป็นผู้ตัดสินว่าควรเริ่มใช้ Humira หรือไม่
- วัคซีนบางชนิดอาจทำให้เกิดการติดเชื้อได้ และไม่ควรให้ในขณะที่รับการรักษาด้วย Humira ปรึกษาแพทย์ของคุณก่อนที่จะให้วัคซีนแก่บุตรหลานของคุณ ในเด็ก ขอแนะนำให้ใช้ตารางการฉีดวัคซีนตามแผน ตามแนวทางการฉีดวัคซีนปัจจุบัน ก่อนเริ่มการรักษาด้วย Humira หากคุณรับประทาน Humira ในระหว่างตั้งครรภ์ ทารกของคุณอาจมีความเสี่ยงเพิ่มขึ้นในการติดเชื้อนี้ได้นานถึงประมาณ 5 เดือนหลังจากรับประทานยาครั้งสุดท้ายในระหว่างตั้งครรภ์เป็นสิ่งสำคัญที่คุณจะต้องแจ้งให้กุมารแพทย์หรือผู้เชี่ยวชาญด้านสุขภาพคนอื่น ๆ ทราบเกี่ยวกับการใช้ Humira ของคุณในระหว่างตั้งครรภ์ เพื่อที่พวกเขาจะได้ตัดสินใจได้ว่าเมื่อใดที่ลูกน้อยของคุณควรได้รับการฉีดวัคซีนชนิดใดๆ
- ในกรณีของภาวะหัวใจล้มเหลวเล็กน้อยและการรักษาร่วมกับ Humira แพทย์จะต้องประเมินและตรวจสอบสถานะหัวใจของทารกอย่างรอบคอบ สิ่งสำคัญคือต้องแจ้งให้แพทย์ทราบเกี่ยวกับปัญหาหัวใจทั้งในอดีตและปัจจุบัน หากมีอาการใหม่ๆ ของภาวะหัวใจล้มเหลว หรือหากอาการเดิมแย่ลง (เช่น หายใจลำบาก หรือเท้าบวม) ให้ติดต่อแพทย์ทันที แพทย์จะเป็นผู้ตัดสินใจว่าเด็กสามารถรับ Humira ได้หรือไม่
- ในผู้ป่วยบางราย ร่างกายอาจไม่สามารถผลิตเซลล์เม็ดเลือดได้เพียงพอเพื่อช่วยต่อสู้กับการติดเชื้อหรือหยุดเลือดไหล หากบุตรของท่านมีไข้ต่อเนื่อง ฟกช้ำ เลือดออกง่าย หรือซีด ให้ไปพบแพทย์ทันที คนหลังอาจตัดสินใจยุติการรักษา
- เนื้องอกบางประเภทเกิดขึ้นน้อยมากในผู้ป่วย ทั้งเด็กและผู้ใหญ่ ที่ได้รับการรักษาด้วย Humira หรือยาต้าน TNF อื่นๆ ผู้ป่วยที่เป็นโรคข้ออักเสบรูมาตอยด์ชนิดรุนแรงในระยะยาวอาจมีความเสี่ยงที่จะเป็นมะเร็งต่อมน้ำเหลือง (มะเร็งชนิดหนึ่งที่ส่งผลต่อระบบน้ำเหลือง) และมะเร็งเม็ดเลือดขาว (มะเร็งชนิดหนึ่งที่มีผลต่อเลือดและไขกระดูก) สูงกว่าปกติ หากบุตรของท่านใช้ Humira ความเสี่ยงในการเป็นมะเร็งต่อมน้ำเหลือง มะเร็งเม็ดเลือดขาว หรือมะเร็งชนิดอื่นๆ อาจเพิ่มขึ้น ในบางกรณี พบมะเร็งต่อมน้ำเหลืองชนิดรุนแรงและเฉพาะเจาะจงในผู้ป่วยที่ได้รับ Humira ผู้ป่วยบางรายได้รับการรักษาด้วย azathioprine หรือ 6-mercaptopurine บอกแพทย์หากคุณกำลังใช้ azathioprine หรือ 6-mercaptopurine ร่วมกับ Humira นอกจากนี้ ยังพบกรณีของมะเร็งผิวหนังที่ไม่ใช่เมลาโนติกในผู้ป่วยที่ใช้ Humira หากรอยโรคที่ผิวหนังใหม่ปรากฏขึ้นระหว่างหรือหลังการรักษา หรือหากลักษณะของรอยโรคที่มีอยู่เปลี่ยนไป โปรดแจ้งให้แพทย์ทราบ
- นอกจากมะเร็งต่อมน้ำเหลืองแล้ว ยังมีกรณีของมะเร็งในผู้ป่วยโรคปอดชนิดหนึ่งที่เรียกว่าโรคปอดอุดกั้นเรื้อรัง (COPD) ที่ได้รับการรักษาด้วยสารต้าน TNF อีกชนิดหนึ่ง หากบุตรของท่านเป็นโรคปอดอุดกั้นเรื้อรังหรือสูบบุหรี่มาก ท่านควรปรึกษากับแพทย์ว่าการรักษาด้วยยาต้าน TNF นั้นเหมาะสมหรือไม่
เด็กและวัยรุ่น
- การฉีดวัคซีน: ถ้าเป็นไปได้ ลูกของคุณควรจะได้รับการฉีดวัคซีนทั้งหมดก่อนที่จะใช้ Humira
- อย่าให้ Humira แก่เด็กที่เป็นโรคข้ออักเสบไม่ทราบสาเหตุ polyarticular ที่อายุน้อยกว่า 2 ปี
ปฏิกิริยา ยาหรืออาหารชนิดใดที่อาจเปลี่ยนผลกระทบของ Humira
ยาอื่นๆ และ Humira
แจ้งแพทย์หรือเภสัชกรของบุตรของท่านว่าบุตรของท่านกำลังรับประทาน พึ่งรับประทานไปเมื่อเร็วๆ นี้ หรืออาจใช้ยาอื่นใดอยู่
Humira สามารถรับประทานร่วมกับ methotrexate หรือยาแก้โรคไขข้ออื่น ๆ ที่ปรับเปลี่ยนโรคได้ (sulfasalazine, hydroxychloroquine, leflunomide และ parenteral gold salts) สเตียรอยด์หรือยาแก้ปวด รวมทั้งยาต้านการอักเสบที่ไม่ใช่สเตียรอยด์ (NSAIDs)
ไม่ควรใช้ Humira ควบคู่กับยาที่มี anakinra หรือ abatacept เป็นสารออกฤทธิ์ หากคุณไม่แน่ใจ ให้ปรึกษาแพทย์ของคุณ
Humira พร้อมอาหารและเครื่องดื่ม
เนื่องจาก Humira ถูกฉีดเข้าไปใต้ผิวหนัง (ใต้ผิวหนัง) อาหารและเครื่องดื่มจะไม่รบกวนการทำงานของ Humira
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
การตั้งครรภ์และให้นมบุตร
ไม่ทราบผลของ Humira ในหญิงตั้งครรภ์ดังนั้นจึงไม่แนะนำให้ใช้ Humira ในหญิงตั้งครรภ์ ขอแนะนำให้หลีกเลี่ยงการตั้งครรภ์โดยใช้การคุมกำเนิดที่เพียงพอระหว่างการรักษาด้วย Humira และอย่างน้อย 5 เดือนหลังการรักษา "การรักษาด้วยยาครั้งสุดท้าย . หากลูกน้อยของคุณตั้งครรภ์คุณควรไปพบแพทย์ของทารก
ไม่ทราบว่า adalimumab ผ่านเข้าสู่น้ำนมแม่หรือไม่
หากผู้ที่รับประทาน Humira เป็นหญิงสาวที่ให้นมบุตร เธอต้องหยุดให้นมลูกระหว่างการรักษาด้วย Humira และอย่างน้อย 5 เดือนหลังจากการรักษาด้วย Humira ครั้งสุดท้าย หากคุณใช้ยา Humira ในระหว่างตั้งครรภ์ ลูกน้อยของคุณอาจมีความเสี่ยงที่จะติดเชื้อมากขึ้น สิ่งสำคัญคือ คุณต้องแจ้งให้กุมารแพทย์หรือผู้เชี่ยวชาญด้านสุขภาพอื่นๆ ทราบเกี่ยวกับการใช้ Humira ระหว่างตั้งครรภ์ ก่อนที่ลูกน้อยของคุณจะได้รับยาใดๆ ก็ตาม (ดูหัวข้อการฉีดวัคซีนสำหรับข้อมูลเพิ่มเติม)
หากคุณสงสัยว่าลูกสาวของคุณเริ่มตั้งครรภ์หรือกำลังวางแผนที่จะตั้งครรภ์ ให้ปรึกษาแพทย์หรือเภสัชกรเพื่อขอคำแนะนำก่อนใช้ยานี้
การขับรถและการใช้เครื่องจักร
Humira อาจส่งผลต่อความสามารถในการขับรถ ขี่จักรยาน หรือใช้เครื่องจักร แม้ว่าจะเป็นเพียงความสุภาพเท่านั้น หลังจากรับประทาน Humira คุณอาจมีอาการผิดปกติทางสายตาและรู้สึกว่าสภาพแวดล้อมของคุณหมุนไป
ปริมาณและวิธีการใช้ วิธีใช้ Humira: ปริมาณ
ใช้ยานี้ตามที่แพทย์หรือเภสัชกรของบุตรของท่านบอกเสมอ หากมีข้อสงสัย ให้ปรึกษาแพทย์หรือเภสัชกรของบุตรของท่าน
เด็กที่เป็นโรคข้ออักเสบไม่ทราบสาเหตุ polyarticular juvenile
ปริมาณ Humira ที่แนะนำสำหรับผู้ป่วยโรคข้ออักเสบไม่ทราบสาเหตุที่มีหลายข้อในเด็กและเยาวชนอายุ 2 ถึง 12 ปีขึ้นอยู่กับส่วนสูงและน้ำหนักของเด็ก แพทย์ของบุตรของท่านจะแนะนำให้คุณใช้ขนาดยาที่ถูกต้อง อายุ 13-17 ปี 40 มก. ทุกสัปดาห์
เด็กที่เป็นโรคข้ออักเสบที่เกี่ยวข้องกับการอักเสบ
ปริมาณ Humira ที่แนะนำสำหรับผู้ป่วยโรคข้ออักเสบที่เกี่ยวข้องกับโรคไขข้ออักเสบอายุ 6 ถึง 17 ปีขึ้นอยู่กับส่วนสูงและน้ำหนักของเด็ก
เด็กหรือวัยรุ่นที่เป็นโรคโครห์น
เด็กหรือวัยรุ่นที่มีน้ำหนักน้อยกว่า 40 กก.:
ขนาดยาปกติคือ 40 มก. ในช่วงเริ่มต้น ตามด้วย 20 มก. ในอีก 2 สัปดาห์ต่อมา หากต้องการการตอบสนองที่เร็วขึ้น แพทย์อาจกำหนดให้ยาเริ่มต้นคือ 80 มก. (เป็นการฉีดสองครั้งในหนึ่งวัน) ตามด้วย 40 มก. ในอีกสองสัปดาห์ต่อมา . หลังจากนั้นขนาดยาปกติคือ 20 มก. ทุก ๆ สัปดาห์ แพทย์อาจเพิ่มความถี่ของขนาดยาเป็น 20 มก. ทุกสัปดาห์ทั้งนี้ขึ้นอยู่กับการตอบสนองของเด็ก
เด็กหรือวัยรุ่นที่มีน้ำหนักตั้งแต่ 40 กก. ขึ้นไป:
ขนาดยาปกติคือ 80 มก. ในช่วงเริ่มต้น ตามด้วย 40 มก. ในอีก 2 สัปดาห์ต่อมา หากต้องการการตอบสนองที่เร็วขึ้น แพทย์อาจกำหนดขนาดยาเริ่มต้นที่ 160 มก. (ฉีด 4 ครั้งในหนึ่งวันหรือ 2 ครั้งต่อวันเป็นเวลา 2 ครั้ง วันติดต่อกัน) ตามด้วย 80 มก. ในอีกสองสัปดาห์ต่อมา หลังจากนั้น ขนาดยาปกติคือ 40 มก. ทุกสัปดาห์ แพทย์อาจเพิ่มความถี่ในการให้ยาเป็น 40 มก. ทั้งนี้ขึ้นอยู่กับการตอบสนองของเด็ก นอกจากนี้ยังมีปากกาขนาด 40 มก. และหลอดฉีดยาแบบเติมล่วงหน้า 40 มก.
เด็กหรือวัยรุ่นที่เป็นโรคสะเก็ดเงิน
ปริมาณ Humira ที่แนะนำสำหรับผู้ป่วยอายุ 4 ถึง 17 ปีที่เป็นโรคสะเก็ดเงินจากคราบจุลินทรีย์ขึ้นอยู่กับน้ำหนักของเด็ก แพทย์ของบุตรของท่านจะแนะนำให้ท่านใช้ยาในปริมาณที่ถูกต้อง
วิธีการและเส้นทางการบริหาร
Humira ให้โดยการฉีดใต้ผิวหนัง (โดยการฉีดใต้ผิวหนัง)
คำแนะนำในการเตรียมและฉีด Humira:
คำแนะนำต่อไปนี้จะอธิบายวิธีการฉีด Humira อ่านคำแนะนำอย่างละเอียดและปฏิบัติตามทีละขั้นตอน คุณจะได้รับคำแนะนำจากแพทย์หรือผู้ช่วยของเขาเกี่ยวกับเทคนิคการบริหารตนเองและจำนวนเงินที่จะให้กับลูกของคุณ อย่าฉีด จนกว่าคุณจะแน่ใจว่าคุณเข้าใจวิธีการเตรียมและการบริหารงาน หลังจากคำแนะนำที่เหมาะสม คุณสามารถฉีดยาให้โดยคุณหรือผู้อื่น เช่น สมาชิกในครอบครัวหรือเพื่อน
การไม่ปฏิบัติตามคำแนะนำด้านล่างตามที่อธิบายไว้อาจส่งผลให้เกิดการปนเปื้อนซึ่งอาจทำให้เกิดการติดเชื้อในทารกได้ เนื้อหาของเข็มฉีดยาต้องไม่ผสมกับยาอื่น ๆ ในหลอดฉีดยาหรือขวดเดียวกัน
1) การเตรียมการ
- ตรวจสอบให้แน่ใจว่าคุณทราบปริมาณ (ปริมาตร) ที่เหมาะสมสำหรับปริมาณของคุณ หากคุณไม่ทราบจำนวนเงิน ให้หยุดและติดต่อแพทย์เพื่อขอคำแนะนำเพิ่มเติม
- คุณจะต้องมีถังขยะแบบพิเศษ เช่น ภาชนะสำหรับใส่ของมีคมหรือตามที่พยาบาล แพทย์ หรือเภสัชกรกำหนด วางภาชนะไว้บนพื้นผิวที่ทำงานของคุณ
- ล้างมือให้สะอาด
- แกะกล่องที่ประกอบด้วยกระบอกฉีดยา กระบอกฉีดยา กระบอกฉีด แอลกอฮอล์ 2 ก้าน และเข็มฉีดยาออกจากกล่อง หากมีกล่องที่สองในกล่องที่จะใช้สำหรับการบริหารครั้งต่อไป ให้นำกลับไปแช่ตู้เย็นทันที
- ตรวจสอบวันหมดอายุบนกล่อง อย่าใช้สิ่งของใด ๆ ในกล่องหลังจากวันหมดอายุ
- วางสิ่งของต่อไปนี้บนพื้นผิวที่สะอาด โดยไม่ต้องนำสิ่งของใดๆ ออกจากบรรจุภัณฑ์เข็มฉีดยาขนาด 1 มล. หนึ่งขวด อะแดปเตอร์ขวดหนึ่งขวด หนึ่งขวดสำหรับเด็กที่มีสารละลาย Humira สำหรับฉีด แอลกอฮอล์สองแผ่นหรือหนึ่งเข็ม
- Humira เป็นของเหลวใสไม่มีสี ห้ามใช้หากของเหลวทึบแสง เปลี่ยนสี หรือมีตะกอนหรืออนุภาคอยู่ภายใน
2) การเตรียมปริมาณ Humira สำหรับการฉีด
คำแนะนำทั่วไป: ห้ามทิ้งสิ่งของใดๆ จนกว่าการฉีดจะเสร็จสิ้น
- เตรียมเข็มโดยเปิดบรรจุภัณฑ์บางส่วนจากปลายที่ใกล้กับขั้วต่อสีเหลืองของกระบอกฉีดยามากที่สุด เปิดบรรจุภัณฑ์ให้เพียงพอเพื่อให้เห็นขั้วต่อกระบอกฉีดยาสีเหลือง วางหีบห่อโดยให้ด้านสว่างหงายขึ้น
- ถอดฝาพลาสติกออกจากขวดจนกว่าคุณจะเห็นด้านบนของจุกขวด
- ใช้แอลกอฮอล์เช็ดทำความสะอาดฝาขวด ห้ามสัมผัสฝาขวดหลังจากทำความสะอาดด้วยผ้าเช็ดทำความสะอาด
- ถอดฝาครอบออกจากบรรจุภัณฑ์อะแดปเตอร์ขวดโดยไม่ต้องนำออกจากบรรจุภัณฑ์
- ถือขวดโดยคว่ำฝาลง
- โดยที่อะแดปเตอร์เคียวยังคงอยู่ในบรรจุภัณฑ์ใส ให้แนบเข้ากับจุกขวดโดยกดจนกว่าอะแดปเตอร์จะคลิก
- เมื่อคุณแน่ใจว่าได้ต่ออะแดปเตอร์เข้ากับขวดแล้ว ให้ดึงบรรจุภัณฑ์ออกจากขวด
- ค่อยๆ วางขวดยาและอะแดปเตอร์ไว้บนพื้นผิวการทำงานที่สะอาด ระวังอย่าให้ตก ห้ามสัมผัสอะแดปเตอร์
- เตรียมกระบอกฉีดยาโดยเปิดบรรจุภัณฑ์บางส่วนจากปลายใกล้กับลูกสูบสีขาวที่สุด
- เปิดบรรจุภัณฑ์ใสให้เพียงพอเพื่อให้เห็นลูกสูบสีขาวโดยไม่ต้องถอดกระบอกฉีดยาออกจากบรรจุภัณฑ์
- ถือกระบอกฉีดยาไว้ ค่อยๆ ดึงลูกสูบออกมาเหนือปริมาณที่กำหนด 0.1 มล. (เช่น ถ้าขนาดยาที่กำหนดคือ 0.5 มล. ให้ดันลูกสูบไปที่ 0.6 มล.) ไม่เกินตำแหน่งที่สอดคล้องกับ 0.9 มล. โดยไม่คำนึงถึงปริมาณที่กำหนด
- ปริมาตรจะถูกปรับจนถึงปริมาณที่กำหนดในขั้นตอนต่อไป
- อย่าดันลูกสูบสีขาวออกจากกระบอกฉีดยาจนสุด
หมายเหตุ: หากดันลูกสูบสีขาวออกจากกระบอกฉีดยาจนสุด ให้ทิ้งกระบอกฉีดยาและติดต่อผู้จำหน่าย Humira เพื่อขอเปลี่ยน อย่าพยายามใส่ลูกสูบสีขาวกลับเข้าไปใหม่
- อย่าใช้ลูกสูบสีขาวเพื่อถอดกระบอกฉีดยาออกจากบรรจุภัณฑ์ ถือกระบอกฉีดยาด้านที่สำเร็จการศึกษาแล้วนำออกจากบรรจุภัณฑ์ ห้ามวางกระบอกฉีดยาลงเมื่อใดก็ได้
- ขณะจับอะแดปเตอร์ ให้สอดปลายกระบอกฉีดยาเข้าไปในอะแดปเตอร์แล้วหมุนเข็มฉีดยาตามเข็มนาฬิกาด้วยมือเดียวจนสุด ห้ามขันจนแน่นเกินไป
- ขณะถือขวดยา ให้ดันลูกสูบสีขาวเข้าไปจนสุด ขั้นตอนนี้มีความสำคัญสำหรับการได้รับปริมาณที่เหมาะสม ถือก้านลูกสูบสีขาวเข้าแล้วพลิกขวดและหลอดฉีดยากลับด้าน
- ค่อยๆ ดึงลูกสูบสีขาวให้สูงกว่าปริมาณที่กำหนด 0.1 มล. สิ่งสำคัญคือต้องถอนยาที่เหมาะสม ปริมาตรที่เทียบเท่ากับขนาดยาที่กำหนดจะถูกกำหนดในขั้นตอนที่ 4 การเตรียมขนาดยา หากปริมาณที่กำหนดคือ 0.5 มล. ให้ดึงลูกสูบสีขาวเป็นปริมาตร 0.6 มล. ของเหลวจะผ่านจากขวดไปยังหลอดฉีดยา
- ดันลูกสูบสีขาวกลับจนสุดเพื่อดันของเหลวกลับเข้าไปในขวด อีกครั้ง ดึงลูกสูบสีขาวอย่างช้าๆ จนกว่าจะถึง 0.1 มล. เหนือปริมาณที่กำหนด สิ่งสำคัญคือต้องถอนขนาดยาที่เหมาะสมและป้องกันการก่อตัวของฟองอากาศในของเหลวหรือช่องว่าง ปริมาตรที่เทียบเท่ากับปริมาณที่กำหนดจะกำหนดไว้ในขั้นตอนที่ 4 การเตรียมขนาดยา
- หากมีฟองอากาศหรือช่องว่างในกระบอกฉีดยา ให้ทำซ้ำ 3 ครั้ง ห้ามเขย่ากระบอกฉีดยา
หมายเหตุ: หากดันลูกสูบสีขาวออกจากกระบอกฉีดยาจนสุด ให้ทิ้งกระบอกฉีดยาและติดต่อผู้จำหน่าย Humira เพื่อขอเปลี่ยน อย่าพยายามใส่ลูกสูบสีขาวกลับเข้าไปใหม่
- ในขณะที่ยังคงถือกระบอกฉีดยาตั้งตรงที่ด้านที่สำเร็จการศึกษา ให้ถอดอะแดปเตอร์ขวดออกโดยใช้มืออีกข้างหนึ่งคลายเกลียวอะแดปเตอร์ออก ตรวจสอบให้แน่ใจว่าได้ถอดอะแดปเตอร์ขวดออกจากหลอดฉีดยาแล้ว ห้ามสัมผัสปลายกระบอกฉีดยา
- หากคุณสังเกตเห็นฟองอากาศขนาดใหญ่หรือพื้นที่ว่างใกล้กับปลายกระบอกฉีดยา ให้ค่อยๆ ดันลูกสูบสีขาวเข้าไปในกระบอกฉีดยาจนกว่าของเหลวจะเริ่มเข้าสู่ปลายกระบอกฉีดยา อย่าดันลูกสูบสีขาวเมื่อผ่านตำแหน่งการให้ยา
- ตัวอย่างเช่น หากปริมาณที่กำหนดคือ 0.5 มล. อย่าดันลูกสูบสีขาวผ่านตำแหน่ง 0.5 มล.
- ตรวจสอบว่าของเหลวที่เหลืออยู่ในหลอดฉีดยาอย่างน้อยเทียบเท่ากับปริมาณที่ฉีด ถ้าต่ำกว่า อย่าใช้กระบอกฉีดยาและติดต่อผู้เชี่ยวชาญด้านการดูแลสุขภาพของคุณ
- ด้วยมือที่ว่าง หยิบชุดเข็มโดยให้ขั้วต่อกระบอกฉีดยาสีเหลืองคว่ำลง
- ให้เข็มฉีดยาชี้ขึ้นด้านบน สอดปลายกระบอกฉีดยาเข้าไปในขั้วต่อสีเหลืองแล้วหมุนกระบอกฉีดยาตามที่ระบุโดยลูกศรในรูปจนสุด เข็มจะติดอยู่กับกระบอกฉีดยาแล้ว
- นำเข็มออกจากบรรจุภัณฑ์ แต่อย่าถอดฝาเข็มใส
- วางกระบอกฉีดยาบนพื้นผิวที่สะอาด ดำเนินการต่อด้วยไซต์การบริหารและขั้นตอนการเตรียมยาทันที
3) การเลือกและการเตรียมสถานที่ฉีด
- เลือกจุดบนต้นขาหรือหน้าท้องของคุณ: อย่าใช้บริเวณเดียวกับที่ใช้ในการฉีดครั้งสุดท้าย
- ควรฉีดใหม่อย่างน้อย 3 ซม. จากบริเวณที่ฉีดครั้งสุดท้าย
- ห้ามฉีดเข้าไปในบริเวณที่ผิวหนังเป็นสีแดง ช้ำ หรือแข็ง เพราะอาจบ่งชี้ว่ามีการติดเชื้อ ดังนั้นคุณควรติดต่อแพทย์ของคุณ
- เพื่อลดโอกาสในการติดเชื้อ ให้เช็ดบริเวณที่ฉีดด้วยแอลกอฮอล์เช็ดอื่นๆ ห้ามสัมผัสบริเวณนั้นอีกก่อนทำการฉีด
4) การเตรียมยา
- หยิบกระบอกฉีดยาโดยให้เข็มชี้ขึ้น
- ใช้มืออีกข้างหมุนฝาครอบเข็มสีชมพูไปทางกระบอกฉีดยา
- ถอดฝาเข็มใสโดยดึงขึ้นด้วยมืออีกข้างหนึ่ง
- เข็มจะสะอาด
- ห้ามสัมผัสเข็ม
- ห้ามหันกระบอกฉีดยาลงหลังจากที่ถอดฝาเข็มใสออกแล้ว
- อย่าพยายามใส่ฝาใสกลับเข้าไปในเข็ม
- ถือกระบอกฉีดยาที่ระดับสายตาโดยให้เข็มชี้ขึ้นเพื่อดูปริมาณของเหลวอย่างชัดเจน ระวังอย่าให้ยาเข้าตา
- ตรวจสอบปริมาณยาที่คุณกินอีกครั้ง
- ค่อยๆ ดันลูกสูบสีขาวเข้าไปในกระบอกฉีดยาจนกว่ากระบอกฉีดยาจะมีปริมาณยาที่กำหนด ของเหลวส่วนเกินอาจรั่วออกจากเข็มขณะกดลูกสูบ ห้ามถอดเข็มหรือกระบอกฉีดยาออก
การฉีด Humira
- ด้วยมือที่ว่างของคุณ ค่อยๆ นำบริเวณที่แอลกอฮอล์ถูแล้วค้างไว้
- ใช้มืออีกข้างหนึ่งจับกระบอกฉีดยาที่ทำมุม 45 องศากับบริเวณที่ฉีด
- ด้วยการเคลื่อนไหวที่รวดเร็วเพียงครั้งเดียว ดันเข็มทั้งหมดเข้าไปในผิวหนัง
- ปล่อยผิวด้วยมือของคุณ
- ดันลูกสูบสีขาวฉีดยาจนเข็มฉีดยาหมด
- เมื่อเข็มฉีดยาหมด ให้ดึงเข็มออกจากผิวหนังโดยดึงออกในมุมเดียวกับเมื่อสอดเข็มเข้าไป
- ด้วยมือที่ว่างของคุณ ค่อยๆ นำบริเวณที่แอลกอฮอล์ถูแล้วค้างไว้
- ใช้มืออีกข้างหนึ่งจับกระบอกฉีดยาที่ทำมุม 45 องศากับบริเวณที่ฉีด
- ด้วยการเคลื่อนไหวที่รวดเร็วเพียงครั้งเดียว ดันเข็มทั้งหมดเข้าไปในผิวหนัง
- ปล่อยผิวด้วยมือของคุณ
- ดันลูกสูบสีขาวฉีดยาจนเข็มฉีดยาหมด
- เมื่อเข็มฉีดยาหมด ให้เอาเข็มออกจากผิวหนังโดยดึงออกในมุมเดียวกับเมื่อสอดเข็มเข้าไป
- ค่อย ๆ ดึงฝาครอบเข็มสีชมพูขึ้นเหนือเข็มแล้วเปิดออก และวางกระบอกฉีดยากับเข็มบนพื้นผิวการทำงานของคุณ อย่าใส่หมวกใสกลับเข้าไปในเข็ม
- ใช้ผ้ากอซกดบริเวณที่ฉีดเป็นเวลา 10 วินาที อาจมีเลือดออกเล็กน้อย ห้ามนวดบริเวณที่ฉีด หากต้องการให้ใช้โปรแกรมแก้ไข
การกำจัดวัสดุ
- คุณจะต้องมีถังขยะพิเศษ เช่น ภาชนะสำหรับใส่ของมีคม หรือตามคำแนะนำของพยาบาล แพทย์ หรือเภสัชกรของคุณ
- วางกระบอกฉีดยาด้วยเข็ม ขวดแก้ว และอะแดปเตอร์ในภาชนะพิเศษสำหรับของมีคม อย่าวางสิ่งของเหล่านี้ในถังขยะในครัวเรือนของคุณ
- กระบอกฉีดยา เข็ม ขวดเล็ก และอะแดปเตอร์ต้องไม่นำกลับมาใช้ใหม่
- เก็บภาชนะนี้ให้พ้นสายตาและมือเด็กเสมอ
- ทิ้งวัสดุที่ใช้แล้วอื่นๆ ทั้งหมดลงในถังขยะในครัวเรือนของคุณ
ยาเกินขนาด จะทำอย่างไรถ้าคุณได้รับ Humira มากเกินไป
หากคุณใช้ Humira มากกว่าที่ควร:
หากคุณฉีด Humira มากขึ้นโดยไม่ได้ตั้งใจ หรือหากคุณฉีดบ่อยกว่าที่แพทย์สั่ง ให้ติดต่อแพทย์และแจ้งว่าลูกของคุณทานยามากขึ้น เก็บกล่องยาหรือขวดยาไว้เสมอ แม้ว่าจะว่างเปล่าก็ตาม
หากคุณใช้ Humira น้อยกว่าที่ควร:
หากคุณฉีด Humira ให้น้อยลงโดยไม่ได้ตั้งใจ หรือหากคุณฉีดน้อยกว่าที่แพทย์หรือเภสัชกรของลูกคุณกำหนด โปรดติดต่อแพทย์หรือเภสัชกรของลูกคุณและบอกพวกเขาว่าลูกของคุณทานยาน้อยกว่า เก็บกล่องยาหรือขวดยาไว้เสมอ แม้ว่าจะว่างเปล่าก็ตาม
หากคุณลืมใช้ Humira:
หากคุณลืมให้ลูกของคุณฉีด Humira เขาควรฉีดยา Humira ทันทีที่เขาจำได้ จากนั้นให้เด็กทานยาต่อไปอย่างสม่ำเสมอตามกำหนดเวลาที่กำหนด
หากบุตรของท่านหยุดใช้ Humira
การตัดสินใจเลิกใช้ Humira ควรปรึกษากับแพทย์ของเด็ก อาการของเด็กอาจกลับมาหลังจากหยุดใช้ หากคุณมีคำถามเพิ่มเติมเกี่ยวกับการใช้ยานี้ ให้สอบถามแพทย์หรือเภสัชกรของคุณ
ผลข้างเคียงของ Humira คืออะไร?
เช่นเดียวกับยาอื่น ๆ ยานี้อาจทำให้เกิดผลข้างเคียงได้ แม้ว่าจะไม่ใช่ทุกคนที่ได้รับก็ตาม ผลข้างเคียงส่วนใหญ่มีน้อยถึงปานกลาง อย่างไรก็ตาม บางรายอาจรุนแรงและต้องได้รับการรักษา ผลข้างเคียงอาจเกิดขึ้นได้ถึง 4 เดือนหลังจากการฉีด Humira ครั้งสุดท้าย
แจ้งให้แพทย์ทราบทันทีหากคุณสังเกตเห็นปฏิกิริยาใด ๆ ต่อไปนี้:
- ผื่นที่ผิวหนังอย่างรุนแรง ลมพิษหรือสัญญาณอื่น ๆ ของอาการแพ้
- บวมที่ใบหน้า, มือ, เท้า;
- หายใจลำบากกลืนลำบาก
- หายใจถี่ด้วยความพยายามหรือเมื่อนอนราบหรือเท้าบวม
แจ้งให้แพทย์ทราบโดยเร็วที่สุดหากคุณสังเกตเห็นปฏิกิริยาใด ๆ ต่อไปนี้:
- สัญญาณของการติดเชื้อเช่นมีไข้, รู้สึกไม่สบาย, บาดแผล, ปัญหาทางทันตกรรม, แสบร้อนเมื่อปัสสาวะ;
- เหน็ดเหนื่อยเมื่อยล้าหรืออ่อนแรง
- ไอ;
- รู้สึกเสียวซ่า;
- ชา;
- วิสัยทัศน์คู่;
- ความอ่อนแอในแขนหรือขา
- บวมหรือเจ็บเปิดที่ไม่หาย
- อาการและอาการแสดงที่บ่งบอกถึงลักษณะที่ปรากฏของการรบกวนที่ส่งผลต่อระบบเม็ดเลือด เช่น มีไข้ต่อเนื่อง ฟกช้ำ ตกเลือด ซีด
อาการที่อธิบายข้างต้นอาจเป็นสัญญาณของผลข้างเคียงต่อไปนี้ ซึ่งพบได้ใน Humira:
พบบ่อยมาก (อาจส่งผลกระทบมากกว่า 1 ใน 10 คน):
- ปฏิกิริยาบริเวณที่ฉีด (รวมถึงอาการปวด, บวม, แดงหรือคัน);
- การติดเชื้อทางเดินหายใจ (รวมถึงโรคหวัด น้ำมูกไหล ไซนัสอักเสบและปอดบวม);
- ปวดหัว;
- อาการปวดท้อง;
- คลื่นไส้และอาเจียน
- ผื่น;
- ปวดกล้ามเนื้อและกระดูก
สามัญ (อาจส่งผลกระทบมากถึง 1 ใน 10 คน):
- การติดเชื้อรุนแรง (รวมถึงภาวะโลหิตเป็นพิษและไข้หวัดใหญ่);
- การติดเชื้อที่ผิวหนัง (รวมถึงเซลลูไลติและการติดเชื้อเริมงูสวัด);
- การติดเชื้อที่หู;
- การติดเชื้อในช่องปาก (รวมถึงการติดเชื้อที่ฟันและเริม);
- การติดเชื้อของระบบสืบพันธุ์
- การติดเชื้อทางเดินปัสสาวะ;
- การติดเชื้อรา
- การติดเชื้อร่วม
- เนื้องอกที่อ่อนโยน;
- มะเร็งผิวหนัง;
- ปฏิกิริยาการแพ้ (รวมถึงการแพ้ตามฤดูกาล);
- การคายน้ำ;
- การเปลี่ยนแปลงทางอารมณ์ (รวมถึงภาวะซึมเศร้า);
- ความวิตกกังวล;
- ความผิดปกติของการนอนหลับ
- ความผิดปกติของความไวเช่นรู้สึกเสียวซ่า, กระตุกหรือชา;
- ไมเกรน;
- การกดทับของรากประสาท (รวมถึงอาการปวดหลังส่วนล่างและปวดขา);
- การรบกวนทางสายตา
- ตาอักเสบ;
- การอักเสบของเปลือกตาและตาบวม;
- อาการวิงเวียนศีรษะ
- ความรู้สึกของการเต้นของหัวใจอย่างรวดเร็ว
- ความดันโลหิตสูง
- ร้อนวูบวาบ;
- ห้อ;
- ไอ;
- โรคหอบหืด;
- หายใจถี่;
- เลือดออกในทางเดินอาหาร;
- อาการอาหารไม่ย่อย (ไม่ย่อย, ท้องอืด, อิจฉาริษยา);
- โรคกรดไหลย้อน;
- ซิกก้าซินโดรม (รวมถึงตาแห้งและปากแห้ง);
- คัน;
- ผื่นคัน;
- ช้ำ;
- การอักเสบของผิวหนัง (เช่นกลาก);
- การทำลายเล็บของนิ้วมือและนิ้วเท้า
- เหงื่อออกเพิ่มขึ้น
- ผมร่วง;
- เริ่มมีอาการหรือเลวลงของโรคสะเก็ดเงิน;
- กล้ามเนื้อกระตุก;
- เลือดในปัสสาวะ
- ปัญหาไต
- อาการเจ็บหน้าอก;
- บวมน้ำ;
- ไข้;
- การลดลงของเกล็ดเลือดใน sanggue ซึ่งเพิ่มความเสี่ยงของการมีเลือดออกหรือช้ำ;
- ความยากลำบากในการรักษา
ผิดปกติ (อาจส่งผลกระทบมากถึง 1 ใน 100 คน):
- การติดเชื้อฉวยโอกาส (ซึ่งรวมถึงวัณโรคและการติดเชื้ออื่น ๆ ที่เกิดขึ้นเมื่อภูมิคุ้มกันลดลง);
- การติดเชื้อทางระบบประสาท (รวมถึงเยื่อหุ้มสมองอักเสบจากไวรัส);
- การติดเชื้อที่ตา;
- การติดเชื้อแบคทีเรีย
- diverticulitis (การอักเสบและการติดเชื้อของลำไส้ใหญ่);
- เนื้องอก;
- เนื้องอกของระบบน้ำเหลือง
- เนื้องอก;
- ความผิดปกติของระบบภูมิคุ้มกันที่อาจส่งผลต่อปอด ผิวหนัง และต่อมน้ำเหลือง (โดยทั่วไปมักแสดงเป็น Sarcoidosis);
- vasculitis (การอักเสบของหลอดเลือด);
- ตัวสั่น;
- จังหวะ;
- โรคระบบประสาท;
- วิสัยทัศน์คู่;
- สูญเสียการได้ยิน, เสียงเรียกเข้า;
- ความรู้สึกของการเต้นของหัวใจผิดปกติเช่นใจสั่น;
- ปัญหาหัวใจซึ่งอาจทำให้หายใจถี่หรือข้อเท้าบวม
- กล้ามเนื้อหัวใจตายเฉียบพลัน
- การก่อตัวของถุงในผนังของหลอดเลือดแดงหลัก, การอักเสบและก้อนในหลอดเลือดดำ, การอุดตันของหลอดเลือด;
- โรคปอดทำให้หายใจถี่ (รวมถึงการอักเสบ);
- เส้นเลือดอุดตันที่ปอด (การอุดตันของหลอดเลือดแดงในปอด);
- เยื่อหุ้มปอด (การสะสมของของเหลวในพื้นที่เยื่อหุ้มปอดผิดปกติ);
- การอักเสบของตับอ่อนทำให้เกิดอาการปวดอย่างรุนแรงในช่องท้องและหลัง
- กลืนลำบาก;
- อาการบวมน้ำบนใบหน้า;
- การอักเสบของถุงน้ำดี, นิ่วในถุงน้ำดี;
- ตับไขมัน
- เหงื่อออกตอนกลางคืน;
- แผลเป็น;
- การเผาผลาญของกล้ามเนื้อผิดปกติ
- systemic lupus erythematosus (รวมถึงการอักเสบของผิวหนัง หัวใจ ปอด ข้อต่อ และอวัยวะอื่นๆ)
- ขัดจังหวะการนอนหลับ;
- ความอ่อนแอ;
- การอักเสบ
หายาก (อาจส่งผลกระทบมากถึง 1 ใน 1,000 คน):
- มะเร็งเม็ดเลือดขาว (เนื้องอกร้ายที่มีผลต่อระบบเม็ดเลือดในระดับต่อพ่วง (เลือด) และไขกระดูก);
- อาการแพ้อย่างรุนแรงเมื่อช็อก
- หลายเส้นโลหิตตีบ;
- ความผิดปกติทางระบบประสาท (เช่น การอักเสบของเส้นประสาทตาและกลุ่มอาการกิลแลง-บาร์เร ซึ่งอาจทำให้กล้ามเนื้ออ่อนแรง ความรู้สึกผิดปกติ รู้สึกเสียวซ่าที่แขนและร่างกายส่วนบน)
- หัวใจหยุดเต้น;
- พังผืดในปอด (แผลเป็นจากปอด);
- การเจาะลำไส้
- โรคตับอักเสบ;
- การเปิดใช้งานใหม่ของไวรัสตับอักเสบบี;
- autoimmune hepatitis (การอักเสบของตับที่เกิดจากระบบภูมิคุ้มกันของคุณเอง);
- vasculitis ผิวหนัง (การอักเสบของหลอดเลือดในผิวหนัง);
- กลุ่มอาการสตีเวนส์-จอห์นสัน (อาการเริ่มแรก ได้แก่ ไม่สบายตัว มีไข้ ปวดศีรษะ และมีผื่นขึ้น)
- อาการบวมน้ำบนใบหน้าที่เกี่ยวข้องกับอาการแพ้
- erythema multiforme (ผื่นผิวหนังอักเสบ);
- โรคลูปัสเหมือน
ไม่ทราบ (ความถี่ไม่สามารถประมาณจากข้อมูลที่มีอยู่):
- มะเร็งต่อมน้ำเหลือง T-cell hepato-splenic (มะเร็งเม็ดเลือดที่หายากซึ่งมักเป็นอันตรายถึงชีวิต);
- มะเร็งเซลล์ Merkel (มะเร็งผิวหนังชนิดหนึ่ง);
- ตับวาย;
- ภาวะที่เรียกว่าโรคผิวหนังอักเสบ (dermatomyositis) แย่ลง (แสดงเป็นผื่นพร้อมกับกล้ามเนื้ออ่อนแรง)
ผลข้างเคียงบางอย่างที่เห็นได้จาก Humira อาจไม่แสดงอาการและสามารถพบได้ในการตรวจเลือดเท่านั้น ซึ่งรวมถึง:
พบบ่อยมาก (อาจส่งผลกระทบมากกว่า 1 ใน 10 คน):
- จำนวนเม็ดเลือดขาวต่ำ
- จำนวนเม็ดเลือดแดงต่ำ
- ไขมันในเลือดเพิ่มขึ้น
- เอนไซม์ตับเพิ่มขึ้น
สามัญ (อาจส่งผลกระทบมากถึง 1 ใน 10 คน):
- เพิ่มจำนวนเม็ดเลือดขาว
- ลดจำนวนเกล็ดเลือด;
- เพิ่มกรดยูริกในเลือด
- การเปลี่ยนแปลงของโซเดียมในเลือด
- การลดแคลเซียมในเลือด
- การลดลงของฟอสฟอรัสในเลือด
- น้ำตาลในเลือดเพิ่มขึ้น
- เพิ่มแลคเตทดีไฮโดรจีเนสในเลือด
- การปรากฏตัวของ autoantibodies ในเลือด
หายาก (อาจส่งผลกระทบมากถึง 1 ใน 1,000 คน):
- จำนวนเม็ดเลือดขาว เม็ดเลือดแดง และเกล็ดเลือดต่ำ
ไม่ทราบ (ความถี่ไม่สามารถประมาณจากข้อมูลที่มีอยู่):
- ตับวาย
การรายงานผลข้างเคียง
หากบุตรของท่านได้รับผลข้างเคียงใด ๆ ให้ปรึกษาแพทย์หรือเภสัชกรของบุตรของท่าน ซึ่งรวมถึงผลข้างเคียงที่อาจเกิดขึ้นซึ่งไม่ได้ระบุไว้ในเอกสารฉบับนี้ คุณยังสามารถรายงานผลข้างเคียงได้โดยตรงผ่านระบบการรายงานระดับประเทศที่ระบุไว้ในภาคผนวก 5 โดยการรายงานผลข้างเคียง คุณสามารถช่วยให้ข้อมูลเพิ่มเติมเกี่ยวกับความปลอดภัยของยานี้ได้
การหมดอายุและการเก็บรักษา
เก็บยานี้ให้พ้นสายตาและมือเด็ก
อย่าใช้ยานี้หลังจากวันหมดอายุซึ่งระบุไว้บนฉลาก / ตุ่ม / กล่องหลังจาก EXP วันหมดอายุหมายถึงวันสุดท้ายของเดือนนั้น
เก็บในตู้เย็น (2 ° C - 8 ° C) อย่าแช่แข็ง
เก็บขวดยาไว้ในบรรจุภัณฑ์ที่เหมาะสมเพื่อป้องกันยาจากแสง
อย่าทิ้งยาผ่านทางน้ำเสียหรือของเสียในครัวเรือน ถามแพทย์หรือเภสัชกรว่าจะทิ้งยาที่คุณไม่ได้ใช้แล้วอย่างไร ซึ่งจะช่วยปกป้องสิ่งแวดล้อม
องค์ประกอบและรูปแบบยา
สิ่งที่ Humira ประกอบด้วย
สารออกฤทธิ์คือ adalimumab
ส่วนผสมอื่นๆ ได้แก่ แมนนิทอล กรดซิตริกโมโนไฮเดรต โซเดียมซิเตรต โซเดียมไดไฮโดรเจนฟอสเฟตไดไฮเดรต ไดโซเดียมฟอสเฟตไดไฮเดรต โซเดียมคลอไรด์ โพลีซอร์เบต 80 โซเดียมไฮดรอกไซด์ และน้ำสำหรับฉีด
ยานี้มีโซเดียมน้อยกว่า 1 มิลลิโมล (23 มก.) ต่อขนาดยา 0.8 มล. ดังนั้นจึงเป็น 'ปราศจากโซเดียม' และไม่มีสารกันบูด
ขวด Humira มีลักษณะอย่างไรและเนื้อหาของแพ็ค
สารละลาย Humira 40 มก. สำหรับฉีดในขวดเป็นสารละลายปลอดเชื้อของ adalimumab 40 มก. ละลายในสารละลาย 0.8 มล.
ขวด Humira ประกอบด้วยสารละลาย adalimumab ที่มีอยู่ในขวดแก้ว หนึ่งแพ็คมี 2 กล่อง แต่ละกล่องประกอบด้วย 1 ขวด, เข็มฉีดยาที่ปราศจากเชื้อ 1 อัน, เข็ม 1 อัน, อะแดปเตอร์ขวด 1 อันและสำลีแอลกอฮอล์ 2 อัน
Humira ยังมีอยู่ในหลอดฉีดยาแบบเติมล่วงหน้าหรือปากกาแบบเติมล่วงหน้า
+ เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่นำเสนออาจไม่ใช่ข้อมูลล่าสุด
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
HUMIRA 40 MG / 0.8 ML SOLUTION สำหรับการฉีดเพื่อการใช้งานในเด็ก
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
ขวดขนาดเดียว 0.8 มล. ประกอบด้วย adalimumab 40 มก.
Adalimumab เป็นโมโนโคลนอลแอนติบอดีของมนุษย์ลูกผสมที่แสดงออกในเซลล์รังไข่หนูแฮมสเตอร์จีน
สำหรับรายการสารปรุงแต่งทั้งหมด โปรดดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
น้ำยาล้างสำหรับฉีด
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
โรคข้ออักเสบไม่ทราบสาเหตุเด็กและเยาวชน
โรคข้ออักเสบไม่ทราบสาเหตุในเด็กและเยาวชนหลายข้อ
Humira ร่วมกับ methotrexate ได้รับการระบุในการรักษาโรคข้ออักเสบไม่ทราบสาเหตุในเด็กและเยาวชนที่เป็นโรค polyarticular ในผู้ป่วยอายุ 2 ปีที่มีการตอบสนองต่อยาต้านรูมาติก (DMARDs) ที่ปรับเปลี่ยนโรคได้อย่างน้อยหนึ่งชนิด Humira อาจใช้เป็นยาเดี่ยว ในกรณีที่ไม่สามารถทนต่อยา methotrexate หรือเมื่อยังคงรักษาด้วย methotrexate นั้นไม่เหมาะสม (สำหรับประสิทธิภาพในการรักษาด้วยยาเดี่ยว ดูหัวข้อ 5.1) Humira ไม่ได้รับการศึกษาในผู้ป่วยที่อายุน้อยกว่า 2 ปี
โรคข้ออักเสบที่เกี่ยวข้องกับ enthesitis
Humira ได้รับการระบุในการรักษาโรคข้ออักเสบที่เกี่ยวข้องกับโรคไขข้ออักเสบในผู้ป่วยอายุ 6 ขวบที่มีการตอบสนองไม่เพียงพอหรือไม่ทนต่อการรักษาแบบเดิม (ดูหัวข้อ 5.1)
โรคโครห์นในผู้ป่วยเด็ก
Humira ได้รับการระบุในการรักษาโรค Crohn's ที่รุนแรงในผู้ป่วยเด็ก (อายุ 6 ปี) ที่มีการตอบสนองต่อการรักษาแบบเดิมไม่เพียงพอรวมถึงการบำบัดทางโภชนาการเบื้องต้น การรักษาด้วย corticosteroid และ immunomodulator หรือผู้ที่ไม่อดทนหรือมีข้อห้าม การบำบัดดังกล่าว
04.2 วิทยาและวิธีการบริหาร
ปริมาณ
การบำบัดด้วย Humira ควรเริ่มต้นและตรวจสอบโดยแพทย์ผู้เชี่ยวชาญที่มีประสบการณ์ในการวินิจฉัยและการรักษาสภาพที่ระบุ Humira ผู้ป่วยที่รักษาด้วย Humira จะต้องได้รับการ์ดแจ้งเตือนพิเศษ
หลังจากคำแนะนำที่ถูกต้องเกี่ยวกับเทคนิคการฉีด Humira ผู้ป่วยสามารถฉีดยาเองได้หากแพทย์เห็นว่าเหมาะสมและต้องตรวจสุขภาพเป็นระยะตามความจำเป็น
ประชากรเด็ก
โรคข้ออักเสบไม่ทราบสาเหตุเด็กและเยาวชน
โรคข้ออักเสบไม่ทราบสาเหตุในเด็กและเยาวชน Polyarticular อายุ 2 ถึง 12 ปี
ปริมาณ Humira ที่แนะนำสำหรับผู้ป่วยโรคข้ออักเสบไม่ทราบสาเหตุ polyarticular อายุ 2 ถึง 12 ปีคือ 24 มก. / ตร.ม. พื้นที่ผิวกายสูงสุด 20 มก. ของ adalimumab (สำหรับผู้ป่วยอายุ 2 ปีฉีดเข้าใต้ผิวหนัง ปริมาตร d " ฉีดถูกเลือก ขึ้นอยู่กับส่วนสูงและน้ำหนักของผู้ป่วย (ตารางที่ 1)
ตารางที่ 1. ปริมาณ Humira ในหน่วยมิลลิลิตร (มล.) โดยความสูงและน้ำหนักของผู้ป่วยที่เป็นโรคข้ออักเสบและข้ออักเสบที่ไม่ทราบสาเหตุจาก polyarticular และโรคข้ออักเสบที่เกี่ยวข้องกับโรคไข้สมองอักเสบ
* ปริมาณสูงสุดครั้งเดียวคือ 40 มก. (0.8 มล.)
โรคข้ออักเสบที่ไม่ทราบสาเหตุในเด็กและเยาวชนหลายข้อตั้งแต่อายุ 13 ปี
สำหรับผู้ป่วยอายุ 13 ปีขึ้นไป จะได้รับยา 40 มก. ทุกสัปดาห์เว้นสัปดาห์โดยไม่คำนึงถึงพื้นที่ผิวกาย
สำหรับผู้ป่วยดังกล่าว ยังมีปากกาขนาด 40 มก. และเข็มฉีดยาที่เติมไว้ล่วงหน้า 40 มก. สำหรับการให้ยาเต็มขนาด 40 มก.
ข้อมูลที่มีอยู่แนะนำว่าการตอบสนองทางคลินิกมักจะทำได้ภายใน 12 สัปดาห์ของการรักษา ในผู้ป่วยที่ตอบสนองต่อการรักษาไม่เพียงพอภายในช่วงเวลานี้ ควรพิจารณาความจำเป็นในการรักษาอย่างต่อเนื่อง
ไม่มีการใช้ Humira ที่เกี่ยวข้องในผู้ป่วยที่อายุน้อยกว่า 2 ปีในข้อบ่งชี้นี้
โรคข้ออักเสบที่เกี่ยวข้องกับ enthesitis
ปริมาณที่แนะนำของ Humira ในผู้ป่วยที่เป็นโรคข้ออักเสบที่เกี่ยวข้องกับโรคไขข้ออักเสบซึ่งมีอายุ 6 ปีขึ้นไปคือพื้นที่ผิวกาย 24 มก. / ตร.ม. สูงสุด 40 มก. เดียวที่ฉีดทุกสัปดาห์โดยการฉีดใต้ผิวหนัง ปริมาณการฉีดจะถูกเลือกตามความสูงและน้ำหนักของผู้ป่วย (ตารางที่ 1)
Humira ไม่ได้รับการศึกษาในผู้ป่วยที่อายุน้อยกว่า 6 ปีที่เป็นโรคข้ออักเสบจากการอักเสบ
โรคโครห์นในผู้ป่วยเด็ก
โรคโครห์นในผู้ป่วยเด็ก
ปริมาณที่แนะนำของ Humira ในเด็กที่เป็นโรค Crohn ที่รุนแรงคือ 40 มก. ในสัปดาห์ที่ 0 ตามด้วย 20 มก. ในสัปดาห์ที่ 2 หากต้องการการตอบสนองอย่างรวดเร็วต่อการรักษาสามารถใช้สูตร 80 มก. ในสัปดาห์ที่ 0 ได้ ( สามารถให้ขนาดยาเป็นการฉีดสองครั้งในหนึ่งวัน) และ 40 มก. ในสัปดาห์ที่ 2 โดยเข้าใจว่าความเสี่ยงของเหตุการณ์ไม่พึงประสงค์อาจสูงขึ้นเมื่อใช้ขนาดยาเหนี่ยวนำที่สูงกว่า
หลังการรักษาแบบเหนี่ยวนำ ขนาดยาที่แนะนำคือ 20 มก. ทุกสัปดาห์โดยการฉีดใต้ผิวหนัง บุคคลบางคนที่มีการตอบสนองไม่เพียงพออาจได้รับประโยชน์จากการเพิ่มความถี่ของขนาดยาเป็น Humira 20 มก. ทุกสัปดาห์
โรคโครห์นในผู้ป่วยเด็ก ≥ 40 กก.:
ปริมาณที่แนะนำของ Humira ในเด็กที่เป็นโรค Crohn รุนแรงคือ 80 มก. ในสัปดาห์ที่ 0 ตามด้วย 40 มก. ในสัปดาห์ที่ 2 หากต้องการการตอบสนองอย่างรวดเร็วต่อการรักษาสามารถใช้สูตร 160 มก. ในสัปดาห์ที่ 0 ได้ ( ขนาดยาสามารถฉีดได้ 4 ครั้งในหนึ่งวันหรือฉีดสองครั้งต่อวันเป็นเวลาสองวันติดต่อกัน) และ 80 มก. ในสัปดาห์ที่ 2 โดยเข้าใจว่าความเสี่ยงของเหตุการณ์ไม่พึงประสงค์อาจสูงขึ้นด้วยการใช้ยาที่สูงกว่า การเหนี่ยวนำ
หลังการรักษาแบบเหนี่ยวนำ ขนาดยาที่แนะนำคือ 40 มก. ทุกสัปดาห์โดยการฉีดใต้ผิวหนัง บุคคลบางคนที่มีการตอบสนองไม่เพียงพออาจได้รับประโยชน์จากการเพิ่มความถี่ของขนาดยาเป็น Humira 40 มก. ในแต่ละสัปดาห์
การรักษาต่อเนื่องควรพิจารณาอย่างรอบคอบในเรื่องที่ไม่ตอบสนองในสัปดาห์ที่ 12
นอกจากนี้ยังมีปากกาขนาด 40 มก. และเข็มฉีดยาที่เติมไว้ล่วงหน้าขนาด 40 มก. สำหรับผู้ป่วยที่ต้องการขนาดยาครบ 40 มก.
ไม่มีการใช้ Humira ที่เกี่ยวข้องในเด็กอายุต่ำกว่า 6 ปีในการบ่งชี้นี้
ไตและ / หรือตับไม่เพียงพอ
Humira ไม่ได้รับการศึกษาในประชากรประเภทนี้ ไม่สามารถให้คำแนะนำในการใช้ยาได้
วิธีการบริหาร
Humira ให้โดยการฉีดใต้ผิวหนัง คำแนะนำการใช้งานฉบับเต็มมีอยู่ในแผ่นพับบรรจุภัณฑ์
04.3 ข้อห้าม
ภูมิไวเกินต่อสารออกฤทธิ์หรือสารเพิ่มปริมาณใด ๆ ที่ระบุไว้ในหัวข้อ 6.1
วัณโรคที่ใช้งานอยู่หรือการติดเชื้อร้ายแรงอื่นๆ เช่น ภาวะติดเชื้อและการติดเชื้อฉวยโอกาส (ดูหัวข้อ 4.4)
ภาวะหัวใจล้มเหลวปานกลางถึงรุนแรง (NYHA class III / IV) (ดูหัวข้อ 4.4)
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
เพื่อปรับปรุงการตรวจสอบย้อนกลับของผลิตภัณฑ์ยาชีวภาพ ควรบันทึกเครื่องหมายการค้าและหมายเลขชุดของผลิตภัณฑ์ที่ให้ยาอย่างชัดเจน (หรือทำเครื่องหมาย)
การติดเชื้อ
ผู้ป่วยที่ได้รับการรักษาด้วย TNF antagonists จะไวต่อการติดเชื้อรุนแรงมากกว่า การทำงานของปอดบกพร่องอาจเพิ่มความเสี่ยงในการติดเชื้อ ดังนั้นผู้ป่วยควรได้รับการตรวจคัดกรองการติดเชื้ออย่างถี่ถ้วน รวมทั้งวัณโรค ก่อน ระหว่าง และหลังการรักษาด้วย Humira เนื่องจากการกำจัด adalimumab อาจใช้เวลานานถึงสี่เดือน ควรติดตามตรวจสอบต่อไปในช่วงเวลานี้
ไม่ควรเริ่มการบำบัดด้วย Humira ในผู้ป่วยที่ติดเชื้อ รวมถึงการติดเชื้อเรื้อรังหรือเฉพาะที่ จนกว่าสิ่งเหล่านี้จะอยู่ภายใต้การควบคุม ในผู้ป่วยที่เคยสัมผัสกับวัณโรคและในผู้ป่วยที่ได้เดินทางไปยังบริเวณที่มีความเสี่ยงสูงต่อวัณโรคหรือโรคติดเชื้อราเฉพาะถิ่น เช่น ฮิสโตพลาสโมซิส, โรคบิดบิดหรือบลาสโตมัยโคซิส ควรพิจารณาความเสี่ยงและประโยชน์ของการรักษาด้วย Humira ก่อนเริ่มการรักษา (เพื่อดู การติดเชื้อฉวยโอกาสอื่นๆ).
ผู้ป่วยที่ติดเชื้อใหม่ในระหว่างการรักษาด้วย Humira ควรได้รับการติดตามอย่างใกล้ชิดและได้รับการประเมินการวินิจฉัยอย่างเต็มรูปแบบ หากมีการติดเชื้อรุนแรงหรือภาวะติดเชื้อรุนแรงขึ้นใหม่ ควรหยุดใช้ Humira และใช้ยาต้านจุลชีพหรือเชื้อราที่เหมาะสมจนกว่าจะมีการควบคุมการติดเชื้อ แพทย์ควรใช้ความระมัดระวังเมื่อใช้ Humira ในผู้ป่วยที่มีประวัติการติดเชื้อซ้ำหรือมีอาการร่วมที่อาจ จูงใจผู้ป่วยให้ติดเชื้อรวมถึงการใช้ยาภูมิคุ้มกันร่วมกัน
การติดเชื้อรุนแรง:
มีรายงานการติดเชื้อร้ายแรง รวมทั้งภาวะติดเชื้อที่เกิดจากแบคทีเรีย มัยโคแบคทีเรีย เชื้อราที่แพร่กระจาย ปรสิต ไวรัส หรือการติดเชื้อฉวยโอกาสอื่นๆ เช่น ลิสเทอริโอซิส ลีเจียนเนลโลซิส และปอดบวม ในผู้ป่วยที่รักษาด้วย Humira
การติดเชื้อร้ายแรงอื่น ๆ ที่พบในการทดลองทางคลินิก ได้แก่ โรคปอดบวม pyelonephritis โรคข้ออักเสบติดเชื้อและภาวะโลหิตเป็นพิษ มีรายงานกรณีการรักษาตัวในโรงพยาบาลหรือเหตุการณ์ร้ายแรงที่เกี่ยวข้องกับการติดเชื้อ
วัณโรค:
มีรายงานผู้ป่วยที่ใช้ Humira ว่าวัณโรค รวมถึงการกระตุ้นใหม่และการเริ่มเป็นวัณโรคครั้งใหม่ มีรายงานกรณีของวัณโรคในปอดและนอกปอด (เช่น แพร่ระบาด)
ก่อนเริ่มการบำบัดด้วย Humira ผู้ป่วยทุกรายควรได้รับการตรวจคัดกรองการมีวัณโรคที่ใช้งานอยู่หรือไม่ใช้งาน ("แฝง") การประเมินนี้ควรรวมถึง "ประวัติทางการแพทย์โดยละเอียดของผู้ป่วยที่มีประวัติวัณโรคหรือการสัมผัสใด ๆ กับผู้ที่เป็นวัณโรคที่ใช้งานอยู่และด้วยการบำบัดด้วยภูมิคุ้มกันก่อนหน้านี้และ / หรือร่วมกัน การตรวจคัดกรองที่เหมาะสม (เช่นการทดสอบผิวหนังที่ tuberculin และทรวงอก X-ray ) ในผู้ป่วยทุกราย (อาจปฏิบัติตามแนวทางท้องถิ่น) ขอแนะนำให้ทำการทดสอบเหล่านี้และบันทึกผลลัพธ์ไว้ในการ์ดแจ้งเตือนผู้ป่วย แพทย์ควรตื่นตัวต่อความเสี่ยงของผลการทดสอบผิวหนัง tuberculin เชิงลบโดยเฉพาะอย่างยิ่งในผู้ป่วยที่ป่วยหนักหรือมีภูมิคุ้มกันบกพร่อง
หากตรวจพบวัณโรคที่ออกฤทธิ์ จะต้องไม่เริ่มการบำบัดด้วย Humira (ดูหัวข้อ 4.3)
ในทุกสถานการณ์ที่อธิบายไว้ด้านล่าง ควรทำการประเมินอย่างรอบคอบเกี่ยวกับอัตราส่วนความเสี่ยง/ผลประโยชน์ของการรักษาด้วย Humira
หากสงสัยว่าเป็นวัณโรคแฝง แนะนำให้ปรึกษาแพทย์ที่เชี่ยวชาญในการรักษาวัณโรค
หากมีการวินิจฉัยวัณโรคที่แฝงอยู่ ควรให้การรักษาด้วยยาต้านวัณโรคตามคำแนะนำของท้องถิ่นก่อนเริ่มการรักษาด้วย Humira
ควรพิจารณาสถาบันการรักษาป้องกันวัณโรคก่อนเริ่มการรักษาด้วย Humira ในผู้ป่วยที่มีปัจจัยเสี่ยงที่แตกต่างกันหรือมีนัยสำคัญสำหรับวัณโรค แม้จะมีการทดสอบเป็นลบสำหรับวัณโรค และในผู้ป่วยที่ประวัติทางการแพทย์แสดงประวัติส่วนตัวของวัณโรคแฝงหรือที่ใช้งานอยู่ใน ซึ่งไม่สามารถยืนยันได้ว่าการรักษาที่ได้รับนั้นเพียงพอหรือไม่
แม้จะมีการรักษาป้องกันวัณโรค แต่ก็มีกรณีของการเปิดใช้งานวัณโรคอีกครั้งในผู้ป่วยที่ได้รับการรักษาด้วย Humira ผู้ป่วยบางรายที่รักษาวัณโรคที่ออกฤทธิ์ได้สำเร็จประสบกับวัณโรคอีกครั้งระหว่างการรักษาด้วย Humira
ผู้ป่วยควรได้รับคำแนะนำให้ไปพบแพทย์หากสัญญาณ/อาการบ่งชี้ว่าอาจมีการติดเชื้อวัณโรค (เช่น ไอต่อเนื่อง, เสียเปล่า, น้ำหนักลด, มีไข้ปานกลาง, กระสับกระส่าย) เกิดขึ้นระหว่างหรือหลังการรักษาด้วย Humira
การติดเชื้อฉวยโอกาสอื่นๆ:
พบกรณีของการติดเชื้อฉวยโอกาสรวมถึงการติดเชื้อราที่แพร่กระจายในผู้ป่วยที่รับ Humira การติดเชื้อเหล่านี้ยังไม่ได้รับการวินิจฉัยอย่างถูกต้องในผู้ป่วยที่ใช้ TNF-antagonists และส่งผลให้การรักษาที่เหมาะสมล่าช้า บางครั้งอาจถึงแก่ชีวิตได้
ในผู้ป่วยที่มีอาการและอาการแสดง เช่น มีไข้ วิงเวียน น้ำหนักลด เหงื่อออก ไอ หายใจลำบาก และ/หรือปอดติดเชื้อ หรือโรคร้ายแรงทางระบบอื่นๆ ที่มีหรือไม่มีช็อกร่วมด้วย ควรสงสัยว่ามีการติดเชื้อราที่ลุกลาม และควรหยุดการรักษาโดยทันที . การบริหาร Humira การวินิจฉัยและการบริหารยาต้านเชื้อราเชิงประจักษ์ในผู้ป่วยเหล่านี้ควรทำโดยปรึกษาหารือกับแพทย์ที่เชี่ยวชาญในการรักษาผู้ป่วยที่มีการติดเชื้อราที่แพร่กระจาย
การเปิดใช้งานของไวรัสตับอักเสบบี
การเปิดใช้งานของไวรัสตับอักเสบบี (เช่น แอนติเจนพื้นผิวเป็นบวก) เกิดขึ้นอีกครั้งในพาหะของไวรัสตับอักเสบบีเรื้อรังที่รักษาด้วย TNF antagonists รวมทั้ง Humira บางกรณีมีผลร้ายแรง ก่อนเริ่มการรักษาด้วย Humira ผู้ป่วยควรได้รับการตรวจหาการติดเชื้อไวรัสตับอักเสบบี ควรปรึกษาแพทย์ที่มีประสบการณ์ในการรักษาโรคตับอักเสบบีสำหรับผู้ป่วยที่ตรวจพบไวรัสตับอักเสบบีเป็นบวก
ควรมีการตรวจสอบพาหะของไวรัสตับอักเสบบีที่ต้องรักษาด้วย Humira อย่างใกล้ชิดสำหรับสัญญาณและอาการของการติดเชื้อไวรัสตับอักเสบบีที่ออกฤทธิ์ไม่เฉพาะตลอดการรักษาแต่ยังรวมถึงในช่วงหลายเดือนหลังการระงับการรักษาด้วย การรักษาผู้ป่วยไม่มีข้อมูลเพียงพอ กับไวรัสตับอักเสบบีที่ได้รับการรักษาด้วยยาต้านไวรัสเพื่อหลีกเลี่ยงการเปิดใช้งานของไวรัสตับอักเสบบีควบคู่ไปกับการรักษา TNF-antagonist ในผู้ป่วยที่พัฒนาไวรัสตับอักเสบบี reactivation การให้ Humira ควรหยุดและให้การรักษาด้วยยาต้านไวรัสที่มีประสิทธิภาพพร้อมกับ การรักษาแบบประคับประคองอย่างเพียงพอ
เหตุการณ์ทางระบบประสาท
TNF-antagonists รวมทั้ง Humira มีความเกี่ยวข้องในกรณีที่ไม่ค่อยเกิดขึ้นกับอาการใหม่หรืออาการกำเริบของอาการทางคลินิกและ / หรือหลักฐานทางรังสีวิทยาของระบบประสาทส่วนกลางที่ทำลายล้างโรครวมทั้งเส้นโลหิตตีบประสาทแก้วนำแสงและโรคทำลายล้างส่วนปลายรวมถึงกลุ่มอาการ Guillain-Barrè ควรใช้ Humira ในผู้ป่วยที่มีอาการผิดปกติของการทำลายล้างส่วนกลางหรือบริเวณรอบข้างก่อนหน้านี้หรือเมื่อเร็ว ๆ นี้
อาการแพ้
ในการทดลองทางคลินิก ปฏิกิริยาการแพ้อย่างรุนแรงที่เกี่ยวข้องกับ Humira นั้นหาได้ยาก อาการแพ้ที่ไม่ร้ายแรงที่เกี่ยวข้องกับ Humira ระหว่างการทดลองทางคลินิกนั้นเป็นเรื่องแปลก มีรายงานการเกิดอาการแพ้อย่างรุนแรงรวมทั้งการเกิด anaphylaxis ภายหลังการให้ Humira ถ้าเกิดปฏิกิริยา anaphylactic หรืออาการแพ้อย่างรุนแรงอื่น ๆ ควรหยุดการให้ Humira ทันทีและเริ่มการรักษาที่เหมาะสม
ภูมิคุ้มกัน
ในการศึกษาผู้ป่วยโรคข้ออักเสบรูมาตอยด์ 64 รายที่ได้รับการรักษาด้วย Humira ไม่มีหลักฐานการยับยั้งการแพ้ที่ล่าช้าหรือการลดระดับอิมมูโนโกลบูลินหรือการเปลี่ยนแปลงของจำนวน T, B, NK, โมโนไซต์ / เซลล์ลิมโฟไซต์ .
เนื้องอกและโรคต่อมน้ำเหลือง
ในส่วนที่ควบคุมของการทดลองทางคลินิก TNF-antagonist พบว่ามีผู้ป่วยที่ได้รับ TNF-blocker มากกว่าในกลุ่มควบคุม อย่างไรก็ตามกรณีต่างๆ นั้นหายาก ในการศึกษาหลังการขาย มีรายงานกรณีของโรคมะเร็งเม็ดเลือดขาวในผู้ป่วยที่ได้รับการรักษาด้วย TNF-antagonist มีความเสี่ยงที่จะเป็นมะเร็งต่อมน้ำเหลืองและมะเร็งเม็ดเลือดขาวมากขึ้นสำหรับผู้ป่วยโรคข้ออักเสบรูมาตอยด์ที่มีฤทธิ์รุนแรงและยาวนาน ซึ่งเป็นโรคที่มีการอักเสบซึ่งทำให้การประเมินความเสี่ยงมีความซับซ้อนมากขึ้น ด้วยความรู้ในปัจจุบัน จึงไม่สามารถแยกแยะการพัฒนาของมะเร็งต่อมน้ำเหลืองออกได้ มะเร็งเม็ดเลือดขาวและมะเร็งชนิดอื่นๆ ในผู้ป่วย รักษาด้วยยาต้าน TNF
มีรายงานกรณีของโรคมะเร็งที่อาจถึงแก่ชีวิตในเด็ก วัยรุ่น และผู้ใหญ่วัยหนุ่มสาว (อายุไม่เกิน 22 ปี) ที่ได้รับการรักษาด้วย TNF antagonists (การเริ่มต้นของการรักษา ≤ 18 ปี) รวมทั้ง adalimumab ในการศึกษาหลังการขาย ประมาณครึ่งหนึ่งของผู้ป่วยเป็นมะเร็งต่อมน้ำเหลือง กรณีอื่น ๆ แสดงถึงความหลากหลายของมะเร็งที่แตกต่างกัน และรวมถึงมะเร็งที่หายากซึ่งมักเกี่ยวข้องกับการกดภูมิคุ้มกัน ไม่สามารถยกเว้นความเสี่ยงในการพัฒนาเนื้องอกในเด็กและวัยรุ่นที่ได้รับการรักษาด้วย TNF antagonists ได้
พบกรณีหลังการขายที่หายากของมะเร็งต่อมน้ำเหลือง T-cell hepatosplenic ในผู้ป่วยที่ได้รับการรักษาด้วย adalimumab มะเร็งต่อมน้ำเหลืองชนิด T-cell ที่หายากนี้มีหลักสูตรทางคลินิกที่ก้าวร้าวมากและมักเป็นอันตรายถึงชีวิต บางกรณีของมะเร็งต่อมน้ำเหลือง hepatosplenic T-cell เกิดขึ้นในผู้ป่วยวัยหนุ่มสาวที่ได้รับ Humira และได้รับการรักษาร่วมกับ azathioprine หรือ 6-mercaptopurine ซึ่งเป็นยาที่ใช้รักษาโรคลำไส้อักเสบ ควรพิจารณาความเสี่ยงที่อาจเกิดขึ้นจากการรวมกันของ azathioprine หรือ 6-mercaptopurine และ Humira ความเสี่ยงของการพัฒนามะเร็งต่อมน้ำเหลืองทีเซลล์ตับไม่สามารถยกเว้นได้ในผู้ป่วยที่รักษาด้วย Humira (ดูหัวข้อ 4.8)
ไม่มีการศึกษาทางคลินิกในผู้ป่วยที่มีประวัติโรคมะเร็งหรือในผู้ป่วยที่รักษาด้วย Humira อย่างต่อเนื่องหลังจากการพัฒนาของมะเร็ง ดังนั้น ควรพิจารณาการรักษาด้วย Humira ในผู้ป่วยรายนี้ด้วยความระมัดระวังเพิ่มเติม (ดูหัวข้อ 4.8)
ก่อนและระหว่างการรักษาด้วย Humira ผู้ป่วยทุกราย โดยเฉพาะอย่างยิ่งผู้ที่มีประวัติของการรักษาด้วยยากดภูมิคุ้มกันอย่างกว้างขวางหรือผู้ที่เป็นโรคสะเก็ดเงินที่มีประวัติในการรักษาด้วย PUVA ควรได้รับการตรวจดูว่ามีมะเร็งผิวหนังที่ไม่ใช่เมลาโนติกหรือไม่ มะเร็งเมลาโนมาและมะเร็งเซลล์ Merkel ยังได้รับการรายงานในผู้ป่วยที่ได้รับการรักษาด้วย TNF antagonists รวมทั้ง adalimumab (ดูหัวข้อ 4.8)
ในการศึกษาทางคลินิกเชิงสำรวจเพื่อประเมินการใช้ Infliximab ซึ่งเป็นปฏิปักษ์ TNF อื่นในผู้ป่วยโรคปอดอุดกั้นเรื้อรังระดับปานกลางถึงรุนแรง (COPD) มีรายงานผู้ป่วยที่รักษาด้วย infliximab มากกว่าผู้ป่วยกลุ่มควบคุม โดยเฉพาะอย่างยิ่งในปอดหรือศีรษะ และคอ ผู้ป่วยทุกรายมีประวัติการสูบบุหรี่มาก ดังนั้น ควรใช้ความระมัดระวังเมื่อใช้ TNF-antagonist ในผู้ป่วยโรคปอดอุดกั้นเรื้อรัง เช่นเดียวกับในผู้ป่วยที่มีความเสี่ยงต่อการเป็นมะเร็งเพิ่มขึ้นเนื่องจากการสูบบุหรี่มากเกินไป
จากข้อมูลปัจจุบัน ไม่ทราบว่าการรักษา adalimumab ส่งผลต่อความเสี่ยงของการเกิด dysplasia หรือมะเร็งลำไส้ใหญ่หรือไม่ ผู้ป่วยทุกรายที่มีอาการลำไส้ใหญ่บวมเป็นแผลที่มีความเสี่ยงเพิ่มขึ้นต่อการเกิด dysplasia ของลำไส้ใหญ่หรือมะเร็ง (เช่น ผู้ป่วยที่มีอาการลำไส้ใหญ่บวมเป็นแผลเป็นเป็นเวลานานหรือ primary sclerosing cholangitis) หรือผู้ที่มีประวัติ dysplasia หรือมะเร็งลำไส้ใหญ่มาก่อนควรได้รับการตรวจคัดกรองอย่างสม่ำเสมอ dysplasia ตลอดระยะเวลาของโรค การประเมินนี้ควรรวมถึงการส่องกล้องตรวจลำไส้ใหญ่และตรวจชิ้นเนื้อตามคำแนะนำในท้องถิ่น
ปฏิกิริยาที่ส่งผลต่อระบบเม็ดเลือด
มีรายงานกรณีของ pancytopenia ที่หายากรวมถึงการเกิด aplastic anemia หลังจากใช้ยา anti-TNF มีรายงานผู้ป่วยที่รักษาด้วย Humira จากมุมมองทางการแพทย์ (เช่น thrombocytopenia, leukopenia) ในระหว่างการรักษาด้วย Humira ผู้ป่วยทุกรายควรได้รับคำแนะนำว่าจำเป็นต้องปรึกษาแพทย์ทันทีเพื่อรับความช่วยเหลือที่เพียงพอในกรณีที่มีอาการและอาการแสดงที่บ่งชี้ว่ามีภาวะ dyscrasia ในเลือด (เช่น มีไข้เรื้อรัง ช้ำ, ตกเลือด, ซีด) ในกรณีของผู้ป่วยที่มีการยืนยันการเปลี่ยนแปลงที่สำคัญในระบบเม็ดเลือดควรพิจารณาความจำเป็นในการยุติการรักษาด้วย Humira
การฉีดวัคซีน
การตอบสนองของแอนติบอดีที่คล้ายคลึงกันกับวัคซีนป้องกันโรคปอดบวม 23 วาเลนต์มาตรฐานและวัคซีนไวรัสไข้หวัดใหญ่ชนิดไตรวาเลนต์ถูกสังเกตพบในการศึกษาที่เกี่ยวข้องกับผู้ใหญ่ 226 คนที่เป็นโรคข้ออักเสบรูมาตอยด์ที่ได้รับ adalimumab หรือยาหลอก ไม่มีข้อมูล เกี่ยวกับการแพร่เชื้อทุติยภูมิจากวัคซีนที่มีชีวิตใน ผู้ป่วยที่รับ Humira
ในผู้ป่วยเด็ก ขอแนะนำให้ใช้ตารางการฉีดวัคซีนตามแผน หากเป็นไปได้ ตามแนวทางการฉีดวัคซีนปัจจุบันก่อนเริ่มการรักษาด้วย Humira
ผู้ป่วยที่ได้รับ Humira อาจได้รับการฉีดวัคซีนพร้อมกัน ยกเว้นวัคซีนที่มีชีวิต ไม่แนะนำให้ฉีดวัคซีนที่มีชีวิตให้กับทารกที่ได้รับ adalimumab ในครรภ์เป็นเวลา 5 เดือนหลังการให้ยา adalimumab ครั้งสุดท้ายของมารดาในระหว่างตั้งครรภ์
หัวใจล้มเหลว
พบการแย่ลงของภาวะหัวใจล้มเหลวและการเสียชีวิตที่เกี่ยวข้องในการทดลองทางคลินิกกับยาต้าน TNF ตัวอื่น นอกจากนี้ยังพบอาการหัวใจล้มเหลวที่แย่ลงในผู้ป่วยที่ได้รับการรักษาด้วย Humira Humira ควรใช้ด้วยความระมัดระวังในผู้ป่วยที่มีภาวะหัวใจล้มเหลวเล็กน้อย (NYHA class I / II) ห้ามใช้ Humira ในภาวะหัวใจล้มเหลวในระดับปานกลางหรือรุนแรง (ดูหัวข้อ 4.3) ควรยุติการรักษาด้วย Humira ในผู้ป่วยที่มีอาการแย่ลงหรือมีอาการใหม่ของภาวะหัวใจล้มเหลว
กระบวนการแพ้ภูมิตัวเอง
การรักษาด้วย Humira สามารถกระตุ้นการสร้างแอนติบอดีต่อภูมิต้านทานผิดปกติ ไม่ทราบผลกระทบของการรักษาระยะยาวด้วย Humira ต่อการพัฒนาของโรคภูมิต้านตนเอง หากผู้ป่วยมีอาการที่บ่งบอกถึงกลุ่มอาการคล้ายลูปัสหลังการรักษาด้วย Humira และเป็นผลบวกต่อแอนติบอดีต่อ DNA แบบเกลียวคู่ อย่าทำการรักษาเพิ่มเติมด้วย Humira ควรให้ (ดูหัวข้อ 4.8)
การบริหารร่วมกันของ DMARDS ทางชีวภาพหรือคู่อริ TNF
การติดเชื้อร้ายแรงที่ไม่มีประโยชน์ทางคลินิกเมื่อเปรียบเทียบกับ etanercept เพียงอย่างเดียวนั้นพบได้ในการทดลองทางคลินิกของการรักษาร่วมกับยา anakinra และยา etanercept ที่ต่อต้าน TNF อีกตัวหนึ่ง เมื่อพิจารณาจากประเภทของเหตุการณ์ไม่พึงประสงค์ที่สังเกตได้จากการใช้อนาคินราร่วมกับอีทาเนอร์เซพต์ร่วมกัน ผลข้างเคียงที่คล้ายคลึงกันอาจเกิดขึ้นหลังจากใช้อนาคินราร่วมกับยาต้าน TNF ตัวอื่น ดังนั้นจึงไม่แนะนำให้ใช้ adalimumab ร่วมกับ anakinra (ดูหัวข้อ 4.5)
ไม่แนะนำให้ใช้ adalimumab ร่วมกับ DMARDS ทางชีวภาพอื่น ๆ (เช่น anakinra และ abatacept) หรือคู่อริ TNF อื่น ๆ โดยพิจารณาจากความเสี่ยงที่เพิ่มขึ้นของการติดเชื้อ รวมถึงการติดเชื้อร้ายแรงและปฏิกิริยาระหว่างยาที่อาจเกิดขึ้น (ดูหัวข้อ 4.5)
การแทรกแซงการผ่าตัด
มีประสบการณ์ "จำกัด" เกี่ยวกับความปลอดภัยของขั้นตอนการผ่าตัดในผู้ป่วยที่ได้รับการรักษาด้วย Humira ควรพิจารณาครึ่งชีวิตที่ยาวนานของ adalimumab เมื่อวางแผนการผ่าตัด ผู้ป่วยที่ได้รับการผ่าตัดในขณะที่รับการรักษาด้วย Humira ควรได้รับการปฏิบัติตามอย่างใกล้ชิดสำหรับการพัฒนาของการติดเชื้อซึ่งในกรณีนี้ควรดำเนินการ มีประสบการณ์ "จำกัด" เกี่ยวกับความปลอดภัยในผู้ป่วยที่ได้รับการผ่าตัดเปลี่ยนข้อในขณะที่รับการรักษาด้วย Humira
ลำไส้อุดตัน
การไม่ตอบสนองต่อการรักษาโรคโครห์นอาจบ่งชี้ว่ามีไฟโบรติกตีบตันที่อาจต้องผ่าตัด ข้อมูลที่มีอยู่แสดงให้เห็นว่า Humira ไม่ได้ทำให้แย่ลงหรือทำให้เกิดภาวะตึงเครียด
ผู้สูงอายุ
ความถี่ของการติดเชื้อรุนแรงในผู้ป่วยที่รักษาด้วย Humira ที่มีอายุมากกว่า 65 ปี (3.5%) นั้นสูงกว่าผู้ที่มีอายุต่ำกว่า 65 ปี (1.5%)สิ่งเหล่านี้บางส่วนมีผลร้ายแรง ควรให้ความสนใจเป็นพิเศษเกี่ยวกับความเสี่ยงของการติดเชื้อในการรักษาผู้ป่วยสูงอายุ
ประชากรเด็ก
ดูการฉีดวัคซีนด้านบน
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
การบำบัดด้วย Humira ได้รับการศึกษาเป็นยาเดี่ยวและใช้ร่วมกับ methotrexate ในผู้ป่วยโรคข้ออักเสบรูมาตอยด์ โรคข้ออักเสบไม่ทราบสาเหตุในเด็กและเยาวชนที่มีหลายข้อ และโรคข้ออักเสบจากสะเก็ดเงิน การสร้างแอนติบอดีลดลงเมื่อให้ Humira ร่วมกับ methotrexate มากกว่าการให้ยาเดี่ยว การบริหารให้ Humira โดยไม่มี methotrexate ส่งผลให้เกิดการสร้างแอนติบอดีเพิ่มขึ้น การชำระล้างเพิ่มขึ้น และประสิทธิภาพของ adalimumab ลดลง (ดูหัวข้อ 5.1)
ไม่แนะนำให้ใช้ Humira และ anakinra ร่วมกัน (ดูหัวข้อ 4.4 "การบริหารร่วมกันของ DMARDs ทางชีววิทยาหรือคู่อริ TNF")
ไม่แนะนำให้ใช้ Humira และ abatacept ร่วมกัน (ดูหัวข้อ 4.4 "การบริหารร่วมกันของ DMARDs ทางชีววิทยาหรือคู่อริ TNF")
04.6 การตั้งครรภ์และให้นมบุตร
การตั้งครรภ์
สำหรับ Humira มีข้อมูลทางคลินิกที่จำกัดเกี่ยวกับการตั้งครรภ์ที่เปิดเผย
ในการศึกษาความเป็นพิษต่อพัฒนาการที่ดำเนินการในลิง ไม่พบความเป็นพิษของมารดา ความเป็นพิษต่อตัวอ่อน หรือการก่อมะเร็งในครรภ์ ไม่มีข้อมูลพรีคลินิกเกี่ยวกับความเป็นพิษหลังคลอดของ adalimumab (ดูหัวข้อ 5.3)
เนื่องจากการยับยั้ง TNFα การให้ adalimumab ระหว่างตั้งครรภ์อาจรบกวนการตอบสนองภูมิคุ้มกันตามปกติของทารกแรกเกิด จึงไม่แนะนำให้ใช้ Adalimumab ในการตั้งครรภ์
Adalimumab สามารถข้ามรกและไปถึงซีรั่มของทารกที่เกิดจากมารดาที่รับการรักษาด้วย adalimumab ในระหว่างตั้งครรภ์ ดังนั้น เด็กเหล่านี้จึงมีความเสี่ยงที่จะติดเชื้อมากขึ้น ไม่แนะนำให้ฉีดวัคซีนที่มีชีวิตให้กับทารกที่ได้รับ adalimumab ในครรภ์เป็นเวลา 5 เดือนหลังการให้ยา adalimumab ครั้งสุดท้ายของมารดาในระหว่างตั้งครรภ์
เวลาให้อาหาร
ไม่ทราบว่า adalimumab ถูกขับออกมาในนมของมนุษย์หรือถูกดูดซึมอย่างเป็นระบบหลังจากการกลืนกิน
อย่างไรก็ตาม เนื่องจากอิมมูโนโกลบูลินของมนุษย์ถูกขับออกมาในนม ผู้หญิงจึงไม่ควรให้นมลูกเป็นเวลาอย่างน้อยห้าเดือนหลังการรักษาด้วย Humira ครั้งสุดท้าย
ภาวะเจริญพันธุ์
ไม่มีข้อมูลพรีคลินิกเกี่ยวกับผลกระทบของ adalimumab ต่อภาวะเจริญพันธุ์
ผู้หญิงในวัยเจริญพันธุ์ การคุมกำเนิดในผู้ชายและผู้หญิง
ผู้หญิงที่มีศักยภาพในการคลอดบุตรควรใช้การคุมกำเนิดอย่างเพียงพอเพื่อป้องกันการตั้งครรภ์และใช้ต่อไปเป็นเวลาอย่างน้อยห้าเดือนหลังจากการรักษาด้วย Humira ครั้งสุดท้าย
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
Humira มีผลเล็กน้อยต่อความสามารถในการขับหรือใช้เครื่องจักร อาการวิงเวียนศีรษะและการรบกวนทางสายตาอาจเกิดขึ้นหลังการให้ Humira (ดูหัวข้อ 4.8)
04.8 ผลกระทบที่ไม่พึงประสงค์
Humira ได้รับการศึกษาในผู้ป่วย 8,198 รายในการทดลองทางคลินิกแบบควบคุมและเปิดฉลากที่สำคัญนานถึง 60 เดือนหรือนานกว่านั้น การศึกษาเหล่านี้ดำเนินการในผู้ป่วยที่เริ่มมีอาการตั้งแต่เนิ่นๆ และโรคข้ออักเสบรูมาตอยด์เป็นเวลานาน โรคข้ออักเสบไม่ทราบสาเหตุในเด็กและเยาวชน (โรคข้ออักเสบไม่ทราบสาเหตุ polyarticular และโรคข้ออักเสบที่เกี่ยวข้องกับ enthesitis) รวมทั้งในผู้ป่วยที่เป็นโรคข้อเข่าเสื่อมในแนวแกน (ankylosing spondylitis และ axial spondylo) ), โรคข้ออักเสบสะเก็ดเงิน, โรคโครห์น, โรคลำไส้ใหญ่บวมเป็นแผลและโรคสะเก็ดเงิน การศึกษาแบบควบคุมการพิจาณาได้ดำเนินการในผู้ป่วย 5,343 รายที่ได้รับ Humira และ 3,148 รายที่ได้รับยาหลอกหรือเครื่องเปรียบเทียบที่ใช้งานอยู่ในช่วงระยะเวลาควบคุม
เปอร์เซ็นต์ของผู้ป่วยที่หยุดการรักษาเนื่องจากเหตุการณ์ไม่พึงประสงค์ระหว่างการศึกษาแบบ double-blind แบบควบคุมระยะที่ 6.1% สำหรับผู้ป่วยที่ใช้ Humira และ 5.7% สำหรับผู้ป่วยที่ได้รับการรักษา ด้วยการควบคุม
สรุปข้อมูลความปลอดภัย
อาการไม่พึงประสงค์ที่รายงานบ่อยที่สุดคือการติดเชื้อ (เช่น หลอดอาหารอักเสบ การติดเชื้อทางเดินหายใจส่วนบน และไซนัสอักเสบ) ปฏิกิริยาในบริเวณที่ฉีด (ผื่นแดง อาการคัน เลือดออก ปวดหรือบวม) ปวดศีรษะและปวดกล้ามเนื้อและกระดูก
มีรายงานอาการไม่พึงประสงค์ที่ร้ายแรงสำหรับ Humira ยาที่ปิดกั้น TNF เช่น Humira ส่งผลต่อระบบภูมิคุ้มกัน และการใช้ยาดังกล่าวอาจส่งผลต่อการป้องกันของร่างกายต่อการติดเชื้อและมะเร็ง
กรณีของการติดเชื้อร้ายแรง (รวมถึงกรณีของภาวะติดเชื้อ, การติดเชื้อฉวยโอกาสและวัณโรค), การเปิดใช้งานของการติดเชื้อ HBV อีกครั้งและมะเร็งชนิดต่างๆ เซลล์).
มีรายงานการเกิดปฏิกิริยาทางโลหิตวิทยา ระบบประสาท และภูมิต้านทานผิดปกติอย่างรุนแรง หลังรวมถึงกรณีที่หายากของ pancytopenia, aplastic anemia, เหตุการณ์ demyelination ส่วนกลางและส่วนปลายและกรณีของ lupus, เงื่อนไขที่เกี่ยวข้องกับ lupus และ Stevens-Johnson syndrome
ประชากรเด็ก
ผลกระทบที่ไม่พึงประสงค์ในผู้ป่วยเด็ก
โดยทั่วไป อาการไม่พึงประสงค์ในผู้ป่วยเด็กมีความคล้ายคลึงกับที่พบในผู้ป่วยผู้ใหญ่ทั้งในด้านความถี่และประเภท
ตารางรายการอาการไม่พึงประสงค์
รายการอาการข้างเคียงต่อไปนี้ขึ้นอยู่กับประสบการณ์จากการทดลองทางคลินิกและประสบการณ์หลังการทำการตลาด และจำแนกตามระบบ/อวัยวะที่เกี่ยวข้องและความถี่ (พบบ่อยมาก ≥1 / 10; พบบ่อย≥1 / 100 ถึง
ตารางที่ 2
ผลข้างเคียง
* มีข้อมูลเพิ่มเติมอยู่ในส่วน 4.3, 4.4 และ 4.8
** รวมถึงการศึกษาส่วนขยายฉลากแบบเปิด
1) รวมข้อมูลจากรายงานที่เกิดขึ้นเอง
คำอธิบายของอาการไม่พึงประสงค์ที่เลือก
ปฏิกิริยาที่บริเวณที่ฉีด
ในการทดลองทางคลินิกที่มีการควบคุมการพิจาณาในผู้ใหญ่และเด็ก 13.6% ของผู้ป่วยที่ได้รับ Humira พบปฏิกิริยาในบริเวณที่ฉีด (ผื่นแดงและ / หรืออาการคัน ตกเลือด ปวดหรือบวมน้ำ) เทียบกับ 7.6% ของผู้ป่วยที่ได้รับยาหลอกหรือกลุ่มควบคุมที่ออกฤทธิ์ โดยทั่วไปไม่จำเป็นต้องหยุดยา
การติดเชื้อ
ในการทดลองทางคลินิกที่มีการควบคุมการพิจาณาในผู้ใหญ่และเด็ก อัตราการติดเชื้อเท่ากับ 1.52 ต่อผู้ป่วย / ปีในกลุ่ม Humira และ 1.45 ต่อผู้ป่วย / ปีในกลุ่มยาหลอกและกลุ่มควบคุมที่ออกฤทธิ์ การติดเชื้อส่วนใหญ่แสดงโดยช่องจมูกอักเสบ การติดเชื้อทางเดินหายใจส่วนบน และ การติดเชื้อทางเดินปัสสาวะ ผู้ป่วยส่วนใหญ่ยังคงใช้ Humira ต่อไปหลังจากการติดเชื้อหายไป
อุบัติการณ์ของการติดเชื้อรุนแรงคือ 0.04 ต่อผู้ป่วย / ปีในกลุ่ม Humira และ 0.03 ต่อผู้ป่วย / ปีในกลุ่มยาหลอกและกลุ่มควบคุมที่ใช้งานอยู่
ในการศึกษาแบบควบคุมและแบบ open-label กับ Humira ในผู้ใหญ่และเด็ก มีรายงานการติดเชื้อร้ายแรง (รวมถึงการติดเชื้อร้ายแรงซึ่งเกิดขึ้นไม่บ่อยนัก) รวมถึงรายงานผู้ป่วยวัณโรค (รวมถึงตำแหน่งทหารและนอกปอด) และการติดเชื้อฉวยโอกาสรุกราน ( ตัวอย่างเช่น ฮิสโตพลาสโมซิสที่แพร่กระจายหรือนอกปอด, บลาสโตมัยโคซิส, ค็อกซิดิออยโดไมโคซิส, โรคปอดบวม, เชื้อราในเชื้อรา, เชื้อราแอสเปอร์จิลโลสิส, และลิสเทอริโอซิส) กรณีส่วนใหญ่ของวัณโรคเกิดขึ้นภายในแปดเดือนแรกหลังจากเริ่มการรักษา และสามารถตีความได้ว่าเป็นการกลับเป็นซ้ำของโรคที่แฝงอยู่
เนื้องอกและโรคต่อมน้ำเหลือง
ในการศึกษาที่ดำเนินการโดยการให้ Humira แก่ผู้ป่วยโรคข้ออักเสบไม่ทราบสาเหตุเด็กและเยาวชน (โรคข้ออักเสบที่ไม่ทราบสาเหตุในเด็กและเยาวชนที่ไม่ทราบสาเหตุหลายข้อและโรคข้ออักเสบที่เกี่ยวข้องกับการอักเสบ) ไม่พบมะเร็งในผู้ป่วยเด็ก 249 รายที่ได้รับ 655.6 คนต่อปี นอกจากนี้ยังไม่พบมะเร็งในเด็ก 192 คน ผู้ป่วยที่มีความเสี่ยง 258.9 ปีผู้ป่วยในระหว่างการศึกษาให้ Humira แก่ผู้ป่วยเด็กที่เป็นโรค Crohn
ในส่วนที่ควบคุมของการศึกษาการพิจาณาในผู้ใหญ่ที่มี Humira เป็นเวลานานอย่างน้อย 12 สัปดาห์ในผู้ป่วยที่มีโรคข้ออักเสบรูมาตอยด์ระดับปานกลางถึงรุนแรง, โรคกระดูกสันหลังยึดติด, โรคกระดูกพรุนในแนวแกนโดยไม่มีหลักฐานทางรังสีวิทยาของ ankylosing spondylitis, โรคข้ออักเสบสะเก็ดเงิน, โรคสะเก็ดเงิน, โรคโครห์นและโรคลำไส้ใหญ่บวมเป็นแผล, โรคลำไส้ใหญ่บวมเป็นแผล มะเร็งต่อมน้ำเหลืองและมะเร็งผิวหนังที่ไม่ใช่เมลาโนติกพบในอัตรา (ช่วงความเชื่อมั่น 95%) ที่ 6.0 (3.7, 9.8) ต่อผู้ป่วย 1,000 รายต่อปีในผู้ป่วย 4,622 รายที่ได้รับการรักษาด้วย Humira ถึง อัตรา 5.1 (2.4, 10.7) ต่อ 1,000 ผู้ป่วยปีของผู้ป่วยควบคุม 2,828 ราย (ระยะเวลามัธยฐานของการรักษาคือ 5.1 เดือนสำหรับผู้ป่วยที่ได้รับ Humira และ 4.0 เดือนสำหรับผู้ป่วยที่ตรวจ) อัตรา (ช่วงความเชื่อมั่น 95%) ของมะเร็งผิวหนังที่ไม่ใช่เมลาโนติกเท่ากับ 9.7 (6.6; 14.3) ต่อ 1,000 ปีผู้ป่วยในผู้ป่วยที่ได้รับการรักษาด้วย Humira และ 5.1 (2.4; 10, 7) ต่อ 1,000 ปีผู้ป่วยในผู้ป่วยกลุ่มควบคุม ของมะเร็งผิวหนังเหล่านี้ มะเร็งเซลล์สความัสเกิดขึ้นในอัตรา (ช่วงความเชื่อมั่น 95%) ที่ 2.6 (1.2; 5.5) ต่อผู้ป่วยที่ได้รับการรักษาด้วย Humira จำนวน 1,000 รายต่อปี และ 0.7 (0.1; 5.2) ต่อผู้ป่วย 1,000 รายต่อปีในผู้ป่วยกลุ่มควบคุม อัตรา (ช่วงความเชื่อมั่น 95%) ของมะเร็งต่อมน้ำเหลืองเท่ากับ 0.7 (0.2, 3.0) ต่อผู้ป่วย 1,000 รายต่อปีในผู้ป่วยที่ได้รับ Humira และ 1.5 (0.4, 5.8) ต่อผู้ป่วย 1, 000 รายในผู้ป่วยที่ได้รับการควบคุม
เมื่อส่วนต่างๆ ของการศึกษาเหล่านี้และการศึกษาการขยายฉลากแบบเปิดทั้งที่ดำเนินการอยู่และที่เสร็จสิ้นแล้วรวมกัน โดยมีระยะเวลาเฉลี่ยประมาณ 3.4 ปี รวมผู้ป่วย 5,727 รายและผู้ป่วยในการรักษามากกว่า 24,568 ปี อัตราเนื้องอกที่สังเกตได้ ยกเว้นมะเร็งต่อมน้ำเหลืองและมะเร็งที่ไม่ใช่เมลาโนติก มะเร็งผิวหนังอยู่ที่ประมาณ 8.8 ต่อผู้ป่วย 1,000 ปี อัตราที่สังเกตได้ของมะเร็งผิวหนังที่ไม่ใช่เมลาโนติกอยู่ที่ประมาณ 10.3 ต่อผู้ป่วย 1,000 ปีและอัตราการสังเกตของมะเร็งต่อมน้ำเหลืองอยู่ที่ประมาณ 1.4 ต่อ 1,000 คนต่อปี
จากประสบการณ์หลังการขายในช่วงมกราคม 2546 ถึงธันวาคม 2553 ส่วนใหญ่ในผู้ป่วยโรคข้ออักเสบรูมาตอยด์ อัตราการรายงานของมะเร็งอยู่ที่ประมาณ 2.7 ต่อการรักษา 1,000 / ปีผู้ป่วย อัตราที่รายงานสำหรับมะเร็งผิวหนังและมะเร็งต่อมน้ำเหลืองชนิด non-melanotic อยู่ที่ประมาณ 0.2 และ 0.3 ต่อการรักษา 1,000 ครั้ง / ปีของผู้ป่วยตามลำดับ (ดูหัวข้อ 4.4)
มีรายงานกรณีที่พบไม่บ่อยของมะเร็งต่อมน้ำเหลืองทีเซลล์ตับ (hepatosplenic T-cell lymphoma) ในประสบการณ์หลังการขายในผู้ป่วยที่ได้รับการรักษาด้วย adalimumab (ดูหัวข้อ 4.4)
แอนติบอดี้
ในการศึกษาโรคข้ออักเสบรูมาตอยด์ IV ตัวอย่างซีรัมของผู้ป่วยได้รับการทดสอบในโอกาสต่าง ๆ สำหรับ autoantibodies ในการศึกษาเหล่านี้ 11.9% ของผู้ป่วยที่ได้รับ Humira และ 8.1% ของผู้ป่วยที่ได้รับยาหลอกและผู้ป่วยที่ควบคุมโดย active ซึ่งมีค่าแอนติบอดีต่อแอนติบอดีเป็นลบเมื่อลงทะเบียน ค่าบวกในสัปดาห์ที่ 24 ผู้ป่วย 2 ใน 3,441 รายที่ได้รับ Humira ในโรคข้ออักเสบรูมาตอยด์ทั้งหมดและโรคข้ออักเสบสะเก็ดเงินแสดงอาการทางคลินิกที่บ่งชี้ว่าเริ่มมีอาการคล้ายลูปัส ผู้ป่วยดีขึ้นหลังจากหยุดการรักษา ไม่มีผู้ป่วยโรคไตอักเสบลูปัสหรือระบบประสาทส่วนกลาง อาการของระบบ
เหตุการณ์ตับและท่อน้ำดี
ในการทดลองทางคลินิกระยะที่ 3 ของ Humira ในผู้ป่วยที่เป็นโรคข้ออักเสบรูมาตอยด์และโรคข้ออักเสบสะเก็ดเงินที่มีระยะเวลาควบคุมตั้งแต่ 4 ถึง 104 สัปดาห์ ALT transaminase สูงกว่าหรือเท่ากับ 3 เท่าของค่าปกติสูงสุดที่เกิดขึ้นใน 3.7% ของ Humira- ผู้ป่วยที่ได้รับการรักษาและ 1.6% ของผู้ป่วยที่ได้รับการควบคุม
ในการทดลองทางคลินิกระยะที่ 3 ที่ควบคุมของ Humira ในผู้ป่วยโรคสะเก็ดเงินจากคราบจุลินทรีย์ที่มีระยะเวลาควบคุม 12 ถึง 24 สัปดาห์ ALT transaminase มีค่าสูงกว่าหรือเท่ากับ 3 เท่าของค่าปกติสูงสุดที่เกิดขึ้นใน " 1.8% ของผู้ป่วยที่ได้รับ Humira และ 1.8 % ของผู้ป่วยที่ได้รับการควบคุม
ในการทดลองทางคลินิกระยะที่ 3 ที่ควบคุมของ Humira ในผู้ป่วยโรคข้ออักเสบไม่ทราบสาเหตุ polyarticular ที่มีอายุระหว่าง 4 ถึง 17 ปีและในผู้ป่วยที่เป็นโรคข้ออักเสบที่เกี่ยวข้องกับโรคไขข้ออักเสบอายุ 6 ถึง 17 ปี ALT สูงกว่าหรือเท่ากับ ULN 3 เท่า เกิดขึ้นในผู้ป่วยที่ได้รับ Humira 6.1% และผู้ป่วยที่ได้รับการควบคุม 1.3% ระดับความสูงของ ALT transaminase ส่วนใหญ่เกิดขึ้นกับการใช้ methotrexate ร่วมกัน ไม่มีระดับเอนไซม์ ALT transaminase ≥ 3 x ULN ในการทดลองทางคลินิกระยะที่ 3 ของ Humira ในผู้ป่วยที่เป็นโรคข้ออักเสบที่ไม่ทราบสาเหตุหลายข้อในเด็กและเยาวชน 2 และ
ในการทดลองทางคลินิกระยะที่ 3 ของ Humira ในผู้ป่วยที่เป็นโรค Crohn และอาการลำไส้ใหญ่บวมเป็นแผลที่มีระยะเวลาควบคุมตั้งแต่ 4 ถึง 52 สัปดาห์ ALT จะสูงกว่าหรือเท่ากับ 3 เท่าของค่าปกติสูงสุดที่เกิดขึ้นในผู้ป่วยที่ได้รับ Humira 0.9% และ 0.9% ของผู้ป่วยที่ได้รับการควบคุม
ในการศึกษา Humira ระยะที่ 3 ในผู้ป่วยเด็กที่เป็นโรค Chron ซึ่งประเมินความปลอดภัยและประสิทธิภาพของสูตรยาที่ปรับน้ำหนักสองสูตรสำหรับการบำบัดด้วยการบำรุงรักษาหลังการบำบัดด้วยการเหนี่ยวนำที่ปรับน้ำหนักได้นานถึง 52 สัปดาห์ ระดับ ALT ≥ 3 x ULN ถูกพบใน 2.6% ของผู้ป่วยทั้งหมดที่ได้รับการรักษาด้วยยากดภูมิคุ้มกันแบบพื้นฐาน
ในการทดลองทางคลินิก ในทุกข้อบ่งชี้ ผู้ป่วยที่มีระดับ transaminase สูงนั้นไม่มีอาการ และระดับความสูงนั้นเกิดขึ้นชั่วคราวและแก้ไขได้ในระหว่างการรักษาในกรณีส่วนใหญ่ อย่างไรก็ตาม กรณีหลังการขายของภาวะตับวายและความผิดปกติของตับที่รุนแรงน้อยกว่าที่อาจเกิดก่อนความล้มเหลวของตับ เช่น โรคตับอักเสบรวมถึงโรคตับอักเสบจากภูมิต้านตนเอง ก็มีรายงานในผู้ป่วยที่ได้รับการรักษาด้วย adalimumab
การรักษาร่วมกับ azathioprine / 6-mercaptopurine
ในการศึกษาโรคของโครห์นในผู้ใหญ่ พบว่ามีอุบัติการณ์ของเหตุการณ์ไม่พึงประสงค์ที่เกี่ยวข้องกับการติดเชื้อร้ายแรงและมะเร็งเพิ่มขึ้นด้วยการใช้ Humira และ azathioprine / 6-mercaptopurine ร่วมกับ Humira เพียงอย่างเดียว
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยซึ่งเกิดขึ้นหลังจากการอนุมัติผลิตภัณฑ์ยามีความสำคัญเนื่องจากช่วยให้สามารถตรวจสอบอัตราส่วนประโยชน์ / ความเสี่ยงของผลิตภัณฑ์ยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านการดูแลสุขภาพรายงานอาการไม่พึงประสงค์ที่น่าสงสัยผ่านทางสำนักงานยาแห่งอิตาลี , เว็บไซต์: http://www.agenziafarmaco.gov.it/it/responsabili
04.9 ใช้ยาเกินขนาด
ไม่พบความเป็นพิษที่เกี่ยวข้องกับขนาดยาในระหว่างการศึกษาทางคลินิก ปริมาณสูงสุดที่ประเมินคือ 10 มก. / กก. ฉีดเข้าเส้นเลือดดำหลายขนาด ปริมาณนี้เทียบเท่ากับปริมาณที่แนะนำประมาณ 15 เท่า
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
กลุ่มเภสัชบำบัด: ยากดภูมิคุ้มกันแบบเลือก รหัส ATC: L04AB04
กลไกการออกฤทธิ์
Adalimumab เลือกจับกับ TNF และทำให้การทำงานทางชีวภาพเป็นกลางโดยการปิดกั้นปฏิสัมพันธ์กับตัวรับ TNF ของเยื่อหุ้มเซลล์ p55 และ p75
นอกจากนี้ Adalimumab ยังปรับการตอบสนองทางชีวภาพที่ถูกเหนี่ยวนำหรือควบคุมโดย TNF ซึ่งรวมถึงการเปลี่ยนแปลงในระดับของโมเลกุลการยึดเกาะที่รับผิดชอบสำหรับการย้ายถิ่นของเม็ดเลือดขาว (ELAM-1, VCAM-1 และ ICAM-1 ด้วย IC50 ที่ 0.1-0, 2 nM)
ผลทางเภสัชพลศาสตร์
หลังการรักษาด้วย Humira พบว่ามีการลดลงอย่างรวดเร็วของโปรตีนระยะเฉียบพลัน ดัชนีการอักเสบ (C-reactive protein -PCR, erythrocyte sedimentation rate -VES) และ serum cytokines (IL-6) ในผู้ป่วยที่เป็นโรคข้ออักเสบรูมาตอยด์เมื่อเทียบกับฐาน ระดับซีรั่มของเมทริกซ์เมทัลโลโปรตีน (MMP-1 และ MMP-3) ที่เกี่ยวข้องกับการเปลี่ยนแปลงเนื้อเยื่อที่รับผิดชอบในการทำลายกระดูกอ่อนก็ลดลงเช่นกันหลังการให้ Humira ผู้ป่วยที่ได้รับ Humira มักมีอาการทางเคมีในเลือดของการอักเสบเรื้อรังดีขึ้น
ระดับ CRP (โปรตีนปฏิกิริยา C) ลดลงอย่างรวดเร็วยังพบในผู้ป่วยโรคข้ออักเสบที่ไม่ทราบสาเหตุในเด็กและเยาวชน Polyarticular, โรค Crohn และอาการลำไส้ใหญ่บวมเป็นแผลหลังการรักษาด้วย Humira การลดจำนวนเซลล์ที่แสดงเครื่องหมายการอักเสบในลำไส้ใหญ่รวมถึงการลดลงอย่างมากในTNFα การแสดงออก การศึกษาส่องกล้องของเยื่อบุลำไส้ได้แสดงให้เห็นการรักษาของเยื่อเมือกในผู้ป่วยที่ได้รับการรักษาด้วย adalimumab
ประสิทธิภาพและความปลอดภัยทางคลินิก
โรคข้ออักเสบไม่ทราบสาเหตุเด็กและเยาวชน (JIA)
โรคข้ออักเสบไม่ทราบสาเหตุเด็กและเยาวชน Polyarticular (pJIA)
ความปลอดภัยและประสิทธิภาพของ Humira ได้รับการประเมินในการศึกษาสองครั้ง (pJIA I และ II) ในเด็กที่เป็นโรคข้ออักเสบไม่ทราบสาเหตุในเด็กและเยาวชนที่มี polyarticular หรือ polyarticular ซึ่งมีอาการ JIA ประเภทต่างๆ (บ่อยที่สุดคือโรคข้ออักเสบรูมาตอยด์ที่เป็นลบหรือบวก polyarthritis และ oligoarthritis ที่กว้างขวาง)
pJIA-I
ความปลอดภัยและประสิทธิภาพของ Humira ได้รับการประเมินในการศึกษาแบบ multicentre, randomized double-blind, parallel-group ในเด็ก 171 คน (อายุ 4-17 ปี) ที่เป็นโรคข้ออักเสบไม่ทราบสาเหตุ polyarticular juvenile idiopathic arthritis (JIA) = OL LI ผู้ป่วยถูกแบ่งออกเป็นสองกลุ่ม คือ กลุ่ม MTX (methotrexate) และกลุ่มที่ไม่ได้รับการรักษา MTX แขนที่ไม่ได้รับการรักษาด้วย MTX ไม่เคยได้รับการรักษาด้วย MTX มาก่อนหรือหยุดใช้ MTX อย่างน้อยสองสัปดาห์ก่อนการให้ยาในการศึกษา ผู้ป่วยได้รับยาต้านการอักเสบที่ไม่ใช่สเตียรอยด์ (NSAIDs) และ / หรือ prednisone (≤0.2 มก. / กก. / วันหรือสูงสุด 10 มก. / วัน) อย่างต่อเนื่อง ในช่วง OL LI ผู้ป่วยทุกรายได้รับ Humira 24 มก. / m2 สูงสุด 40 มก. ทุกสัปดาห์ เป็นเวลา 16 สัปดาห์ การกระจายตัวของผู้ป่วยตามอายุและขนาดยาต่ำสุด เฉลี่ย และสูงสุดที่ได้รับระหว่างระยะ OL LI แสดงไว้ในตารางที่ 3
ตารางที่ 3
การกระจายของผู้ป่วยตามอายุและขนาดยา adalimumab ที่ได้รับระหว่างระยะ OL LI
ผู้ป่วยที่แสดงการตอบสนอง ACR30 ในเด็กในสัปดาห์ที่ 16 มีสิทธิ์ได้รับการสุ่มให้เข้าสู่ระยะ Double Blind (DB) และได้รับ Humira 24 มก. / ม. 2 สูงสุด 40 มก. หรือยาหลอก ทุกสัปดาห์เว้นอีก 32 สัปดาห์หรือจนกว่าจะเกิดโรค วู่วาม. เกณฑ์สำหรับการกำหนดการกำเริบของโรคถูกกำหนดบนพื้นฐานของการแย่ลงมากกว่าหรือเท่ากับ 30% (≥ 30%) เมื่อเทียบกับค่าพื้นฐาน 3 หรือมากกว่าจาก 6 เกณฑ์หลักของ "ACR Pediatric core" ใน การปรากฏตัวของข้อต่อที่ใช้งาน 2 ข้อขึ้นไปและขึ้นอยู่กับการปรับปรุงมากกว่า 30% ในเกณฑ์ไม่เกิน 1 ใน 6 ข้อข้างต้น หลังจาก 32 สัปดาห์หรือเมื่อโรคกำเริบขึ้นผู้ป่วยจะถือว่ามีสิทธิ์เข้ารับการรักษา เปิดเฟสขยาย.
ตารางที่ 4
การตอบสนอง PedACR 30 ระหว่างการศึกษา JIA
การตอบสนองของ PedACR 30/50/70 ในสัปดาห์ที่ 48 มีค่ามากกว่าที่ได้รับในผู้ป่วยที่ได้รับยาหลอกอย่างมีนัยสำคัญ
b p = 0.015
c p = 0.031
ในบรรดาผู้ที่ตอบสนองต่อการรักษาในสัปดาห์ที่ 16 (n = 144) การตอบสนองของ Ped ACR 30/50/70/90 นั้นคงอยู่นานถึงหกปีในช่วง OLE ในผู้ป่วยที่ได้รับ Humira ระหว่างการทำทั้งสตูดิโอ โดยรวมแล้ว 19 คน รวมทั้ง 11 คนจากกลุ่มฐานอายุ 4 ถึง 12 และ 8 จากกลุ่มฐานอายุ 13 ถึง 17 ปี ได้รับการรักษาเป็นเวลา 6 ปีหรือมากกว่า
การตอบสนองโดยรวมดีขึ้นโดยทั่วไป และ ผู้ป่วยบางรายพัฒนาแอนติบอดีเมื่อรับการรักษาด้วย Humira และ MTX ร่วมกับการรักษา Humira เพียงอย่างเดียว เมื่อคำนึงถึงผลลัพธ์เหล่านี้ แนะนำให้ใช้ Humira ร่วมกับ MTX และเป็นยาเดี่ยวในผู้ป่วยที่ไม่แนะนำให้ใช้ MTX (ดูหัวข้อ 4.2)
pJIA II
ความปลอดภัยและประสิทธิภาพของ Humira ได้รับการประเมินในการศึกษาแบบ multicenter แบบ open-label ในเด็ก 32 คน (พื้นที่ผิวกาย 2-2 ตัวของ Humira สูงสุด 20 มก. ทุกสัปดาห์เป็นขนาดเดียวใต้ผิวหนังเป็นเวลาอย่างน้อย 24 สัปดาห์ ในการศึกษานี้ อาสาสมัครส่วนใหญ่ใช้ MTX พร้อมกัน โดยบางวิชารายงานการใช้คอร์ติโคสเตียรอยด์หรือยาต้านการอักเสบที่ไม่ใช่สเตียรอยด์ (NSAIDs)
ในสัปดาห์ที่ 12 และสัปดาห์ที่ 24 การตอบสนองของ PedACR30 เท่ากับ 93.5% และ 90.0% ตามลำดับ โดยใช้วิธีข้อมูลที่สังเกตได้ สัดส่วนของอาสาสมัครที่ได้รับ PedACR50 / 70/90 ในสัปดาห์ที่ 12 และสัปดาห์ที่ 24 เท่ากับ 90.3% / 61.3% / 38.7% และ 83.3% / 73.3% / 36.7%.ในบรรดาผู้ที่ตอบสนอง (PedACR30) ในสัปดาห์ที่ 24 (n = 27 คนจาก 30 ราย) การตอบสนองของ PedACR30 ยังคงรักษาไว้ได้นานถึง 60 สัปดาห์ในผู้ป่วยที่ได้รับ Humira ในช่วงเวลานี้ในการศึกษาส่วนขยายแบบเปิดฉลาก ทั้งหมด 20 คนได้รับการรักษาเป็นเวลา 60 สัปดาห์หรือนานกว่านั้น
โรคข้ออักเสบที่เกี่ยวข้องกับ enthesitis
ความปลอดภัยและประสิทธิภาพของ Humira ได้รับการประเมินในการศึกษาแบบ multicentre, randomized, double-blind ในผู้ป่วยเด็ก 46 คน (อายุ 6 ถึง 17 ปี) ที่มีโรคไขข้ออักเสบในระดับปานกลาง ผู้ป่วยได้รับการสุ่มให้ได้รับหรือ Humira 24 มก. / ตร.ม. พื้นผิวร่างกาย สูงสุด 40 มก. หรือยาหลอกทุก ๆ สัปดาห์เป็นเวลา 12 สัปดาห์ ตามด้วยระยะเวลาการศึกษาแบบ open-label ซึ่งผู้ป่วยได้รับ Humira 24 มก. / ตร.ม. พื้นที่ผิวกายสูงถึง a ฉีดเข้าใต้ผิวหนังสูงสุด 40 มก. ทุกสัปดาห์ เพิ่มอีก 192 สัปดาห์ จุดยุติหลักคือเปอร์เซ็นต์การเปลี่ยนแปลงของจำนวนข้อต่อที่มีโรคข้ออักเสบเชิงรุกจากการตรวจวัดพื้นฐานเป็นสัปดาห์ที่ 12 (อาการบวมไม่ได้เกิดจากการผิดรูปหรือข้อต่อที่สูญเสียการเคลื่อนไหวบวกกับความเจ็บปวด และ / หรือความอ่อนโยน) และประสบความสำเร็จโดยมีค่าเฉลี่ยลดลง -62.6% (การเปลี่ยนแปลงร้อยละมัธยฐาน - 88.9%) ในผู้ป่วยในกลุ่ม Humira เทียบกับ -11.6% (การเปลี่ยนแปลงร้อยละมัธยฐาน - 50.0%) ในผู้ป่วยในกลุ่มยาหลอก การปรับปรุงจำนวนของข้อต่อที่ใช้งานกับโรคข้ออักเสบยังคงรักษาไว้ในช่วงระยะเวลาเปิดฉลากของการศึกษาจนถึงสัปดาห์ที่ 52 แม้ว่าจะไม่มีนัยสำคัญทางสถิติ แต่ผู้ป่วยส่วนใหญ่มีการปรับปรุงทางคลินิกในจุดยุติทุติยภูมิ เช่น จำนวนจุดเกิดการอักเสบ , จำนวนข้อที่เจ็บปวด (TJC), จำนวนข้อบวม (SJC), การตอบสนอง ACR 50 ในเด็ก และการตอบสนอง ACR 70 ในเด็ก
โรคข้ออักเสบรูมาตอยด์ในผู้ใหญ่
Humira ได้รับการประเมินในผู้ป่วยมากกว่า 3,000 รายในการทดลองทางคลินิกทั้งหมดเกี่ยวกับโรคข้ออักเสบรูมาตอยด์ ประสิทธิภาพและความปลอดภัยของ Humira ได้รับการประเมินในการศึกษาแบบสุ่ม ผู้ป่วยบางรายได้รับการรักษานานถึง 120 เดือน
การศึกษา RA I ดำเนินการในผู้ป่วย 271 รายที่มีอายุ≥ 18 ปีที่เป็นโรคข้ออักเสบรูมาตอยด์ที่ดื้อต่อยาปานกลางถึงรุนแรงถึงอย่างน้อยหนึ่ง DMARD รวมถึง methotrexate ในขนาดตั้งแต่ 12.5 ถึง 25 มก. (10 มก. หากไม่ทนต่อ methotrexate) ต่อสัปดาห์ และยังคงมีปริมาณยา methotrexate อยู่ คงที่ที่ 10-25 มก. ต่อสัปดาห์ Humira 20, 40 หรือ 80 มก. หรือยาหลอกได้รับทุกสัปดาห์เว้น 24 สัปดาห์
การศึกษา AR II ได้ทำการศึกษาผู้ป่วย 544 คนที่มีอายุระหว่าง 18 ปีขึ้นไปที่เป็นโรคข้ออักเสบรูมาตอยด์ระดับปานกลางถึงรุนแรง โดยมีการตอบสนองต่อยา DMARD อย่างน้อยหนึ่งตัวไม่เพียงพอ ปริมาณ Humira 20 หรือ 40 มก. ได้รับโดยการฉีดใต้ผิวหนังทุกสองสัปดาห์ด้วยยาหลอกทุกสัปดาห์หรือทุกสัปดาห์เป็นเวลา 26 สัปดาห์; ยาหลอกได้รับทุกสัปดาห์ในช่วงเวลาเดียวกัน ไม่อนุญาตให้ใช้ DMARD อื่นๆ
การศึกษา AR III เกี่ยวข้องกับผู้ป่วย 619 รายที่มีอายุ≥ 18 ปี ที่เป็นโรคข้ออักเสบรูมาตอยด์ระดับปานกลางถึงรุนแรงที่มีการตอบสนองต่อการรักษาด้วยยา methotrexate ไม่เพียงพอในขนาดตั้งแต่ 12.5 ถึง 25 มก. หรือไม่สามารถทนต่อยา methotrexate ได้ถึง 10 มก. ทุกสัปดาห์ ในการศึกษาครั้งนี้มีการสร้าง 3 กลุ่ม อดีตได้รับการฉีดยาหลอกทุกสัปดาห์เป็นเวลา 52 สัปดาห์ คนที่สองได้รับ Humira 20 มก. ต่อสัปดาห์เป็นเวลา 52 สัปดาห์ ในขณะที่คนที่สามได้รับ Humira 40 มก. ทุกสองสัปดาห์และฉีดยาหลอกทุกสัปดาห์ เมื่อเสร็จสิ้น 52 สัปดาห์แรก ผู้ป่วย 457 รายได้รับการลงทะเบียนในระยะขยายฉลากแบบเปิดซึ่ง Humira / MTX ให้ในขนาด 40 มก. ทุกสัปดาห์เว้นเป็นเวลาสูงสุด 10 ปี
การศึกษา AR IV ครั้งแรกประเมินความปลอดภัยของ Humira ในผู้ป่วย 636 รายที่เป็นโรคข้ออักเสบรูมาตอยด์ระดับปานกลางถึงรุนแรงที่มีอายุ≥ 18 ปี ประชากรที่ศึกษาประกอบด้วยผู้ป่วยทั้งสองรายที่ไม่เคยได้รับการรักษาด้วย DMARD และผู้ป่วยที่ยังคงรักษาด้วยยาต้านรูมาติกที่มีอยู่ก่อนแล้วโดยที่การรักษาจะคงที่เป็นเวลาอย่างน้อย 28 วัน การรักษาเหล่านี้รวมถึง methotrexate, leflunomide, hydroxychloroquine, sulfasalazine และ / หรือเกลือทอง ผู้ป่วยได้รับการสุ่มให้รับ Humira 40 มก. หรือยาหลอกทุกสองสัปดาห์เป็นเวลา 24 สัปดาห์
การศึกษา AR V ประเมินผู้ป่วยผู้ใหญ่ 799 คนที่ไม่เคยได้รับการรักษาด้วย methotrexate มาก่อนและมีอาการข้ออักเสบรูมาตอยด์ในระยะเริ่มแรกในระดับปานกลางถึงรุนแรง (ระยะเวลาเฉลี่ยของโรคน้อยกว่า 9 เดือน) การศึกษานี้ประเมินประสิทธิภาพของ Humira 40 มก. ที่ได้รับทุกสัปดาห์ร่วมกับ methotrexate, Humira 40 มก. ให้เป็นยาเดี่ยวทุกสัปดาห์และ methotrexate เพียงอย่างเดียวในการลดสัญญาณและอาการของโรคและดัชนีความก้าวหน้าของความเสียหายร่วมที่เกิดจากโรคข้ออักเสบรูมาตอยด์สำหรับ 104 สัปดาห์
จุดยุติหลักของการศึกษา AR I, II, III และจุดยุติทุติยภูมิของ AR IV คือการประเมินสัดส่วนของผู้ป่วยที่ได้รับการตอบสนอง ACR 20 ในสัปดาห์ที่ 24 หรือ 26 จุดสิ้นสุดหลักของการศึกษา AR V คือการประเมินเปอร์เซ็นต์ ของผู้ป่วยที่บรรลุการตอบสนอง ACR 50 ในสัปดาห์ที่ 52 นอกจากนี้ การศึกษา AR III และ V มีวัตถุประสงค์หลักเพื่อแสดงให้เห็นถึงการยับยั้งการลุกลามของโรค (ผ่านการตรวจด้วยภาพรังสี) ในสัปดาห์ที่ 52 การศึกษา AR III ยังมีวัตถุประสงค์หลักเพื่อ แสดงให้เห็นถึงคุณภาพชีวิตที่ดีขึ้น
การตอบสนอง ACR
เปอร์เซ็นต์ของผู้ป่วยที่ได้รับ Humira ที่ได้รับการตอบสนอง ACR 20, 50 และ 70 นั้นเทียบได้ในการศึกษา AR I, II และ III ผลลัพธ์สำหรับการรักษาด้วยยา 40 มก. ทุกสองสัปดาห์สรุปไว้ในตารางที่ 5
ในการศึกษา RA I-IV พารามิเตอร์ทั้งหมดที่ประเมินสำหรับคำจำกัดความของการตอบสนอง ACR (จำนวนของข้อต่อที่เจ็บปวดและบวม การประเมินกิจกรรมของโรคโดยแพทย์และผู้ป่วย การประเมินความเจ็บปวดโดยผู้ป่วย ดัชนีความทุพพลภาพ - HAQ) และค่า CRP (mg / dL) ดีขึ้นที่ 24 หรือ 26 สัปดาห์เมื่อเทียบกับยาหลอก ในการศึกษา AR III การปรับปรุงเหล่านี้คงอยู่นานกว่า 52 สัปดาห์
ในระยะขยายฉลากแบบเปิดของการศึกษา AR III ผู้ป่วยส่วนใหญ่ที่ได้รับการตอบสนองจาก ACR จะคงการตอบสนองไว้เมื่อรักษาต่อเนื่องเป็นเวลา 10 ปี จากผู้ป่วยทั้งหมด 207 ราย 114 รายยังคงให้ Humira 40 มก. ทุกสัปดาห์เว้น 5 ปี ในจำนวนนี้ ผู้ป่วย 86 ราย (75.4%) มีการตอบสนอง ACR 20; ผู้ป่วย 72 ราย (63.2%) มีการตอบสนอง ACR 50; และผู้ป่วย 41 ราย (36%) มีการตอบสนอง ACR 70 จากผู้ป่วยทั้งหมด 207 ราย 81 รายยังคงรักษาด้วย Humira 40 มก. ทุกสัปดาห์เว้น 10 ปี ในจำนวนนี้ ผู้ป่วย 64 ราย (79.0%) มีการตอบสนอง ACR 20; ผู้ป่วย 56 ราย (69.1%) มีการตอบสนอง ACR 50; และผู้ป่วย 43 ราย (53.1%) มีการตอบสนอง ACR 70
ในการศึกษา RA IV การตอบสนอง ACR 20 ของผู้ป่วยที่ได้รับ Humira ร่วมกับการรักษาแบบเดิมมีนัยสำคัญทางสถิติดีกว่าผู้ป่วยที่ได้รับยาหลอกร่วมกับยาแผนโบราณ (p
ในการศึกษา RA I-IV ผู้ป่วยที่ได้รับ Humira ได้รับการตอบสนอง ACR 20 และ 50 ที่สูงกว่าอย่างมีนัยสำคัญทางสถิติอย่างมีนัยสำคัญทางสถิติในช่วง 1-2 สัปดาห์หลังจากเริ่มการรักษา
ในการศึกษา RA V ในผู้ป่วยที่เป็นโรคข้ออักเสบรูมาตอยด์ในระยะเริ่มต้นที่ไม่เคยได้รับการรักษาด้วย methotrexate มาก่อน การรักษาแบบผสมผสานของ Humira / methotrexate ส่งผลให้การตอบสนอง ACR เร็วขึ้นและมีนัยสำคัญมากกว่า methotrexate monotherapy และ Humira monotherapy ในสัปดาห์ที่ 52 และการตอบสนองเหล่านี้ยังคงมีอยู่นานกว่า 104 สัปดาห์ ( ดูตารางที่ 6)
ในสัปดาห์ที่ 52 ผู้ป่วย 42.9% ที่ได้รับการบำบัดร่วมกับ Humira / methotrexate ได้รับการบรรเทาอาการทางคลินิก (DAS28)
การตอบสนองทางรังสี
ในการศึกษา AR III ซึ่งผู้ป่วยที่ได้รับการรักษาด้วย Humira มีระยะเวลาของโรคเฉลี่ยประมาณ 11 ปี ความเสียหายของโครงสร้างได้รับการประเมินด้วยการถ่ายภาพรังสีและแสดงเป็นการเปลี่ยนแปลงใน Total Sharp Score (TSS) ที่แก้ไขแล้วและส่วนประกอบที่เกี่ยวข้อง การกัดเซาะ และการลดช่องว่างของข้อต่อ ดัชนี (JSN) ผู้ป่วยที่ได้รับการรักษาด้วย Humira / MTX มีความก้าวหน้าทางรังสีน้อยกว่าผู้ป่วยที่ได้รับ MTX เพียงอย่างเดียวที่ 6 และ 12 เดือน (ดูตารางที่ 7) อย่างมีนัยสำคัญ
ในการขยายฉลากแบบเปิดของการศึกษา AR III การลดอัตราการลุกลามของความเสียหายของโครงสร้างจะคงอยู่เป็นเวลา 8 และ 10 ปีในกลุ่มย่อยของผู้ป่วย เมื่ออายุ 8 ปี ผู้ป่วย 81 คนจาก 207 คนได้รับการรักษาด้วย Humira 40 มก. ทุกๆ สัปดาห์อื่นๆ มีผู้ป่วย 48 รายที่ไม่พบความก้าวหน้าของความเสียหายเชิงโครงสร้างที่กำหนดโดยการเปลี่ยนแปลงของ mTSS ที่ 0.5 หรือน้อยกว่าจากการตรวจวัดพื้นฐาน เมื่ออายุ 10 ปี ผู้ป่วย 79 รายจาก 207 รายที่ได้รับการรักษาด้วย Humira 40 มก. ทุกสัปดาห์เว้นสัปดาห์นี้มีผู้ป่วย 40 ราย ไม่แสดงความคืบหน้าของความเสียหายเชิงโครงสร้างที่กำหนดโดยการเปลี่ยนแปลงใน mTSS 0.5 หรือน้อยกว่าจากการตรวจวัดพื้นฐาน
ตารางที่ 7
การเปลี่ยนแปลงภาพรังสีเฉลี่ยหลังจาก 12 เดือนในการศึกษา AR III
เพื่อ methotrexate
b ช่วงความเชื่อมั่น 95% สำหรับความแตกต่างในการเปลี่ยนแปลงดัชนีระหว่าง methotrexate และ Humira
c ขึ้นอยู่กับการวิเคราะห์อันดับ
d Joint Space Narrowing (การลดช่องว่างร่วม)
ในการศึกษา AR V ความเสียหายของข้อต่อของโครงสร้างได้รับการประเมินโดยการถ่ายภาพรังสีและแสดงในแง่ของการเปลี่ยนแปลงใน Total Sharp Score ที่แก้ไขแล้ว (ดูตารางที่ 8)
หลังการรักษา 52 สัปดาห์และ 104 สัปดาห์ สัดส่วนของผู้ป่วยที่ไม่คืบหน้า (เปลี่ยนจากค่าพื้นฐานใน Total Sharp Score ที่แก้ไข ≤ 0.5) สูงขึ้นอย่างมีนัยสำคัญเมื่อใช้ Humira / methotrexate combination therapy ( 63.8% และ 61.2% ตามลำดับ) เมื่อเทียบกับ methotrexate monotherapy (37.4% และ 33.5% ตามลำดับ p
คุณภาพชีวิตและสมรรถภาพทางกาย
คุณภาพชีวิตและการทำงานทางกายภาพได้รับการประเมินด้วยดัชนีความทุพพลภาพที่ได้รับจากแบบสอบถามการประเมินสุขภาพ (HAQ) ในการศึกษาดั้งเดิมสี่ฉบับที่เพียงพอและมีการควบคุมอย่างดีและเป็นหนึ่งในจุดสิ้นสุดหลักของการศึกษา AR III ในสัปดาห์ที่ 52 ทั้งหมด สูตรควบคุมของ Humira ในการศึกษาทั้งสี่แสดงให้เห็นการปรับปรุงอย่างมีนัยสำคัญทางสถิติในดัชนีความทุพพลภาพของ HAQ ระหว่างการตรวจวัดพื้นฐานและเดือนที่ 6 เมื่อเทียบกับยาหลอกและในการศึกษา AR III ผลลัพธ์เดียวกันถูกสังเกตพบในสัปดาห์ที่ 52 การวิเคราะห์สถานะสุขภาพทั่วไป ประเมินโดย Short แบบสำรวจสุขภาพ (SF -36) ในการศึกษาทั้งสี่ฉบับ สนับสนุนข้อสรุปเหล่านี้สำหรับสูตรการให้ยา Humira ทั้งหมดที่มีผลลัพธ์ที่มีนัยสำคัญทางสถิติ เกี่ยวกับดัชนีของการออกกำลังกาย ความเจ็บปวด และความเป็นอยู่ที่ดี บันทึกด้วย Humira 40 มก. ต่อสัปดาห์ สลับกัน การลดลงอย่างมีนัยสำคัญทางสถิติในความรู้สึกของความเหนื่อยล้าตามที่แสดงโดยดัชนีของการประเมินการทำงานที่เกี่ยวข้องกับการรักษาโรคเรื้อรัง (FACIT) พบในการศึกษาทั้งสามซึ่งได้รับการประเมิน (การศึกษา AR I, III, IV)
ในการศึกษา AR III อาสาสมัครส่วนใหญ่ที่ได้รับการปรับปรุงสมรรถภาพทางกายและผู้ที่รักษาอย่างต่อเนื่องยังคงรักษาการปรับปรุงเป็นเวลา 520 สัปดาห์ (120 เดือน) ของการรักษาแบบเปิดฉลาก คุณภาพชีวิตที่ดีขึ้นวัดได้จนถึงสัปดาห์ที่ 156 (36 เดือน) และปรับปรุงอย่างต่อเนื่องเมื่อเวลาผ่านไป
ในการศึกษา AR V ดัชนีความพิการที่ประเมินตาม HAQ และองค์ประกอบทางกายภาพของ SF 36 พบว่ามีการปรับปรุงที่เหนือกว่า (p
โรคโครห์นในผู้ป่วยเด็ก
Humira ได้รับการทดสอบในการทดลองทางคลินิกแบบ double-blind multicentre แบบสุ่ม ที่ออกแบบมาเพื่อประเมินประสิทธิภาพและความปลอดภัยของการเหนี่ยวนำและการรักษาที่ขึ้นกับน้ำหนักโดยขึ้นอยู่กับน้ำหนัก (30. อาสาสมัครต้องล้มเหลวในการรักษาแบบเดิม (รวมถึง corticosteroid และ / หรือ immunomodulator) ) สำหรับซีดี และอาสาสมัครอาจสูญเสียการตอบสนองก่อนหน้านี้หรือไม่ทนต่อ infliximab
ทุกวิชาได้รับการบำบัดด้วยการชักนำแบบเปิดฉลากโดยให้ยาตามน้ำหนักตัวที่การตรวจวัดพื้นฐาน: 160 มก. ในสัปดาห์ที่ 0 และ 80 มก. ในสัปดาห์ที่ 2 สำหรับผู้ที่มีน้ำหนัก ≥ 40 กก. และ 80 มก. และ 40 มก. ตามลำดับ สำหรับผู้ที่มีน้ำหนัก
ในสัปดาห์ที่ 4 ตามน้ำหนักตัว อาสาสมัครได้รับการสุ่มตัวอย่าง 1: 1 กับสูตรการบำรุงรักษาปริมาณต่ำหรือปริมาณมาตรฐานตามที่แสดงในตารางที่ 9
ผลลัพธ์ประสิทธิผล
จุดสิ้นสุดหลักของการศึกษาคือการบรรเทาอาการทางคลินิกในสัปดาห์ที่ 26 ซึ่งกำหนดโดยคะแนน PCDAI ≤ 10
อัตราภาวะทุเลาทางคลินิกและการตอบสนองทางคลินิก (กำหนดเป็นคะแนน PCDAI ที่ลดลงอย่างน้อย 15 คะแนนจากการตรวจวัดพื้นฐาน) แสดงไว้ในตารางที่ 10 อัตราการหยุดยาคอร์ติโคสเตียรอยด์หรือเครื่องกระตุ้นภูมิคุ้มกันแสดงไว้ในตารางที่ 11
เพิ่มขึ้นอย่างมีนัยสำคัญทางสถิติ (การปรับปรุง) ในดัชนีมวลกายและอัตราการเติบโตจากพื้นฐานถึงสัปดาห์ที่ 26 และ 52 สำหรับทั้งสองกลุ่มการรักษา
นอกจากนี้ยังพบการปรับปรุงอย่างมีนัยสำคัญทางสถิติและทางคลินิกจากค่าพื้นฐานในพารามิเตอร์คุณภาพชีวิต (รวมถึง IMPACT III) ในกลุ่มการรักษาทั้งสองกลุ่ม
โรคโครห์นในผู้ใหญ่
ความปลอดภัยและประสิทธิภาพของ Humira ได้รับการประเมินในผู้ป่วยมากกว่า 1500 รายที่มีโรค Crohn ในระดับปานกลางถึงรุนแรง (ดัชนีกิจกรรมโรคของ Crohn (CDAI) ≥ 220 และ≤ 450) ในการทดลองแบบสุ่ม อนุญาตให้ใช้ยา aminosalicylates, corticosteroids และ / หรือ immunomodulatory ในปริมาณคงที่ร่วมกันและผู้ป่วย 80% ยังคงใช้ยาเหล่านี้อย่างน้อยหนึ่งตัว
การชักนำให้เกิดการให้อภัยทางคลินิก (กำหนดเป็น CDAI
การรักษาภาวะทุเลาทางคลินิกได้รับการประเมินในการศึกษาซีดี III (CHARM) ในการศึกษาซีดี III ผู้ป่วย 854 รายได้รับยา Humira 80 มก. ในสัปดาห์ที่ 0 และ 40 มก. ในสัปดาห์ที่ 2ในสัปดาห์ที่ 4 ผู้ป่วยได้รับการสุ่มให้รับ 40 มก. ทุกสัปดาห์ 40 มก. ทุกสัปดาห์ หรือยาหลอก ระยะเวลาทั้งหมดของการศึกษาคือ 56 สัปดาห์ ผู้ป่วยที่มีการตอบสนองทางคลินิกที่เพียงพอ (CDAI ลดลง≥ 70) ในสัปดาห์ที่ 4 ได้รับการแบ่งชั้นและวิเคราะห์แยกจากผู้ที่ไม่ได้รับการตอบสนองทางคลินิกที่เพียงพอในสัปดาห์ที่ 4 อนุญาตให้ลดขนาดยาทีละน้อยได้ corticosteroids หลังจากสัปดาห์ที่ 8
อัตราการเหนี่ยวนำของการทุเลาและการตอบสนองทางคลินิกจากการศึกษาซีดี I และการศึกษาซีดี II แสดงไว้ในตารางที่ 12
อัตราการบรรเทาอาการที่คล้ายกันพบได้ในกลุ่มขนาดยาเหนี่ยวนำ 160/80 มก. และ 80/40 มก. ในสัปดาห์ที่ 8 และเหตุการณ์ไม่พึงประสงค์เกิดขึ้นบ่อยขึ้นในกลุ่มขนาดยา 160/80 มก. 80 มก.
ในการศึกษาซีดีที่ 3 ในสัปดาห์ที่ 4 ผู้ป่วย 58% (499/854) มีการตอบสนองทางคลินิกที่เพียงพอและได้รับการประเมินในการวิเคราะห์เบื้องต้น ในผู้ป่วยที่ได้รับการตอบสนองทางคลินิกอย่างเพียงพอในสัปดาห์ที่ 4 พบว่า 48% เคยสัมผัสมาก่อน เพื่อบำบัดด้วยยาปฏิปักษ์ของ TNF อื่น ๆ เปอร์เซ็นต์สำหรับการรักษาการให้อภัยและการตอบสนองทางคลินิกแสดงไว้ในตารางที่ 13 ผลลัพธ์ของการให้อภัยทางคลินิกยังคงค่อนข้างคงที่โดยไม่คำนึงถึงการได้รับยาต้านยาก่อนหน้านี้ -TNF
ในสัปดาห์ที่ 56 การรักษาในโรงพยาบาลและการผ่าตัดที่เกี่ยวข้องกับโรคลดลงอย่างมีนัยสำคัญทางสถิติเมื่อใช้ adalimumab เมื่อเทียบกับยาหลอก
ในผู้ป่วยที่ไม่ตอบสนองอย่างเพียงพอในสัปดาห์ที่ 4 พบว่า 43% ของผู้ป่วยที่ได้รับการรักษาด้วย Humira มีการตอบสนองที่เพียงพอในสัปดาห์ที่ 12 เมื่อเทียบกับ 30% ของผู้ป่วยที่ได้รับยาหลอก ผลลัพธ์เหล่านี้ชี้ให้เห็นว่าผู้ป่วยบางรายที่ไม่แสดงการตอบสนองที่เพียงพอในสัปดาห์ที่ 4 ได้รับประโยชน์จากการรักษาอย่างต่อเนื่องจนถึงสัปดาห์ที่ 12 การบำบัดที่ดำเนินต่อไปเกิน 12 สัปดาห์ไม่ได้นำไปสู่จำนวนการตอบสนองที่สูงขึ้นอย่างมีนัยสำคัญ (ดูหัวข้อ 4.2 )
ผู้ป่วย 117/276 รายจากการศึกษา CD I และ 272/777 รายจากการศึกษา CD II และ III ได้รับการติดตามด้วย adalimumab แบบ open-label อย่างน้อย 3 ปี ผู้ป่วย 88 และ 189 รายตามลำดับยังคงรักษาระดับการบรรเทาอาการทางคลินิก การตอบสนองทางคลินิก (CR-100) ได้รับการรักษาในผู้ป่วย 102 และ 233 รายตามลำดับ
คุณภาพชีวิต
ในการศึกษา CD I และ CD II การปรับปรุงอย่างมีนัยสำคัญทางสถิติในแบบสอบถามโรคลำไส้อักเสบเฉพาะโรค (IBDQ) ได้รับคะแนนรวมในสัปดาห์ที่ 4 ในผู้ป่วยที่สุ่มรับ Humira 80/40 มก. และ 160/80 มก. เมื่อเทียบกับยาหลอกและพบได้ที่ สัปดาห์ที่ 26 และ 56 ในการศึกษา D III รวมทั้งระหว่างกลุ่มการรักษา Humira เมื่อเทียบกับกลุ่มยาหลอก
ภูมิคุ้มกัน
การก่อตัวของแอนติบอดีต้าน adalimumab สัมพันธ์กับการกวาดล้างที่เพิ่มขึ้นและประสิทธิภาพของ adalimumab ลดลง ไม่มีความสัมพันธ์ที่ชัดเจนระหว่างการมีอยู่ของแอนติบอดีต้าน adalimumab กับการเกิดขึ้นของเหตุการณ์ไม่พึงประสงค์
ในผู้ป่วยโรคข้ออักเสบไม่ทราบสาเหตุ polyarticular อายุ 4-17 ปีแอนติบอดีต่อต้าน adalimumab พบในผู้ป่วย 15.8% (27/171) ที่ได้รับ adalimumab ในผู้ป่วยที่ไม่ได้รับ methotrexate ร่วมกับ Humira อุบัติการณ์คือ 25.6% (22/86) เทียบกับ 5.9% (5/85) เมื่อใช้ adalimumab ร่วมกับ methotrexate
ในผู้ป่วยที่เป็นโรคข้ออักเสบจากการอักเสบ พบว่าแอนติบอดีต้าน adalimumab ในผู้ป่วย 10.9% (5/46) ที่ได้รับการรักษาด้วย adalimumab ในผู้ป่วยที่ไม่ได้รับ methotrexate ร่วมกับ Humira อุบัติการณ์เท่ากับ 13.6% (3/22) เทียบกับ 8.3% (2/24) เมื่อใช้ adalimumab ร่วมกับ methotrexate
ผู้ป่วยในการศึกษาโรคข้ออักเสบรูมาตอยด์ได้รับการตรวจคัดกรองในช่วงเวลาต่างๆ สำหรับแอนติบอดีต่อ adalimumab ในช่วง 6 ถึง 12 เดือน ในการทดลองทางคลินิกที่สำคัญ ตรวจพบแอนติบอดีต่อ adalimumab ใน 5.5% (58/1053) ของผู้ป่วยที่ได้รับการรักษาด้วย adalimumab เปรียบเทียบ กับผู้ป่วยที่ได้รับยาหลอก 0.5% (2/370) ในผู้ป่วยที่ไม่ได้รับ methotrexate ร่วมกัน อุบัติการณ์คือ 12.4% เทียบกับ 0.6% เมื่อใช้ adalimumab ร่วมกับ methotrexate
เนื่องจากการทดสอบอิมมูโนเจนิซิตี้เป็นแบบจำเพาะของผลิตภัณฑ์ การเปรียบเทียบปริมาณแอนติบอดีกับผลิตภัณฑ์อื่นๆ จึงไม่เหมาะสม
05.2 คุณสมบัติทางเภสัชจลนศาสตร์
การดูดซึมและการกระจาย
หลังจากฉีดเข้าใต้ผิวหนัง 24 มก. / ม. 2 (สูงสุด 40 มก.) ทุกสัปดาห์สำหรับผู้ป่วยอายุ 4 ถึง 17 ปีที่มีโรคข้ออักเสบไม่ทราบสาเหตุ polyarticular juvenile idiopathic arthritis (JIA) ค่าเฉลี่ยสมดุลขั้นต่ำของความเข้มข้นของ adalimumab ในซีรัม (ค่าที่วัดได้จากสัปดาห์ที่ 20 ถึง 48) คือ 5.6 ± 5.6 ไมโครกรัม / มิลลิลิตร (102% CV) กับ adalimumab โดยไม่ใช้ methotrexate ร่วมกันและ 10.9 ± 5.2 μg / mL (47, 7% CV) ที่บริหารร่วมกับ methotrexate
ในผู้ป่วยที่มี polyarticular JIA อายุ 2 ถึง 2 ปี ความเข้มข้นของ adalimumab ในซีรัมของรางน้ำเฉลี่ยเท่ากับ 6.0 ± 6.1 μg / mL (101% CV) กับ adalimumab โดยไม่ต้องใช้ methotrexate ร่วมกัน และ 7.9 ± 5.6 mcg / mL (71.2% CV) เมื่อใช้ร่วมกับ methotrexate
หลังจากฉีดเข้าใต้ผิวหนัง 24 มก. / ม. 2 (สูงสุด 40 มก.) ทุกสัปดาห์สำหรับผู้ป่วยอายุ 6-17 ปีที่เป็นโรคข้ออักเสบที่เกี่ยวข้องกับการอักเสบ ค่าต่ำสุดเฉลี่ยของความเข้มข้นของ adalimumab ในซีรัมในสภาวะคงตัว (ค่าที่วัดได้ ที่สัปดาห์ที่ 24) มีค่าเท่ากับ 8.8 ± 6.6 ไมโครกรัม/มิลลิลิตรด้วย adalimumab โดยไม่ต้องใช้ methotrexate ร่วมกันและ 11.8 ± 4.3 mcg / mL เมื่อใช้ร่วมกับ methotrexate
ในผู้ป่วยเด็กที่มี CD ระดับปานกลางถึงรุนแรง ปริมาณ adalimumab แบบ open-label คือ 160/80 มก. หรือ 80/40 มก. ในสัปดาห์ที่ 0 และ 2 ตามลำดับ ขึ้นอยู่กับการตัดน้ำหนักตัวที่ 40 กก. ในสัปดาห์ที่ 4 ผู้ป่วยได้รับการสุ่มตัวอย่าง 1: 1 โดยพิจารณาจากน้ำหนักตัวในกลุ่มที่ได้รับยามาตรฐาน (40/20 มก. ทุกสัปดาห์) หรือขนาดต่ำ (20/10 มก. ทุกสัปดาห์เว้น) ค่าเฉลี่ยความเข้มข้น (± SD) ในซีรัมของระดับ adalimumab ในสัปดาห์ที่ 4 คือ 15.7 ± 6.6 มก. / มล. สำหรับผู้ป่วย≥ 40 กก. (160/80 มก.) และ 10.6 ± 6.1 มก. / มล. สำหรับผู้ป่วย
สำหรับผู้ป่วยที่เหลืออยู่ในการรักษาด้วยการสุ่มตัวอย่าง ความเข้มข้นของ adalimumab เฉลี่ย (± SD) ของรางในสัปดาห์ที่ 52 เท่ากับ 9.5 ± 5.6 มก. / มล. สำหรับกลุ่มขนาดยามาตรฐานและ 3.5 ± 2.2 มก. / มล. สำหรับกลุ่มขนาดต่ำ ความเข้มข้นของรางน้ำเฉลี่ยยังคงอยู่ในผู้ป่วยที่ยังคงได้รับการรักษา adalimumab ทุกสัปดาห์เว้น 52 สัปดาห์ สำหรับผู้ป่วยที่เพิ่มขนาดยาจากสัปดาห์อื่นเป็นสูตรการรักษารายสัปดาห์ ความเข้มข้นเฉลี่ย (± SD) ในซีรัมของ adalimumab ในสัปดาห์ที่ 52 เท่ากับ 15.3 ± 11.4 ไมโครกรัม / มิลลิลิตร (40/20 มก. ต่อสัปดาห์) และ 6.7 ± 3.5 ไมโครกรัม / มล. (20/10 มก. ต่อสัปดาห์)
ผู้ใหญ่
หลังจากได้รับยา adalimumab ขนาด 40 มก. ฉีดเข้าใต้ผิวหนัง การดูดซึมและการกระจายของ adalimumab ช้า โดยความเข้มข้นของซีรั่มสูงสุดเกิดขึ้นประมาณ 5 วันหลังการให้ยา การดูดซึมเฉลี่ยของ adalimumab จากการศึกษาทั้ง 3 ครั้งหลังการให้ยาฉีดเข้าใต้ผิวหนังขนาด 40 มก. หนึ่งครั้งเท่ากับ 64 %. หลังจากฉีดเข้าเส้นเลือดดำครั้งเดียว 0.25 ถึง 10 มก. / กก. ความเข้มข้นเป็นสัดส่วนของขนาดยา หลังจากขนาด 0.5 มก. / กก. (≈40 มก.) ระยะห่างระหว่าง 11 ถึง 15 มล. / ชม. ปริมาณการกระจาย (Vss) อยู่ในช่วง จาก 5 ถึง 6 ลิตร และครึ่งชีวิตเฉลี่ยของระยะสุดท้ายอยู่ที่ประมาณสองสัปดาห์ ความเข้มข้นของ Adalimumab ในน้ำไขข้อในผู้ป่วยโรคข้ออักเสบรูมาตอยด์ต่างๆ อยู่ระหว่าง 31-96% ของผู้ป่วยในซีรัม
หลังจากได้รับ adalimumab 40 มก. ฉีดเข้าใต้ผิวหนังทุกสองสัปดาห์ในผู้ป่วยผู้ใหญ่ที่เป็นโรคข้ออักเสบรูมาตอยด์ (RA) ความเข้มข้นของรางน้ำเฉลี่ยประมาณ 5 มก. / มล. (ไม่มี methotrexate ร่วมกัน) และ 8-9 มก. / มล. (ร่วมกับ methotrexate) ระดับของ adalimumab ที่สมดุลตามปริมาณที่ฉีดเข้าใต้ผิวหนัง 20, 40 และ 80 มก. ทุก 2 สัปดาห์หรือทุกสัปดาห์เพิ่มขึ้นในลักษณะที่เกือบจะขึ้นกับขนาดยา
การกำจัด
การวิเคราะห์เภสัชจลนศาสตร์ของประชากรในกลุ่มตัวอย่างของผู้ป่วย RA มากกว่า 1,300 ราย พบว่ามีแนวโน้มเพิ่มขึ้นอย่างเห็นได้ชัดในการกวาดล้าง adalimumab เมื่อน้ำหนักตัวเพิ่มขึ้น หลังจากแก้ไขน้ำหนักตัวแล้ว พบว่าความแตกต่างระหว่างเพศและอายุมีผลน้อยที่สุดต่อการกวาดล้าง adalimumab adalimumab ฟรี (unbound to anti-adalimumab antibodies - AAA) ต่ำกว่าในผู้ป่วยที่มี AAA titers ที่วัดได้ Humira ยังไม่ได้รับการศึกษาในผู้ป่วยที่มีภาวะไตไม่เพียงพอหรือตับ
ตับหรือไตไม่เพียงพอ
Humira ยังไม่ได้รับการศึกษาในผู้ป่วยที่มีภาวะตับหรือไตไม่เพียงพอ
05.3 ข้อมูลความปลอดภัยพรีคลินิก
ข้อมูลที่ไม่ใช่ทางคลินิกเปิดเผยว่าไม่มีอันตรายพิเศษสำหรับมนุษย์โดยพิจารณาจากความเป็นพิษในครั้งเดียว ความเป็นพิษในขนาดยาซ้ำ และการศึกษาความเป็นพิษต่อพันธุกรรม
การศึกษาความเป็นพิษต่อพัฒนาการของทารกในครรภ์และทารกในครรภ์ได้ดำเนินการในลิง cynomologic ด้วยขนาด 0, 30 และ 100 มก. / กก. (9-17 ลิง / กลุ่ม); การศึกษานี้ไม่พบอันตรายต่อทารกในครรภ์ที่เกิดจาก adalimumab การทดสอบสารก่อมะเร็งและการประเมินภาวะเจริญพันธุ์แบบมาตรฐานและความเป็นพิษหลังคลอดไม่ได้ดำเนินการเนื่องจากขาดแบบจำลองที่เหมาะสมสำหรับแอนติบอดีที่มีปฏิกิริยาข้ามที่จำกัดต่อ TNF ในหนูและการพัฒนาแอนติบอดีที่ทำให้เป็นกลางในหนู
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
แมนนิทอล
กรดซิตริกโมโนไฮเดรต
โซเดียมซิเตรต
โซเดียมโมโนเบสิกฟอสเฟตไดไฮเดรต
ไดโซเดียม ฟอสเฟตไดไฮเดรต
เกลือแกง
โพลีซอร์เบต 80
โซเดียมไฮดรอกไซด์
น้ำฉีด.
06.2 ความเข้ากันไม่ได้
ในกรณีที่ไม่มีการศึกษาความเข้ากันได้ ยานี้ต้องไม่ผสมกับผลิตภัณฑ์ยาอื่น ๆ
06.3 ระยะเวลาที่ใช้ได้
24 เดือน
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
เก็บในตู้เย็น (2 ° C - 8 ° C) อย่าแช่แข็ง เก็บขวดในกล่องเพื่อป้องกันยาจากแสง
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
สารละลาย Humira 40 มก. สำหรับการฉีดบรรจุอยู่ในขวดขนาดเดียว (แก้วประเภท I) ปิดด้วยจุกยาง หุ้มด้วยชั้นอะลูมิเนียมและฝาปิดแบบพลิกออก
1 แพ็คๆละ 2 กล่องประกอบด้วย:
1 ขวด (สารละลายปราศจากเชื้อ 0.8 มล.), เข็มฉีดยาที่ปราศจากเชื้อ 1 อัน, เข็ม 1 อัน, อะแดปเตอร์ขวด 1 อันและผ้าเช็ดแอลกอฮอล์ 2 อัน
06.6 คำแนะนำในการใช้งานและการจัดการ
สารละลาย Humira 40 มก. สำหรับฉีดไม่มีสารกันบูด ยาที่ไม่ได้ใช้และของเสียที่ได้จากยานี้ต้องกำจัดตามระเบียบข้อบังคับของท้องถิ่น
07.0 ผู้ทรงอำนาจการตลาด
สาวใช้
SL6 4XE
สหราชอาณาจักร
08.0 หมายเลขอนุญาตการตลาด
EU / 1/03/256/001 40 มก. สารละลายสำหรับฉีด 1 ขวด 0.8 มล. + 1 เข็มฉีดยา + 2 สำลีสำหรับใช้ใต้ผิวหนัง 035946019 / E
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
วันที่ได้รับอนุญาตครั้งแรก: 8 กันยายน 2546
วันที่ต่ออายุครั้งล่าสุด: 8 กันยายน 2551
10.0 วันที่แก้ไขข้อความ
09/2014