สารออกฤทธิ์: กรด Risedronic (Risedronate sodium)
MEDEOROS 35 มก. เม็ดเคลือบฟิล์ม
เหตุใดจึงใช้ Medeoros? มีไว้เพื่ออะไร?
MEDEOROS อยู่ในกลุ่มของยาที่ไม่ใช่ฮอร์โมนที่เรียกว่า bisphosphonates ซึ่งใช้ในการรักษาโรคกระดูก (โรคกระดูกพรุน) มันทำหน้าที่โดยตรงกับกระดูก เสริมสร้างพวกเขา และลดความเสี่ยงของกระดูกหัก
กระดูกคือเนื้อเยื่อที่มีชีวิต ร่างกายจะขจัดเนื้อเยื่อกระดูกเก่าออกอย่างต่อเนื่องและแทนที่ด้วยกระดูกใหม่
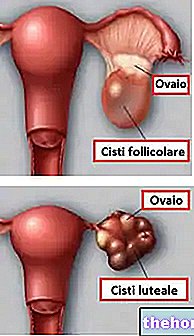
โรคกระดูกพรุนในวัยหมดประจำเดือนเป็นภาวะที่เกิดขึ้นในสตรีหลังวัยหมดประจำเดือนเมื่อกระดูกอ่อนตัวและบางลง ซึ่งส่งผลให้มีความเสี่ยงที่จะกระดูกหักเพิ่มขึ้นภายหลังจากการหกล้มหรือความเครียด
โรคกระดูกพรุนยังสามารถเกิดขึ้นได้ในผู้ชายจากสาเหตุต่างๆ เช่น อายุมากขึ้น และ/หรือฮอร์โมนเพศชายในระดับต่ำ ฮอร์โมนเทสโทสเตอโรน
กระดูกที่มีแนวโน้มแตกหักได้ง่ายที่สุดคือกระดูกสันหลัง สะโพก และข้อมือ แม้ว่ากระดูกทั้งหมดในร่างกายจะแตกหักได้ การแตกหักที่เกี่ยวข้องกับโรคกระดูกพรุนก็ทำให้เกิดอาการปวดหลัง ความสูงลดลง (น้ำหนักลด) , หลังหย่อนคล้อย (โคก) ). ผู้ป่วยโรคกระดูกพรุนจำนวนมากไม่มีอาการและไม่รู้ด้วยซ้ำว่ามีอาการดังกล่าว
MEDEOROS ใช้ในการรักษาโรคกระดูกพรุน:
- ในสตรีวัยหมดประจำเดือนแม้ในกรณีที่เป็นโรคกระดูกพรุนอย่างรุนแรง ลดความเสี่ยงของการแตกหักของกระดูกสันหลังและสะโพก
- ในผู้ชายที่มีความเสี่ยงสูงต่อการแตกหัก
ข้อห้าม เมื่อไม่ควรใช้ Medeoros
อย่าใช้ MEDEOROS:
- หากคุณแพ้ risedronate sodium หรือส่วนผสมอื่น ๆ ของยานี้
- หากคุณมีอาการที่เรียกว่าภาวะแคลเซียมในเลือดต่ำ (แคลเซียมในเลือดต่ำ)
- หากคุณกำลังตั้งครรภ์ สงสัยหรือกำลังวางแผนที่จะตั้งครรภ์
- หากคุณกำลังให้นมบุตร
- หากคุณมีปัญหาเกี่ยวกับไตอย่างรุนแรง
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนรับประทาน Medeoros
พูดคุยกับแพทย์หรือเภสัชกรของคุณก่อนรับประทาน MEDEOROS โดยเฉพาะ:
- หากคุณเคยมีปัญหาเกี่ยวกับหลอดอาหาร (ท่อที่เชื่อมปากของคุณกับท้องของคุณ) ซึ่งทำให้เกิดอาการปวดหรือกลืนอาหารลำบาก
- หากคุณไม่สามารถรักษาร่างกายส่วนบนให้ตรง (นั่งหรือยืน) เป็นเวลาอย่างน้อย 30 นาทีนับจากเวลาที่คุณใช้แท็บเล็ต
- หากคุณมีหรือเพิ่งมีปัญหากับหลอดอาหารของคุณ รวมทั้งหลอดอาหารของ Barrett (เงื่อนไขที่เกี่ยวข้องกับการเปลี่ยนแปลงในเซลล์ที่เรียงแถวหลอดอาหารล่าง);
- หากคุณมีความผิดปกติในการเผาผลาญของกระดูกและแร่ธาตุ (เช่น การขาดวิตามินดี ความผิดปกติของฮอร์โมนพาราไทรอยด์ซึ่งทำให้ระดับแคลเซียมในเลือดลดลง)
- หากคุณมีหรือเคยมีอาการปวด บวมหรือชาที่กราม หรือ 'รู้สึกกรามหนัก' หรือฟันหลุด
- หากคุณกำลังรับการรักษาโดยทันตแพทย์หรือวางแผนการผ่าตัดทางทันตกรรม โปรดแจ้งทันตแพทย์ว่าคุณกำลังรับการรักษาด้วย Risedronate sodium
- หากคุณมีอาการ "แพ้น้ำตาลบางชนิด (เช่น แลคโตส น้ำตาลนม) ผู้ป่วยที่มีปัญหาทางพันธุกรรมที่หาได้ยากจากการแพ้กาแลคโตส การขาดแลคเตส หรือการดูดซึมน้ำตาลกลูโคส-กาแลคโตสบกพร่อง ไม่ควรรับประทานยานี้ แพทย์ของคุณจะบอกคุณว่าต้องทำอย่างไร ทำในขณะที่ใช้ MEDEOROS หากคุณมีเงื่อนไขข้างต้น
เด็กและวัยรุ่น
ไม่แนะนำให้ใช้ risedronate sodium ในเด็กและวัยรุ่นที่มีอายุต่ำกว่า 18 ปี เนื่องจากข้อมูลด้านความปลอดภัยและประสิทธิภาพไม่เพียงพอ
ปฏิกิริยา ยาหรืออาหารชนิดใดที่สามารถเปลี่ยนแปลงผลของ Medeoros
ยาที่มีส่วนประกอบอย่างใดอย่างหนึ่งต่อไปนี้จะลดผลของ MEDEOROS เมื่อรับประทานพร้อมกัน:
- ฟุตบอล
- แมกนีเซียม
- เหล็ก
- อะลูมิเนียม (เช่น สารผสมบางชนิดสำหรับปัญหาทางเดินอาหาร)
ใช้ยาเหล่านี้อย่างน้อย 30 นาทีหลังจากรับประทาน MEDEOROS
แจ้งให้แพทย์หรือเภสัชกรทราบ หากคุณกำลังรับประทาน เพิ่งกำลังรับประทาน หรืออาจกำลังใช้ยาอื่นอยู่
MEDEOROS กับอาหารและเครื่องดื่ม
เป็นสิ่งสำคัญมากที่คุณจะต้องไม่รับประทานอาหารหรือเครื่องดื่ม (ยกเว้นน้ำประปา) ร่วมกับแท็บเล็ต MEDEOROS เพื่อให้ทำงานได้อย่างเหมาะสม โดยเฉพาะอย่างยิ่ง อย่ารับประทานยานี้พร้อมกับผลิตภัณฑ์นม (เช่น นม) เนื่องจาก มีแคลเซียม (ดูหัวข้อ 2 "ยาอื่นๆ และ MEDEOROS")
รับประทานอาหารและเครื่องดื่ม (ยกเว้นน้ำประปา) อย่างน้อย 30 นาทีหลังจากแท็บเล็ต MEDEOROS
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
การตั้งครรภ์และให้นมบุตร
อย่าใช้ MEDEOROS หากคุณกำลังตั้งครรภ์ คิดว่าคุณอาจกำลังตั้งครรภ์หรือกำลังวางแผนที่จะตั้งครรภ์ (ดูหัวข้อที่ 2 "อย่าใช้ MEDEOROS") ไม่ทราบความเสี่ยงที่อาจเกิดขึ้นจากการใช้ risedronate sodium (สารออกฤทธิ์ของ MEDEOROS) ในหญิงตั้งครรภ์
อย่าใช้ MEDEOROS หากคุณกำลังให้นมบุตร (ดูหัวข้อที่ 2 "อย่าใช้ MEDEOROS")
MEDEOROS ใช้สำหรับการรักษาสตรีและผู้ชายวัยหมดประจำเดือนเท่านั้น
การขับรถและการใช้เครื่องจักร
ไม่มีผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
MEDEOROS มีแลคโตส
หากคุณได้รับแจ้งจากแพทย์ว่าคุณแพ้น้ำตาลบางชนิด โปรดติดต่อแพทย์ก่อนใช้ยานี้ (ดูหัวข้อที่ 2 "คำเตือนและข้อควรระวัง")
ปริมาณ วิธีการ และระยะเวลาในการบริหาร วิธีใช้ Medeoros: Posology
ใช้ยานี้ตามที่แพทย์ของคุณบอกเสมอ หากมีข้อสงสัย ควรปรึกษาแพทย์หรือเภสัชกร
ปริมาณที่แนะนำคือ 1 เม็ด MEDEOROS (โซเดียม Risedronate 35 มก.) สัปดาห์ละครั้ง เลือกวันในสัปดาห์ที่เหมาะกับกิจกรรมของคุณมากที่สุด รับประทาน MEDEOROS หนึ่งเม็ดต่อสัปดาห์ในวันที่เลือก
กล่องมีช่องใส่ของ/ช่องว่าง จดวันในสัปดาห์ที่คุณเลือกใช้แท็บเล็ต MEDEOROS จดวันที่ที่คุณจะใช้แท็บเล็ตด้วย
รับประทานยาเม็ดแรกอย่างน้อย 30 นาทีก่อนอาหารมื้อแรกของวัน ดื่มครั้งแรก ยกเว้นน้ำประปา หรือก่อนยาอื่นๆ
ใช้แท็บเล็ตขณะยืนตัวตรง (นั่งหรือยืน) เพื่อหลีกเลี่ยงอาการเสียดท้อง กลืนแท็บเล็ตด้วยน้ำประปาอย่างน้อยหนึ่งแก้ว (120 มล.) ควรกลืนแท็บเล็ตทั้งหมด อย่าเคี้ยวหรือปล่อยให้แท็บเล็ตละลายในปากของคุณ อย่านอนลงเป็นเวลา 30 นาทีหลังจากกลืนแท็บเล็ต
แพทย์ของคุณจะบอกคุณว่าคุณต้องการอาหารเสริมแคลเซียมและวิตามินหรือไม่หากได้รับอาหารไม่เพียงพอ
หากคุณลืมทาน MEDEOROS
หากคุณลืมนำแท็บเล็ตไปตามเวลาปกติ ให้ทานในวันที่จำได้
ดำเนินการต่อโดยใช้หนึ่งเม็ดสัปดาห์ละครั้งในวันที่คุณเลือก
อย่าใช้สองเม็ดในวันเดียวกันเพื่อชดเชยยาเม็ดที่ถูกลืม
หากคุณหยุดใช้ MEDEOROS
หากคุณหยุดใช้ MEDEOROS คุณอาจเริ่มสูญเสียมวลกระดูก พูดคุยกับแพทย์ของคุณก่อนตัดสินใจหยุดใช้ยานี้
หากคุณมีคำถามเพิ่มเติมเกี่ยวกับการใช้ยานี้ ให้สอบถามแพทย์หรือเภสัชกรของคุณ
ยาเกินขนาด จะทำอย่างไรถ้าคุณได้รับ Medeoros มากเกินไป
หากคุณหรือผู้อื่นได้รับยาเม็ด MEDEOROS มากกว่าที่กำหนดโดยไม่ได้ตั้งใจ ให้ดื่มนมเต็มแก้วและปรึกษาแพทย์ทันที
ผลข้างเคียง ผลข้างเคียงของ Medeoros คืออะไร
เช่นเดียวกับยาอื่นๆ ยานี้อาจทำให้เกิดผลข้างเคียงได้ แม้ว่าจะไม่ใช่ทุกคนที่ได้รับก็ตาม
หยุดใช้ MEDEOROS และติดต่อแพทย์ทันทีหากคุณพบผลข้างเคียงใด ๆ ต่อไปนี้:
- อาการแพ้อย่างรุนแรง เช่น
- หน้า ลิ้น หรือคอบวม
- กลืนลำบาก
- wheals (ยกขึ้น, เป็นหย่อมสีแดง) และหายใจลำบาก
- ปฏิกิริยาผิวหนังพุพองอย่างรุนแรงรวมทั้งพุพอง
แจ้งให้แพทย์ทราบทันทีหากคุณสังเกตเห็นผลข้างเคียงต่อไปนี้: ตาอักเสบ มักมีอาการปวด ตาแดง และไวต่อแสง
เนื้อร้าย (การทำลาย) ของกระดูกในกราม (osteonecrosis) ที่เกี่ยวข้องกับการรักษาที่ล่าช้าและการเริ่มต้นของการติดเชื้อ ซึ่งมักจะเกิดขึ้นหลังจากการถอนฟัน (ดูหัวข้อที่ 2 "ก่อนรับประทาน MEDEOROS")
ความผิดปกติของหลอดอาหาร เช่น เจ็บขณะกลืน กลืนลำบาก เจ็บหน้าอก หรือเริ่มมีอาการ / อาการเสียดท้องแย่ลง
อย่างไรก็ตาม ผลข้างเคียงอื่น ๆ ที่พบในการทดลองทางคลินิกมักมีลักษณะไม่รุนแรง และไม่ต้องการให้ผู้ป่วยหยุดการรักษา
ทั่วไป (มีผลกับผู้ใช้ 1 ถึง 10 ใน 100):
- อาการอาหารไม่ย่อย, รู้สึกคลื่นไส้, ปวดท้อง, ปวดท้องหรือปวดท้อง, ท้องผูก, ท้องอืด, ท้องอืด (อากาศในลำไส้เพิ่มขึ้น), ท้องร่วง
- ปวดในกระดูก กล้ามเนื้อ หรือข้อต่อ
- ปวดศีรษะ.
ผิดปกติ (มีผลกับผู้ใช้ 1 ถึง 10 คนใน 1,000 คน):
- การอักเสบหรือแผลในหลอดอาหาร (ท่อที่เชื่อมระหว่างปากกับกระเพาะอาหาร) ซึ่งทำให้กลืนลำบากและเจ็บปวด (ดูหัวข้อที่ 2 "ก่อนรับประทาน MEDEOROS") การอักเสบของกระเพาะอาหารและลำไส้เล็กส่วนต้น (ส่วนแรกของลำไส้ที่ตามมา) ท้อง). - การอักเสบของส่วนที่มีสีของดวงตา (ม่านตา) (ตาสีแดงที่เจ็บปวดและการมองเห็นบกพร่องที่เป็นไปได้)
หายาก (มีผลกับผู้ใช้ 1 ถึง 10 คนใน 10,000):
- การอักเสบของลิ้น (บวมแดงและบางครั้งเจ็บปวด) หลอดอาหารตีบ (ท่อที่เชื่อมต่อปากกับกระเพาะอาหาร)
- มีรายงานความผิดปกติในการทดสอบการทำงานของตับ สิ่งเหล่านี้สามารถวินิจฉัยได้โดยการตรวจเลือด
มีการรายงานผลกระทบที่ไม่พึงประสงค์ต่อไปนี้ระหว่างประสบการณ์หลังการขาย:
ไม่ทราบ (ความถี่ไม่สามารถประมาณจากข้อมูลที่มีอยู่)
- ปฏิกิริยาภูมิแพ้ทางผิวหนังเช่นลมพิษ (ลมพิษ), ผื่นที่ผิวหนัง (ผิวแดงอย่างกะทันหัน), อาการบวมที่ใบหน้า, ริมฝีปาก, ลิ้นและ / หรือคอ, กลืนลำบากหรือหายใจลำบาก;
- ปฏิกิริยาทางผิวหนังอย่างรุนแรงรวมทั้งพุพองใต้ผิวหนัง การอักเสบของหลอดเลือดขนาดเล็กที่โดดเด่นด้วยจุดสีแดงบนผิวหนัง (leukocytoclastic vasculitis);
- ภาวะร้ายแรงที่เรียกว่ากลุ่มอาการสตีเวนส์ จอห์นสัน (SJS) โดยมีแผลพุพองที่ผิวหนัง ปาก ตา และบริเวณที่มีความชื้นอื่นๆ ของร่างกาย (อวัยวะเพศ) โรคร้ายแรงที่เรียกว่า toxic epidermal necrolysis (TEN) ซึ่งทำให้เกิดผื่นแดงในหลายส่วนของร่างกายและ / หรือการลอกของชั้นผิวหนังชั้นนอก
- ผมร่วง
- ปฏิกิริยาการแพ้ (ภูมิไวเกิน).
- ปัญหาเกี่ยวกับตับอย่างรุนแรง โดยเฉพาะอย่างยิ่งหากคุณกำลังรับการรักษาด้วยยาอื่นๆ ที่ทราบว่าทำให้เกิดปัญหาตับ
- การอักเสบของดวงตาทำให้เกิดอาการปวดและแดง
ในช่วงเริ่มต้นของการรักษา ระดับแคลเซียมและฟอสเฟตในเลือดของผู้ป่วยอาจลดลง
การเปลี่ยนแปลงเหล่านี้มักไม่รุนแรงและไม่มีอาการ
กระดูกโคนขาหักแบบผิดปกติอาจเกิดขึ้นได้ไม่บ่อยนักโดยเฉพาะในผู้ป่วยที่รักษาโรคกระดูกพรุนเป็นเวลานาน ติดต่อแพทย์ หากคุณมีอาการปวด อ่อนแรง หรือรู้สึกไม่สบายที่ต้นขา สะโพก หรือขาหนีบ เนื่องจากอาจเป็นสัญญาณบ่งชี้ในระยะเริ่มต้น การแตกหักของกระดูกโคนขา
หายากมาก (มีผลถึง 1 ใน 10,000 คน)
- ปรึกษาแพทย์หากคุณปวดหู หูอื้อ และ/หรือติดเชื้อที่หู อาการเหล่านี้อาจเป็นสัญญาณของความเสียหายของกระดูกในหูของคุณ
การรายงานผลข้างเคียง
หากคุณได้รับผลข้างเคียงใดๆ ให้ปรึกษาแพทย์หรือเภสัชกร ซึ่งรวมถึงผลข้างเคียงที่อาจเกิดขึ้นซึ่งไม่ได้ระบุไว้ในเอกสารฉบับนี้ คุณยังสามารถรายงานผลข้างเคียงได้โดยตรงผ่านทางเว็บไซต์ของหน่วยงานยาอิตาลี: www.agenziafarmaco.gov.it/it/responsabili การรายงานผลข้างเคียง คุณสามารถช่วยให้ข้อมูลเพิ่มเติมเกี่ยวกับความปลอดภัยของยานี้ได้
การหมดอายุและการเก็บรักษา
เก็บยานี้ให้พ้นสายตาและมือเด็ก
ยานี้ไม่ต้องการเงื่อนไขการจัดเก็บพิเศษใด ๆ
ห้ามใช้ยานี้หลังจากวันหมดอายุซึ่งระบุไว้บนกล่อง วันหมดอายุหมายถึงวันสุดท้ายของเดือนนั้น
ห้ามทิ้งยาลงในน้ำเสียหรือของเสียในครัวเรือน ถามเภสัชกรว่าจะทิ้งยาที่ไม่ได้ใช้แล้วอย่างไร ซึ่งจะช่วยปกป้องสิ่งแวดล้อม
ข้อมูลอื่น ๆ
MEDEOROS ประกอบด้วยอะไรบ้าง
- สารออกฤทธิ์คือไรโดรเนตโซเดียม แต่ละเม็ดประกอบด้วย risedronate sodium 35 มก. (ในรูปของ risedronate sodium hemipentahydrate)
- ส่วนประกอบอื่นๆ ได้แก่: แกนกลาง: ไมโครคริสตัลไลน์ เซลลูโลส, ครอสโพวิโดน, สเตียเรตแมกนีเซียม, แลคโตสโมโนไฮเดรต
- การเคลือบผิว: เหล็กออกไซด์สีแดง, เหล็กออกไซด์สีเหลือง, ซิลิกาคอลลอยด์ปราศจากน้ำ, ไททาเนียมไดออกไซด์, macrogol 400, macrogol 8000, hypromellose, ไฮดรอกซีโพรพิลเซลลูโลส
คำอธิบายของ MEDEOROS หน้าตาและเนื้อหาของแพ็ค
MEDEOROS เป็นเม็ดกลมเคลือบฟิล์มสีส้มอ่อน เส้นผ่านศูนย์กลาง 9 มม.
มีอยู่ในแผลพุพองที่มี 4 เม็ด
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่แสดงอาจไม่ทันสมัย
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
MEDEOROS 35 MG เม็ดเคลือบฟิล์ม
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
แต่ละเม็ดประกอบด้วย:
สารออกฤทธิ์: โซเดียม Risedronate 35 มก. (เป็น 40.2 มก. risedronate โซเดียม hemipentahydrate)
สารเพิ่มปริมาณที่ทราบผลกระทบ: แลคโตส
สำหรับรายการสารปรุงแต่งทั้งหมด ดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
เม็ดเคลือบฟิล์ม
เม็ดกลม สีส้มอ่อน เส้นผ่านศูนย์กลาง 9 มม.
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
การรักษาโรคกระดูกพรุนในวัยหมดประจำเดือนเพื่อลดความเสี่ยงของกระดูกหัก การรักษาโรคกระดูกพรุนในวัยหมดประจำเดือนอย่างชัดแจ้งเพื่อลดความเสี่ยงของกระดูกสะโพกหัก (ดูหัวข้อ 5.1)
การรักษาโรคกระดูกพรุนในผู้ชายที่มีความเสี่ยงสูงที่จะกระดูกหัก (ดูหัวข้อ 5.1)
04.2 วิทยาและวิธีการบริหาร
ปริมาณ
ปริมาณที่แนะนำสำหรับผู้ใหญ่คือหนึ่งเม็ด 35 มก. รับประทานสัปดาห์ละครั้ง ควรรับประทานยาเม็ดในวันเดียวกันทุกสัปดาห์
ประชากรเด็ก:
ไม่แนะนำให้ใช้ risedronate sodium ในเด็กอายุต่ำกว่า 18 ปีเนื่องจากข้อมูลด้านความปลอดภัยและประสิทธิภาพไม่เพียงพอ (ดูหัวข้อ 5.1 เพิ่มเติม)
ผู้ป่วยสูงอายุ:
ไม่จำเป็นต้องปรับขนาดยา เนื่องจากพบว่าการดูดซึม การกระจาย และการกำจัดในผู้สูงอายุ (> 60 ปี) มีความคล้ายคลึงกับผู้ป่วยที่อายุน้อยกว่า ซึ่งพบในผู้ป่วยสูงอายุมาก เช่น อายุ 75 ปี และเกินในวัยหมดประจำเดือน ประชากร.
การทำงานของไตบกพร่อง:
ไม่จำเป็นต้องปรับขนาดยาในผู้ป่วยที่มีภาวะไตวายเล็กน้อยถึงปานกลาง ห้ามใช้ risedronate sodium ในผู้ป่วยที่มีภาวะไตวายอย่างรุนแรง (creatinine clearance น้อยกว่า 30 มล. / นาที) (ดูหัวข้อ 4.3 และ 5.2)
วิธีการบริหาร
การดูดซึมของ risedronate sodium ได้รับผลกระทบจากอาหาร ดังนั้นเพื่อให้แน่ใจว่ามีการดูดซึมที่เพียงพอ ผู้ป่วยควรรับประทาน risedronate sodium:
• ก่อนอาหารเช้า: อย่างน้อย 30 นาทีก่อนรับประทานอาหารมื้อแรก ผลิตภัณฑ์ยาอื่นๆ หรือเครื่องดื่มประจำวัน (ยกเว้นน้ำประปา)
ผู้ป่วยควรได้รับคำแนะนำว่า หากลืมรับประทานยาเม็ด MEDEOROS 35 มก. ควรรับประทานในวันที่จำได้ ผู้ป่วยควรกลับมารับประทานยาเม็ดละ 1 เม็ดต่อสัปดาห์ในวันที่มักรับประทานยาเม็ด ไม่ควรรับประทาน 2 เม็ดในวันเดียวกัน
ควรกลืนยาเม็ดทั้งเม็ดและไม่ละลายในปากหรือเคี้ยว เพื่ออำนวยความสะดวกในการผ่านของเม็ดยาหลอดอาหาร ให้นำ Risedronate sodium กับน้ำประปาหนึ่งแก้ว (≥120 มล.) โดยให้ลำตัวตั้งตรง (ยืนหรือนั่ง) เมื่อกลืนกินยาเม็ดเข้าไปแล้ว ผู้ป่วยควรหลีกเลี่ยงเวลาเข้านอนเป็นเวลา 30 นาที (ดูหัวข้อ 4.4)
การเสริมแคลเซียมและวิตามินดีควรพิจารณาในกรณีที่รับประทานอาหารไม่เพียงพอ
ยังไม่มีการกำหนดระยะเวลาที่เหมาะสมในการรักษาโรคกระดูกพรุนด้วย bisphosphonate ความจำเป็นในการรักษาต่อเนื่องควรได้รับการประเมินใหม่ในผู้ป่วยแต่ละรายเป็นระยะตามประโยชน์และความเสี่ยงที่อาจเกิดขึ้น
04.3 ข้อห้าม
ภูมิไวเกินต่อสารออกฤทธิ์หรือสารเพิ่มปริมาณใด ๆ ที่ระบุไว้ในหัวข้อ 6.1
ภาวะแคลเซียมในเลือดต่ำ (ดูหัวข้อ 4.4)
การตั้งครรภ์และให้นมบุตร.
การด้อยค่าของไตอย่างรุนแรง (creatinine clearance
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
อาหาร เครื่องดื่ม (ยกเว้นน้ำประปา) และผลิตภัณฑ์ยาที่มีโพลีวาเลนท์ cation (เช่น แคลเซียม แมกนีเซียม เหล็ก และอลูมิเนียม) ขัดขวางการดูดซึมของบิสฟอสโฟเนต และไม่ควรรับประทานพร้อมๆ กับยาไรซ์โดรเนตโซเดียม (ดูหัวข้อ 4.5 )เพื่อให้บรรลุประสิทธิภาพที่ต้องการ ต้องปฏิบัติตามคำแนะนำในการบริหารอย่างเคร่งครัด (ดูหัวข้อ 4.2)
ประสิทธิภาพของ bisphosphonates ในการรักษาโรคกระดูกพรุนในวัยหมดประจำเดือนมีความสัมพันธ์กับความหนาแน่นของกระดูกลดลงและ / หรือความชุกของกระดูกหัก
อายุที่มากขึ้นหรือปัจจัยเสี่ยงทางคลินิกสำหรับกระดูกหักเพียงอย่างเดียวไม่ได้แสดงให้เห็นถึงการเริ่มต้นการรักษาโรคกระดูกพรุนด้วยบิสฟอสโฟเนต
มีหลักฐานที่จำกัดในการสนับสนุนประสิทธิภาพของบิสฟอสโฟเนตรวมทั้งโซเดียมไรเซโดรเนตในสตรีสูงอายุมาก (อายุมากกว่า 80 ปี) (ดูหัวข้อ 5.1)
บิสฟอสโฟเนตมีความเกี่ยวข้องกับหลอดอาหารอักเสบ โรคกระเพาะ แผลในหลอดอาหาร และแผลในกระเพาะอาหารและลำไส้ ดังนั้น ควรใช้ความระมัดระวัง:
• ในผู้ป่วยที่มีประวัติความผิดปกติของหลอดอาหารทำให้เกิดการขนส่งหลอดอาหารล่าช้าหรือการล้างข้อมูลในกระเพาะอาหาร เช่น การตีบหรือ achalasia;
• ในผู้ป่วยที่ไม่สามารถตั้งลำตัวให้ตั้งตรงได้อย่างน้อย 30 นาที นับจากเวลาที่รับประทานยาเม็ด
• หากใช้ risedronate sodium ในผู้ป่วยที่มีปัญหาในปัจจุบันหรือล่าสุดเกี่ยวกับระบบทางเดินอาหารส่วนบนหรือหลอดอาหาร (รวมทั้งหลอดอาหารของ Barrett)
แพทย์ควรเน้นให้ผู้ป่วยทราบถึงความสำคัญของการปฏิบัติตามคำแนะนำในการบริหารและตื่นตัวต่อสัญญาณหรืออาการใด ๆ ที่บ่งชี้ว่าอาจมีปฏิกิริยาต่อหลอดอาหาร ผู้ป่วยควรได้รับคำแนะนำว่าหากมีอาการระคายเคืองหลอดอาหาร เช่น กลืนลำบาก กลืนลำบาก ปวดหลัง หรือ เริ่มมีอาการ / กำเริบของอาการเสียดท้องควรไปพบแพทย์ทันที
ภาวะแคลเซียมในเลือดต่ำควรได้รับการแก้ไขก่อนเริ่มการรักษาด้วย Risedronate sodium นอกจากนี้ยังจำเป็นต้องแก้ไขการรบกวนอื่นๆ ของการเผาผลาญของกระดูกและแร่ธาตุ (เช่น ความผิดปกติของพาราไทรอยด์, ภาวะ hypovitaminosis D) เมื่อเริ่มการรักษาด้วย risedronate sodium
โรคกระดูกพรุนของขากรรไกรซึ่งมักเกี่ยวข้องกับการถอนฟันและ/หรือการติดเชื้อเฉพาะที่ (รวมถึงโรคกระดูกพรุน) มีรายงานในผู้ป่วยมะเร็งที่รักษาด้วยสูตรยา ซึ่งรวมถึง bisphosphonates ที่ฉีดเข้าเส้นเลือดดำเป็นหลัก ผู้ป่วยเหล่านี้จำนวนมากได้รับการรักษาด้วยเคมีบำบัดและคอร์ติโคสเตียรอยด์ ขากรรไกรยังได้รับการรายงานในผู้ป่วยโรคกระดูกพรุนที่ได้รับการรักษาด้วยยาบิสฟอสโฟเนตในช่องปาก
ก่อนเริ่มการรักษาด้วยบิสฟอสโฟเนตในผู้ป่วยที่มีปัจจัยเสี่ยงร่วมด้วย (เช่น มะเร็ง เคมีบำบัด รังสีรักษา คอร์ติโคสเตียรอยด์ สุขอนามัยช่องปากไม่ดี) ควรพิจารณาความจำเป็นในการตรวจทางทันตกรรมด้วยวิธีการทางทันตกรรมป้องกันที่เหมาะสม
ในระหว่างการรักษา ผู้ป่วยเหล่านี้ควรหลีกเลี่ยงขั้นตอนทางทันตกรรมที่รุกราน หากเป็นไปได้ ในผู้ป่วยที่เป็นโรคกระดูกพรุนของกรามและ / หรือกรามระหว่างการรักษาด้วยยาบิสฟอสโฟเนต การผ่าตัดทางทันตกรรมอาจทำให้อาการรุนแรงขึ้นได้ สำหรับผู้ป่วยที่ต้องผ่าตัดทางทันตกรรม ไม่มีข้อมูลใดที่สามารถแนะนำได้ว่าการหยุดการรักษาด้วยยาบิสฟอสโฟเนตจะช่วยลดความเสี่ยงของการเกิดกระดูกพรุนที่ขากรรไกรได้
การตัดสินทางคลินิกของแพทย์จะต้องเป็นแนวทางในโปรแกรมการจัดการของผู้ป่วยแต่ละราย โดยพิจารณาจากการประเมินรายบุคคลของอัตราส่วนความเสี่ยง/ผลประโยชน์
มีรายงานการเกิดโรคกระดูกพรุนของช่องหูชั้นนอกร่วมกับการใช้บิสฟอสโฟเนตซึ่งส่วนใหญ่เกี่ยวข้องกับการรักษาระยะยาว ปัจจัยเสี่ยงที่เป็นไปได้สำหรับภาวะกระดูกพรุนของช่องหูภายนอก ได้แก่ การใช้สเตียรอยด์และเคมีบำบัดและ/หรือปัจจัยเสี่ยงในท้องถิ่น เช่น เช่นการติดเชื้อหรือการบาดเจ็บ ควรพิจารณา Osteonecrosis ของช่องหูภายนอกในผู้ป่วยที่ได้รับ bisphosphonates ที่มีอาการหูรวมทั้งการติดเชื้อที่หูเรื้อรัง
กระดูกโคนขาหักผิดปกติ
มีรายงานการเกิดกระดูกหักแบบ subtrochanteric และ shaft fracture ที่ผิดปรกติ โดยส่วนใหญ่ในผู้ป่วยที่รักษาด้วย bisphosphonate therapy สำหรับโรคกระดูกพรุนในระยะยาว กระดูกหักตามขวางหรือเฉียงสั้นเหล่านี้สามารถเกิดขึ้นได้ทุกที่ในกระดูกโคนขาตั้งแต่ด้านล่างของ trochanter ที่น้อยกว่าไปจนถึงเหนือเส้น supracondylar กระดูกหักเหล่านี้ เกิดขึ้นเองตามธรรมชาติหรือหลังจากได้รับบาดเจ็บเพียงเล็กน้อยและผู้ป่วยบางรายมีอาการปวดที่ต้นขาหรือขาหนีบ ซึ่งมักเกี่ยวข้องกับการค้นพบภาพและหลักฐานทางรังสีวิทยาของการแตกหักจากความเครียด สัปดาห์หรือเดือนก่อนเกิดภาวะกระดูกหักจากความเครียด กระดูกหักมักเป็นแบบทวิภาคี ดังนั้นในผู้ป่วยที่ได้รับยาบิสฟอสโฟเนตซึ่งมีกระดูกต้นขาหักอย่างต่อเนื่อง ควรทำการตรวจกระดูกโคนขาด้านข้าง มีรายงานการรักษากระดูกหักเหล่านี้อย่างจำกัด ในผู้ป่วยที่สงสัยว่ามีกระดูกต้นขาหักผิดปรกติ ควรพิจารณาให้หยุดการรักษาด้วยยาบิสฟอสโฟเนตเพื่อรอการประเมินผู้ป่วยโดยพิจารณาจากความเสี่ยงของผลประโยชน์ส่วนบุคคล
ในระหว่างการรักษาด้วยยาบิสฟอสโฟเนต ผู้ป่วยควรได้รับคำแนะนำให้รายงานอาการปวดที่ต้นขา สะโพก หรือขาหนีบ และผู้ป่วยที่มีอาการดังกล่าวควรได้รับการประเมินหาการแตกหักของกระดูกโคนขาที่ไม่สมบูรณ์
ยานี้มีแลคโตส ผู้ป่วยที่มีปัญหาทางพันธุกรรมที่หายากของการแพ้กาแลคโตส การขาดแลคเตส หรือการดูดซึมกลูโคส-กาแลคโตส malabsorption ไม่ควรรับประทานยานี้
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
ไม่มีการศึกษาปฏิสัมพันธ์กับการรักษาอื่น ๆ อย่างไรก็ตาม ปฏิสัมพันธ์ที่เกี่ยวข้องทางคลินิกกับผลิตภัณฑ์ยาอื่น ๆ ยังไม่ได้รับการสังเกตในการทดลองทางคลินิก ในการศึกษาระยะที่ 3 ของ risedronate sodium ในการรักษาโรคกระดูกพรุน 33% และ 45% ตามลำดับของผู้ป่วยได้รับ acetylsalicylic กรดหรือยาต้านการอักเสบที่ไม่ใช่สเตียรอยด์ (NSAIDs) ในการศึกษาระยะที่ 3 โดยใช้การให้ยาทุกสัปดาห์ 57% และ 40% ของผู้ป่วยวัยหมดประจำเดือนได้รับกรดอะซิติลซาลิไซลิกหรือยาแก้อักเสบอื่น ๆ ที่ไม่ใช่สเตียรอยด์ตามลำดับ ในบรรดาผู้ป่วยที่ได้รับการรักษาด้วยกรดอะซิติลซาลิไซลิกหรือ NSAIDs เป็นประจำ (3 วันขึ้นไปต่อสัปดาห์) อุบัติการณ์ของเหตุการณ์ไม่พึงประสงค์ทางเดินอาหารส่วนบนในผู้ป่วยที่ได้รับการรักษาด้วย risedronate sodium มีความคล้ายคลึงกับในกลุ่มควบคุม
หากเห็นว่าเหมาะสม สามารถใช้ risedronate sodium ร่วมกับการบำบัดทดแทนฮอร์โมนเอสโตรเจนได้ (สำหรับผู้หญิงเท่านั้น)
การใช้ผลิตภัณฑ์ยาร่วมกันที่มีโพลีวาเลนท์ไพเพอร์ (เช่น แคลเซียม แมกนีเซียม เหล็ก และอะลูมิเนียม) ร่วมกันจะขัดขวางการดูดซึมของไรเซโดรเนตโซเดียม (ดูหัวข้อ 4.4)
โซเดียม Risedronate ไม่ได้รับการเผาผลาญอย่างเป็นระบบ ไม่กระตุ้นเอนไซม์ cytochrome P-450 และมีโปรตีนที่จับกับโปรตีนต่ำ
04.6 การตั้งครรภ์และให้นมบุตร
การตั้งครรภ์
มีข้อมูลไม่เพียงพอเกี่ยวกับการใช้ risedronate sodium ในหญิงตั้งครรภ์ การศึกษาในสัตว์แสดงความเป็นพิษต่อการเจริญพันธุ์ (ดูหัวข้อ 5.3) ยังไม่ทราบความเสี่ยงที่อาจเกิดขึ้นในสตรี
เวลาให้อาหาร
การศึกษาในสัตว์ทดลองระบุว่าไรซ์โดรเนตโซเดียมจำนวนเล็กน้อยผ่านเข้าสู่น้ำนมแม่
ไม่ควรให้ Risedronate sodium ในสตรีมีครรภ์หรือให้นมบุตร
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
ไม่มีผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
04.8 ผลกระทบที่ไม่พึงประสงค์
โซเดียม Risedronate ได้รับการศึกษาในการทดลองทางคลินิกระยะที่ 3 ซึ่งมีผู้ป่วยมากกว่า 15,000 ราย
ผลกระทบที่ไม่พึงประสงค์ส่วนใหญ่ที่พบในการทดลองทางคลินิกมีความรุนแรงน้อยหรือปานกลาง และโดยปกติไม่จำเป็นต้องหยุดการรักษา
ผลกระทบที่ไม่พึงประสงค์ที่เกิดขึ้นระหว่างการทดลองทางคลินิกระยะที่ 3 ในสตรีที่เป็นโรคกระดูกพรุนในวัยหมดประจำเดือนที่รักษานานถึง 36 เดือนด้วย risedronate sodium ในขนาด 5 มก. / วัน (n = 5020) หรือยาหลอก (n = 5048) และถือว่าเป็นไปได้หรืออาจจะ ที่เกี่ยวข้องกับ risedronate sodium แสดงโดยใช้คำจำกัดความต่อไปนี้ (อุบัติการณ์เทียบกับยาหลอกระบุไว้ในวงเล็บ):
พบบ่อยมาก (≥1 / 10); ทั่วไป (≥1 / 100;
ความผิดปกติของระบบประสาท:
ร่วมกัน: ปวดหัว (1.8% เทียบกับ 1.4%)
ความผิดปกติของดวงตา:
ผิดปกติ: ม่านตาอักเสบ *
ความผิดปกติของระบบทางเดินอาหาร:
ร่วมกัน: อาการท้องผูก (5.0% เทียบกับ 4.8%) อาการอาหารไม่ย่อย (4.5% เทียบกับ 4.1%) คลื่นไส้ (4.3% เทียบกับ 4.0%) ปวดท้อง (3.5% เทียบกับ 3.3%) ท้องร่วง (3.0% เทียบกับ 2.7 %)
พบไม่บ่อย: โรคกระเพาะ (0.9% เทียบกับ 0.7%), หลอดอาหารอักเสบ (0.9% เทียบกับ 0.9%), อาการกลืนลำบาก (0.4% เทียบกับ 0.2%), ลำไส้เล็กส่วนต้น (0.2% เทียบกับ 0.1%), แผลในหลอดอาหาร (0.2% เทียบกับ 0.2) %)
หายาก: glossitis (หลอดอาหารตีบ (
ความผิดปกติของกล้ามเนื้อและกระดูกและเนื้อเยื่อเกี่ยวพัน:
ร่วมกัน: ปวดกล้ามเนื้อและกระดูก (2.1% เทียบกับ 1.9%)
การตรวจวินิจฉัย:
หายาก: การทดสอบการทำงานของตับผิดปกติ *
* ไม่มีอุบัติการณ์ที่เกี่ยวข้องจากการทดลองทางคลินิกระยะที่ 3 ในโรคกระดูกพรุน ความถี่ขึ้นอยู่กับข้อมูลที่ไม่พึงประสงค์ / ห้องปฏิบัติการ / การทดสอบซ้ำจากการทดลองทางคลินิกครั้งก่อน
ในการศึกษาแบบหลายศูนย์แบบ double-blind และ multicenter เป็นเวลา 1 ปีซึ่งเปรียบเทียบ risedronate 5 มก. ต่อวัน (n = 480) และ risedronate sodium 35 มก. สัปดาห์ละครั้ง (n = 485) ในสตรีวัยหมดประจำเดือนที่เป็นโรคกระดูกพรุน ความทนทานโดยรวมและโปรไฟล์ความปลอดภัยมีความคล้ายคลึงกัน มีรายงานผลกระทบที่ไม่พึงประสงค์เพิ่มเติมต่อไปนี้ซึ่งผู้วิจัยพิจารณาว่าอาจหรืออาจเกี่ยวข้องกับยา (อุบัติการณ์สูงกว่าในกลุ่ม risedronate 35 มก. มากกว่าในกลุ่ม risedronate sodium 5 มก.): ความผิดปกติของระบบทางเดินอาหาร (1.6% เทียบกับ 1.0%) และความเจ็บปวด ( 1.2% เทียบกับ 0.8%)
ในการศึกษาแบบหลายศูนย์ในระยะเวลา 2 ปีที่ดำเนินการในผู้ชายที่เป็นโรคกระดูกพรุน ข้อมูลด้านความปลอดภัยและความสามารถในการทนต่อยาโดยรวมระหว่างกลุ่มที่ได้รับการบำบัดแบบแอคทีฟและกลุ่มยาหลอกมีความคล้ายคลึงกัน ผลข้างเคียงตรงกับที่พบในผู้หญิงก่อนหน้านี้
พารามิเตอร์ห้องปฏิบัติการในผู้ป่วยบางรายพบว่ามีการลดลงของแคลเซียมและฟอสเฟตในเลือดเล็กน้อยชั่วคราวและไม่มีอาการ
มีการรายงานผลกระทบที่ไม่พึงประสงค์เพิ่มเติมต่อไปนี้จากการตลาด: (ไม่ทราบความถี่):
ความผิดปกติของดวงตา:
ม่านตาอักเสบ, ม่านตาอักเสบ
ความผิดปกติของกล้ามเนื้อและกระดูกและเนื้อเยื่อเกี่ยวพัน:
osteonecrosis ของขากรรไกรล่างและ / หรือกระดูกขากรรไกร
ความผิดปกติของผิวหนังและเนื้อเยื่อใต้ผิวหนัง:
ปฏิกิริยาทางผิวหนังและภาวะภูมิไวเกิน เช่น แองจิโออีดีมา ผื่นทั่วๆ ไป ลมพิษและปฏิกิริยาทางผิวหนังที่เป็นเม็ดนูน และโรคหลอดเลือดอักเสบจากเม็ดโลหิตขาว รวมทั้งกรณีแยกอย่างร้ายแรงของ Stevens Johnson syndrome และ toxic epidermal necrolysis
ผมร่วง
ความผิดปกติของระบบภูมิคุ้มกัน:
ปฏิกิริยาตอบสนอง
ความผิดปกติของตับและท่อน้ำดี:
โรคตับที่รุนแรง ในกรณีส่วนใหญ่ที่รายงาน ผู้ป่วยยังได้รับการรักษาด้วยผลิตภัณฑ์อื่นๆ ที่ทราบว่าทำให้เกิดโรคตับ
มีการรายงานปฏิกิริยาต่อไปนี้ระหว่างประสบการณ์หลังการขาย
หายากมาก: osteonecrosis ของช่องหูภายนอก (อาการไม่พึงประสงค์สำหรับคลาส bisphosphonate)
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยซึ่งเกิดขึ้นหลังจากการอนุมัติผลิตภัณฑ์ยามีความสำคัญเนื่องจากช่วยให้สามารถตรวจสอบอัตราส่วนประโยชน์ / ความเสี่ยงของผลิตภัณฑ์ยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านการดูแลสุขภาพรายงานอาการไม่พึงประสงค์ที่น่าสงสัยผ่านทางสำนักงานยาแห่งอิตาลี ตามที่อยู่ http://www.agenziafarmaco.gov.it/it/responsabili
04.9 ใช้ยาเกินขนาด
ไม่มีข้อมูลเฉพาะเกี่ยวกับการรักษากรณีที่ให้ยาเกินขนาดด้วย risedronate sodium
ในกรณีที่ให้ยาเกินขนาดอาจทำให้แคลเซียมในเลือดลดลงได้ ผู้ป่วยบางรายอาจมีอาการและอาการแสดงของภาวะแคลเซียมในเลือดต่ำ
ควรให้นมหรือยาลดกรดที่มีแมกนีเซียม แคลเซียม หรืออะลูมิเนียมเพื่อยึดเกาะ risedronate และลดการดูดซึม ในกรณีของการใช้ยาเกินขนาด อาจพิจารณาการล้างกระเพาะเพื่อขจัด risedronate sodium ที่ไม่ถูกดูดซึม
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
หมวดหมู่ยารักษาโรค: Bisphosphonates, รหัส ATC M05BA07
Risedronate sodium เป็น pyridinyl bisphosphonate ซึ่งยึดติดกับไฮดรอกซีอะพาไทต์ของกระดูกและยับยั้งการสลายของกระดูกโดย osteoclasts การหมุนเวียนของกระดูกจะลดลงในขณะที่ยังคงรักษากิจกรรมของ osteoblastic และการทำให้เป็นแร่ของกระดูก ในการศึกษาพรีคลินิก โซเดียม Risedronate ได้แสดงฤทธิ์ต้านการสลายกระดูกและต้านการสลายซึ่งส่งผลให้มวลกระดูกเพิ่มขึ้นตามขนาดยาและความแข็งแรงทางชีวกลศาสตร์ของกระดูก กิจกรรมของ risedronate sodium ได้รับการยืนยันโดยการวัดค่าดัชนีทางชีวเคมีของการหมุนเวียนของกระดูกในระหว่างการศึกษาเภสัชพลศาสตร์และทางคลินิก ในการศึกษาของสตรีวัยหมดประจำเดือนพบว่าการลดลงของดัชนีทางชีวเคมีของการหมุนเวียนของกระดูกพบได้ภายในเดือนแรกและถึงระดับสูงสุด ภายใน 3-6 เดือน การลดลงของดัชนีเหล่านี้มีความคล้ายคลึงกับ Risedronate 35 มก. ต่อสัปดาห์ และ Risedronate 5 มก. / วัน หลังจาก 12 เดือน
ในการศึกษาในผู้ชายที่เป็นโรคกระดูกพรุน พบว่าดัชนีทางชีวเคมีของการหมุนเวียนของกระดูกลดลงในช่วง 3 เดือนและยังคงสังเกตได้เมื่อ 24 เดือน
การบำบัดและการป้องกันโรคกระดูกพรุนในวัยหมดประจำเดือน :
ปัจจัยเสี่ยงหลายประการ ได้แก่ มวลกระดูกต่ำ ความหนาแน่นของกระดูกต่ำ วัยหมดประจำเดือนก่อนกำหนด การสูบบุหรี่ และประวัติครอบครัวเป็นโรคกระดูกพรุนมีความเกี่ยวข้องกับโรคกระดูกพรุนในวัยหมดประจำเดือน ผลทางคลินิกของโรคกระดูกพรุนคืออุบัติการณ์ของกระดูกหักที่เพิ่มขึ้น ความเสี่ยงของการแตกหักเพิ่มขึ้นตามปัจจัยเสี่ยงที่เพิ่มขึ้น
จากผลกระทบต่อ BMD กระดูกสันหลังส่วนเอว พบว่า Risedronate 35 มก. / สัปดาห์ (n = 485) เทียบเท่ากับ Risedronate 5 มก. / วัน (n = 480) ในการศึกษาแบบหลายศูนย์แบบ double-blind ในระยะเวลาหนึ่งปี ในสตรีวัยหมดประจำเดือนที่เป็นโรคกระดูกพรุน
โปรแกรมการพัฒนาทางคลินิก risedronate sodium แบบใช้รายวันประเมินผลของ risedronate sodium ต่อความเสี่ยงของกระดูกสะโพกและกระดูกสันหลังหักและรวมถึงสตรีวัยหมดประจำเดือนทั้งช่วงต้นและปลายที่มีหรือไม่มีกระดูกหัก ประเมินปริมาณ 2 ขนาด , 5 และ 5 มก. ต่อวันและทั้งหมด รวมทั้งกลุ่มควบคุมที่ได้รับแคลเซียมและวิตามินดี (หากระดับพื้นฐานต่ำ) ความเสี่ยงแบบสัมบูรณ์และสัมพัทธ์ของกระดูกสันหลังหักใหม่และกระดูกสะโพกหักคำนวณโดยการใช้ "การวิเคราะห์"ถึงเวลาจัดงานครั้งแรก'.
• การศึกษาที่ควบคุมด้วยยาหลอกสองครั้ง (n = 3,661) ที่ลงทะเบียนเรียนในสตรีวัยหมดประจำเดือนที่อายุน้อยกว่า 85 ปีที่มีอาการกระดูกสันหลังหักที่พื้นฐาน Risedronate sodium 5 มก. ต่อวันเป็นเวลา 3 ปีส่งผลให้ความเสี่ยงของกระดูกสันหลังหักใหม่ลดลงเมื่อเทียบกับกลุ่มควบคุม กลุ่ม. ในสตรีที่มีกระดูกสันหลังหักอย่างน้อย 2 ชิ้น ความเสี่ยงสัมพันธ์ของการแตกหักของกระดูกหักใหม่ลดลง 49% (อุบัติการณ์ของการแตกหักของกระดูกสันหลังใหม่ด้วย Risedronate sodium คือ 18.1% และด้วยยาหลอก 29%) ในผู้ที่มีกระดูกหักอย่างน้อย 1 ครั้ง การลดลงนี้คือ 41% (อุบัติการณ์ของการแตกหักของกระดูกสันหลังใหม่ด้วย risedronate เท่ากับ 11.3% ในขณะที่ได้รับยาหลอกคือ 16.3%) ผลการรักษาสังเกตได้ตั้งแต่ช่วงสิ้นปีแรกของการรักษา นอกจากนี้ ยังแสดงให้เห็นประโยชน์ในสตรีที่กระดูกหักหลายครั้งที่การตรวจวัดพื้นฐาน Risedronate sodium 5 มก. ต่อวันช่วยลดการสูญเสียประจำปีเมื่อเทียบกับกลุ่มควบคุม
• การศึกษาที่ควบคุมด้วยยาหลอกเพิ่มเติม 2 ฉบับที่ลงทะเบียนในสตรีวัยหมดประจำเดือนที่มีอายุมากกว่า 70 ปีที่มีหรือไม่มีกระดูกหักที่การตรวจวัดพื้นฐาน สตรีอายุ 70-79 ปีที่มีกระดูกต้นขา BMD T-score ได้รับการลงทะเบียนสำหรับการแตกหักของกระดูกสะโพกหรือโดยพิจารณาจากความหนาแน่นของแร่ธาตุที่ลดลง คอต้นขา ตามสถิติ ประสิทธิภาพของ risedronate sodium เทียบกับ placebo ทำได้ก็ต่อเมื่อทั้งสองกลุ่มที่ได้รับยา 2.5 และ 5 มก. รวมกัน ผลลัพธ์ต่อไปนี้อ้างอิงจากการวิเคราะห์หลังโพสต์ของผู้ป่วยกลุ่มย่อยเท่านั้น โดยเลือกจากกรณีศึกษาทางคลินิกหรือตามคำจำกัดความปัจจุบันของ โรคกระดูกพรุน:
• ในกลุ่มย่อยของผู้ป่วยที่มี BMD T-score ที่คอกระดูกต้นขา ≤-2.5 SD (NHANES III) และมีการแตกหักของกระดูกสันหลังที่เส้นพื้นฐานอย่างน้อย 1 อัน การใช้ Risedronate sodium เป็นเวลา 3 ปีจะช่วยลดความเสี่ยงของการเกิดกระดูกสะโพกหัก กระดูกสะโพกหักใน 46% ของผู้ป่วย เมื่อเทียบกับกลุ่มควบคุม (อุบัติการณ์ของกระดูกสะโพกหักในกลุ่มโซเดียมที่เพิ่มขึ้น 2.5 และ 5 มก. เท่ากับ 3.8%, 7.4% ในกลุ่มยาหลอก)
• ข้อมูลชี้ให้เห็นว่าการป้องกันที่จำกัดมากขึ้นในผู้ป่วยสูงอายุ (≥80 ปี) นี่อาจเป็นผลมาจากความสำคัญที่เพิ่มขึ้นของปัจจัยเสี่ยงที่ไม่ใช่โครงกระดูกสำหรับกระดูกสะโพกหักในช่วงหลายปีที่ผ่านมา ในการศึกษาเหล่านี้ การวิเคราะห์จุดยุติทุติยภูมิชี้ให้เห็นถึงความเสี่ยงที่ลดลงของการแตกหักของกระดูกสันหลังใหม่ในผู้ป่วยที่มี BMD ที่คอต้นขาลดลงโดยไม่มีการแตกหักของกระดูกสันหลัง และในผู้ป่วยที่มี BMD ที่คอกระดูกต้นขาลดลงที่มีหรือไม่มีกระดูกหัก
• Risedronate sodium 5 มก. ต่อวันเป็นเวลา 3 ปี เพิ่มความหนาแน่นของกระดูก (BMD) ของกระดูกสันหลังส่วนเอว คอตีบ trochanter และข้อมือ เมื่อเทียบกับกลุ่มควบคุมและป้องกันการสูญเสียกระดูกในส่วนที่สามของวิทยุ
• การลดลงอย่างรวดเร็วของผลกดขี่ของ risedronate sodium ต่ออัตราการหมุนเวียนของกระดูกถูกสังเกตพบใน "ปีหลังการหยุดการรักษาหลังจากสามปีของการรักษาด้วย risedronate sodium 5 มก. ต่อวัน"
• การตรวจชิ้นเนื้อในสตรีวัยหมดประจำเดือนที่รักษาด้วย risedronate sodium 5 มก. ต่อวันเป็นเวลา 2-3 ปี ยืนยันว่าการหมุนเวียนของกระดูกลดลงในระดับปานกลาง เนื้อเยื่อกระดูกระหว่างการรักษาด้วย risedronate sodium พบว่ามีโครงสร้าง lamellar ปกติและอัตราการเกิดแร่ธาตุของกระดูก ข้อมูลเหล่านี้ร่วมกับอุบัติการณ์ที่ลดลงของกระดูกพรุนในผู้หญิงที่เป็นโรคกระดูกพรุน ดูเหมือนว่าจะยืนยันได้ว่าไม่มีผลที่เป็นอันตรายต่อคุณภาพของกระดูก
การวัดด้วยการส่องกล้องในผู้ป่วยหลายราย ทั้งในกลุ่มควบคุม risedronate sodium และในกลุ่มควบคุม ที่มีความผิดปกติของระบบทางเดินอาหารในระดับปานกลางถึงรุนแรง ไม่พบแผลที่หลอดอาหาร กระเพาะอาหาร หรือลำไส้เล็กส่วนต้นที่เกี่ยวข้องกับการรักษา แม้ว่ากรณีของ duodenitis จะพบได้ไม่บ่อยนัก ในกลุ่มไรโดรเนตโซเดียม
การรักษาโรคกระดูกพรุนในผู้ชาย
Risedronate sodium 35 มก. สัปดาห์ละครั้งแสดงให้เห็นว่ามีประสิทธิภาพในผู้ชายที่เป็นโรคกระดูกพรุน (อายุ 36 ถึง 84 ปี) ในการศึกษา 2 ปีแบบ double-blind ที่ได้รับยาหลอกในผู้ป่วย 284 ราย (risedronate sodium 35 mg n = 191) ผู้ป่วยทุกรายได้รับการเสริมแคลเซียมและวิตามินดี
การเพิ่มขึ้นของ BMD เกิดขึ้นได้ภายใน 6 เดือนหลังจากเริ่มการรักษาด้วย risedronate sodium Risedronate sodium 35 มก. สัปดาห์ละครั้งทำให้ BMD เฉลี่ยของกระดูกสันหลังส่วนเอว คอต้นขา trochanter และสะโพกเพิ่มขึ้นเมื่อเทียบกับยาหลอกหลังการรักษา 2 ปี ประสิทธิภาพในการต้านการแตกหักไม่ได้แสดงให้เห็นในการศึกษานี้
ผลกระทบต่อกระดูก (BMD ที่เพิ่มขึ้นและเครื่องหมายทางชีวเคมีที่ลดลงของการหมุนเวียนของกระดูก) ของ risedronate sodium มีความคล้ายคลึงกันในผู้ชายและผู้หญิง
ประชากรเด็ก
ความปลอดภัยและประสิทธิภาพของ risedronate sodium กำลังได้รับการประเมินในการศึกษาต่อเนื่องในผู้ป่วยเด็กที่มีอายุตั้งแต่ 4 ปีถึงน้อยกว่า 16 ปีที่มีความไม่สมบูรณ์ของการสร้างกระดูก หลังจากเสร็จสิ้นขั้นตอนการควบคุมด้วยยาหลอกแบบ randomized double-blind ซึ่งกินเวลานานหนึ่งปี การเพิ่มขึ้นของ BMD ของกระดูกสันหลังส่วนเอวมีนัยสำคัญทางสถิติแสดงให้เห็นในกลุ่ม Risedronate เทียบกับกลุ่มยาหลอก อย่างไรก็ตาม พบการแตกหักของกระดูกสันหลังส่วนกระดูกสันหลังชนิดใหม่อย่างน้อย 1 ครั้ง (ประเมินด้วยรังสี) ในกลุ่ม Risedronate เมื่อเทียบกับยาหลอก ผลลัพธ์ไม่สนับสนุนการใช้ risedronate sodium ในผู้ป่วยเด็กที่มีภาวะกระดูกพรุน
05.2 คุณสมบัติทางเภสัชจลนศาสตร์
การดูดซึม
การดูดซึมของขนาดยาทางปากค่อนข้างเร็ว (Tmax ~ 1 ชั่วโมง) และเป็นอิสระจากขนาดยาที่ศึกษา (การศึกษาในขนาดยาครั้งเดียว 2.5 ถึง 30 มก. การศึกษาขนาดยาหลายครั้ง 2.5 ถึง 5 มก. / วันและสูงถึง 50 มก. / สัปดาห์) การดูดซึมทางปากของยาเม็ดเฉลี่ย 0.63% และลดลงเมื่อให้ risedronate sodium กับอาหาร การดูดซึมมีความคล้ายคลึงกันในผู้ชายและผู้หญิง
การกระจาย: ปริมาณการกระจายของสภาวะคงตัวเฉลี่ยในมนุษย์คือ 6.3 ลิตรต่อกิโลกรัม
เศษส่วนของยาที่จับกับโปรตีนในพลาสมาอยู่ที่ประมาณ 24%
การเปลี่ยนแปลงทางชีวภาพ:
ไม่มีหลักฐานว่าโซเดียมไรโดรเนตถูกเผาผลาญอย่างเป็นระบบ
การกำจัด
ประมาณครึ่งหนึ่งของปริมาณที่ดูดซึมจะถูกกำจัดในปัสสาวะภายใน 24 ชั่วโมง ในขณะที่ 85% ของขนาดยาทางหลอดเลือดดำจะถูกกำจัดในปัสสาวะหลังจาก 28 วัน ค่าล้างไตเฉลี่ย 105 มล. / นาที และการกวาดล้างทั้งหมด 122 มล. / นาที: ความแตกต่างน่าจะมาจากการกวาดล้างเนื่องจากการดูดซึมไปยังกระดูก การกวาดล้างของไตไม่ขึ้นกับความเข้มข้น และมีความสัมพันธ์เชิงเส้นระหว่างการกวาดล้างของไตและการกวาดล้างของครีเอตินีน Unabsorbed risedronate sodium จะถูกกำจัดออกทางอุจจาระโดยไม่เปลี่ยนแปลง หลังจากการบริหารช่องปาก กราฟแสดงความเข้มข้น-เวลาจะแสดงเป็น 3 ขั้นตอนการกำจัดที่มีครึ่งชีวิตขั้ว 480 ชั่วโมง
ประชากรพิเศษ
ผู้ป่วยสูงอายุ:
ไม่จำเป็นต้องปรับขนาดยา
ผู้ป่วยที่รักษาด้วยกรดอะซิติลซาลิไซลิก / NSAID:
ในผู้ป่วยที่รักษาอย่างสม่ำเสมอ (อย่างน้อย 3 วันต่อสัปดาห์) ด้วยกรดอะซิติลซาลิไซลิกหรือ NSAIDs อุบัติการณ์ของเหตุการณ์ไม่พึงประสงค์ในทางเดินอาหารส่วนบนใน Risedronate sodium มีความคล้ายคลึงกับในกลุ่มควบคุม
05.3 ข้อมูลความปลอดภัยพรีคลินิก
การศึกษาทางพิษวิทยาในหนูและสุนัขโดยหลักจากการเพิ่มขึ้นของเอนไซม์ที่มีการเปลี่ยนแปลงทางเนื้อเยื่อวิทยาในหนู ไม่ทราบความเกี่ยวข้องทางคลินิกของการสังเกตเหล่านี้ ความเป็นพิษของลูกอัณฑะปรากฏในหนูและสุนัขเมื่อได้รับสัมผัสซึ่งเกินจากการสัมผัสทางการรักษาในมนุษย์ ในสัตว์ฟันแทะมักพบการระคายเคืองที่ขึ้นกับขนาดยาของทางเดินหายใจส่วนบน มีรายงานผลกระทบที่คล้ายกันกับ bisphosphonates อื่น ๆ ผลกระทบต่อระบบทางเดินหายใจส่วนล่างได้รับการสังเกตในการศึกษาหนูในระยะยาว อย่างไรก็ตาม ความเกี่ยวข้องทางคลินิกของการค้นพบนี้ไม่ชัดเจน ในการศึกษาความเป็นพิษต่อการเจริญพันธุ์ในระยะใกล้กับการสัมผัสทางคลินิก การเปลี่ยนแปลงของการสร้างกระดูกที่ระดับกระดูกสันอกและ/หรือกะโหลกพบในทารกในครรภ์ของหนูที่ได้รับการรักษาและแคลเซียมในเลือดต่ำและการตายในสตรีที่ได้รับการรักษาที่คลอดบุตร ไม่มีหลักฐานของการก่อการก่ออวัยวะภายในขณะคลอด . ปริมาณ 3.2 มก. / กก. / วันในหนูและ 10 มก. / กก. / วันในกระต่ายแม้ว่าข้อมูลจะมีอยู่ในกระต่ายจำนวน จำกัด เท่านั้น ความเป็นพิษของมารดาทำให้ไม่สามารถศึกษาปริมาณที่สูงขึ้นได้ เกี่ยวกับ genotoxicity และ carcinogenesis ไม่ได้แสดงให้เห็น ความเสี่ยงเฉพาะสำหรับมนุษย์
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
แกนกลาง: ไมโครคริสตัลลีน เซลลูโลส, ครอสโพวิโดน, แมกนีเซียมสเตียเรต, แลคโตสโมโนไฮเดรต,
การเคลือบผิว: เหล็กออกไซด์สีแดง, เหล็กออกไซด์สีเหลือง, ซิลิกาคอลลอยด์ปราศจากน้ำ, ไททาเนียมไดออกไซด์, macrogol 400, macrogol 8000, hypromellose, ไฮดรอกซีโพรพิลเซลลูโลส
06.2 ความเข้ากันไม่ได้
ไม่เกี่ยวข้อง
06.3 ระยะเวลาที่มีผลบังคับใช้
3 ปี
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
ยานี้ไม่ต้องการเงื่อนไขการจัดเก็บพิเศษใด ๆ
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
PVC ทึบแสง / PVDC / ตุ่มอลูมิเนียมในกล่องกระดาษแข็ง
แพ็ค: 4 เม็ด
06.6 คำแนะนำในการใช้งานและการจัดการ
ไม่มีคำแนะนำพิเศษ
07.0 ผู้ทรงอำนาจการตลาด
FENIX ฟาร์มา SOC. สหกรณ์
ผ่าน Ercolano Salvi n. 18
00143 โรม
อิตาลี
08.0 หมายเลขอนุญาตการตลาด
เอไอซี น. 040044012 "เม็ดเคลือบฟิล์ม MEDEOROS 35 มก. - 4 เม็ด"
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
วันที่ให้สิทธิ์ครั้งแรก: 20 มิถุนายน 2011
วันที่ต่ออายุล่าสุด:
10.0 วันที่แก้ไขข้อความ
กุมภาพันธ์ 2016