สารออกฤทธิ์: Prasugrel
เม็ดเคลือบฟิล์มที่มีประสิทธิภาพ 10 มก.
เม็ดเคลือบฟิล์ม 5 มก. ที่มีประสิทธิภาพ
เหตุใดจึงใช้ Efient? มีไว้เพื่ออะไร?
Efient ซึ่งมีสารออกฤทธิ์ prasugrel อยู่ในกลุ่มยาที่เรียกว่ายาต้านเกล็ดเลือด เกล็ดเลือดเป็นเซลล์ขนาดเล็กมากที่ไหลเวียนอยู่ในเลือด เมื่อหลอดเลือดเสียหาย เช่น ถ้าถูกตัด เกล็ดเลือดจะจับตัวเป็นก้อนทำให้เกิดลิ่มเลือด (thrombus) ดังนั้นเกล็ดเลือดจึงจำเป็นต่อการช่วยหยุดเลือด ถ้าเกิดลิ่มเลือดอุดตันในเส้นเลือดที่แข็งตัว เช่น หลอดเลือดแดง อาจเกิดอันตรายได้มาก เพราะสามารถปิดกั้นทางเดินของเลือด ทำให้หัวใจวาย (กล้ามเนื้อหัวใจตาย) โรคหลอดเลือดสมอง หรือเสียชีวิตได้ การอุดตันในหลอดเลือดแดงที่นำเลือดไปเลี้ยงหัวใจยังช่วยลดการไหลเวียนของเลือดไปยังหัวใจ ทำให้เกิดโรคหลอดเลือดหัวใจตีบที่ไม่คงที่ (เจ็บหน้าอกอย่างรุนแรง)
Efient ยับยั้งการรวมตัวของเกล็ดเลือด ดังนั้นจึงช่วยลดโอกาสการเกิดลิ่มเลือด
Efient ถูกกำหนดให้คุณเพราะก่อนหน้านี้คุณเคยมีอาการหัวใจวายหรือโรคหลอดเลือดหัวใจตีบที่ไม่เสถียรและได้รับการรักษาด้วยขั้นตอนในการเปิดหลอดเลือดหัวใจตีบตัน คุณอาจเคยใส่ขดลวดอย่างน้อย 1 อันในหลอดเลือดแดงที่อุดตันหรือตีบเพื่อฟื้นฟูการไหลเวียนของเลือด Efient ช่วยลดโอกาสที่คุณจะมีอาการหัวใจวายหรือโรคหลอดเลือดสมองหรือเสียชีวิตจากเหตุการณ์ atherothrombotic เหล่านี้ แพทย์ของคุณจะสั่งกรดอะซิติลซาลิไซลิก ( เช่น แอสไพริน) ยาต้านเกล็ดเลือดอีกตัวหนึ่ง
ข้อห้ามเมื่อไม่ควรใช้ Efient
อย่าเอาอีไฟท์
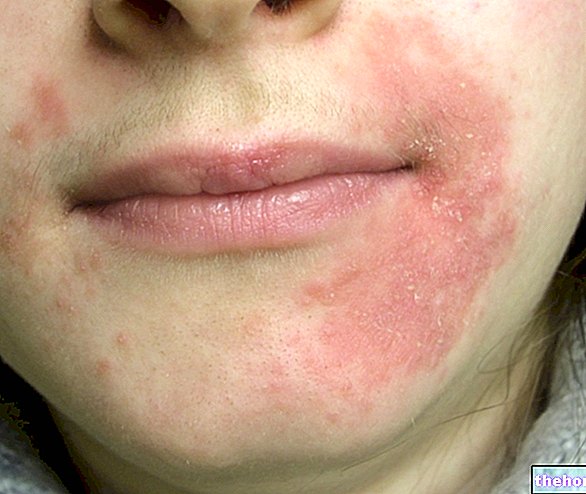
- หากคุณแพ้ (แพ้ง่าย) ต่อ prasugrel หรือส่วนผสมอื่นๆ ของ Efient อาการแพ้สามารถรับรู้ได้เนื่องจากทำให้เกิดผื่น คัน ใบหน้าบวม ริมฝีปากบวม หรือหายใจมีเสียงหวีด หากมีอาการเหล่านี้เกิดขึ้น ควรแจ้งให้แพทย์ทราบทันที
- หากคุณมีอาการป่วยที่ทำให้คุณมีเลือดออก เช่น มีเลือดออกในกระเพาะอาหารหรือในลำไส้
- หากคุณเคยเป็นโรคหลอดเลือดสมองตีบหรือการโจมตีขาดเลือดชั่วคราว (TIA)
- หากคุณมีโรคตับรุนแรง
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนรับประทาน Efient
หากเกิดสถานการณ์ใด ๆ ที่กล่าวถึงด้านล่าง แจ้งให้แพทย์ทราบก่อนใช้ยา Efient:
- หากคุณมีความเสี่ยงที่จะมีเลือดออกมากขึ้น เช่น:
- อายุ 75 ปีขึ้นไป. แพทย์จะสั่งจ่ายยาวันละ 5 มก. เนื่องจากมีความเสี่ยงที่จะมีเลือดออกมากขึ้นในผู้ป่วยที่มีอายุมากกว่า 75 ปี
- การบาดเจ็บรุนแรงล่าสุด
- การผ่าตัดล่าสุด (รวมถึงขั้นตอนทางทันตกรรมบางอย่าง)
- เลือดออกในกระเพาะอาหารหรือลำไส้เมื่อเร็ว ๆ นี้หรือซ้ำ (เช่น แผลในกระเพาะอาหารหรือติ่งเนื้อลำไส้ใหญ่)
- น้ำหนักตัวน้อยกว่า 60 กก. แพทย์ของคุณจะกำหนดให้ยา Efient 5 มก. ต่อวันหากน้ำหนักของคุณน้อยกว่า 60 กก. - โรคตับหรือไตปานกลาง
- หากคุณกำลังใช้ยาบางชนิด (ดู "การรับประทานยาที่มีประสิทธิภาพร่วมกับยาอื่น")
- หากคุณมีกำหนดจะเข้ารับการผ่าตัด (รวมถึงการทำหัตถการบางอย่าง) ภายในเจ็ดวันข้างหน้า แพทย์ของคุณอาจแนะนำให้คุณหยุดใช้ Efient ชั่วคราวเนื่องจากมีความเสี่ยงที่จะมีเลือดออกมากขึ้น
- หากคุณเคยมีอาการแพ้ (แพ้) ต่อ clopidogrel หรือยาต้านเกล็ดเลือดอื่น ๆ โปรดแจ้งให้แพทย์ทราบก่อนเริ่มการรักษาด้วย Efient หากคุณใช้ยาอีไฟท์และพบอาการแพ้ซึ่งอาจเรียกได้ว่าเป็น "ผื่น คัน หน้าบวม ริมฝีปากบวม หรือหายใจลำบาก คุณควรแจ้งให้แพทย์ทราบทันที
ในขณะที่รับ Efient:
บอกแพทย์ของคุณทันทีหากคุณมีอาการป่วยที่เรียกว่า Thrombotic Thrombocytopenic Purpura (PTT) ซึ่งรวมถึงไข้และรอยฟกช้ำใต้ผิวหนังซึ่งอาจปรากฏเป็นจุดสีแดงเล็ก ๆ โดยมีหรือไม่มีอาการอ่อนเพลีย สับสน เปลี่ยนสี ผิวหรือตาเหลือง (ดีซ่าน) (ดูหัวข้อ 4 "ผลข้างเคียงที่เป็นไปได้")
เด็กและวัยรุ่น
Efient ไม่เหมาะสำหรับเด็กและวัยรุ่นที่มีอายุต่ำกว่า 18 ปี
ปฏิกิริยา ยาหรืออาหารชนิดใดที่สามารถเปลี่ยนผลของเอไฟน์ได้
แจ้งให้แพทย์ทราบหากคุณกำลังรับประทาน เพิ่งได้รับ หรืออาจกำลังใช้ยาอื่น ๆ รวมถึงยาที่ได้รับโดยไม่มีใบสั่งยา อาหารเสริม และยาสมุนไพร เป็นสิ่งสำคัญอย่างยิ่งที่คุณต้องแจ้งให้แพทย์ทราบหากคุณกำลังรับการรักษาด้วย clopidogrel (ยาต้านเกล็ดเลือด) วาร์ฟาริน (ยาต้านการแข็งตัวของเลือด) หรือด้วย "ยาต้านการอักเสบที่ไม่ใช่สเตียรอยด์" เพื่อบรรเทาอาการปวดและลดไข้ (เช่น ไอบูโพรเฟน นาพรอกเซน, อีโทรอริกซิบ ). เมื่อให้ร่วมกับ Efient ยาเหล่านี้อาจเพิ่มความเสี่ยงต่อการตกเลือด
ใช้ยาอื่นในขณะที่ใช้ Efient หากแพทย์ของคุณบอกว่าคุณทำได้
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
การตั้งครรภ์และให้นมบุตร
บอกแพทย์หากคุณกำลังตั้งครรภ์หรือวางแผนที่จะตั้งครรภ์ในขณะที่คุณกำลังใช้ Efient คุณควรใช้ Efient หลังจากพูดคุยเกี่ยวกับประโยชน์ที่อาจเกิดขึ้นและความเสี่ยงที่อาจเกิดขึ้นกับทารกในครรภ์ของคุณกับแพทย์ของคุณเท่านั้น
หากคุณกำลังให้นมบุตร ปรึกษาแพทย์หรือเภสัชกรเพื่อขอคำแนะนำก่อนรับประทานยาใดๆ
การขับรถและการใช้เครื่องจักร
Efient ไม่น่าจะส่งผลต่อความสามารถในการขับขี่หรือใช้เครื่องจักร
Efient มีแลคโตส
หากคุณได้รับแจ้งจากแพทย์ว่าคุณมี "การแพ้น้ำตาลบางชนิด โปรดปรึกษาแพทย์ก่อนใช้ยานี้
ปริมาณ วิธีการ และระยะเวลาในการบริหาร วิธีใช้ Efient: Posology
ใช้ Efient ตามที่แพทย์ของคุณบอกคุณเสมอ หากมีข้อสงสัย ควรปรึกษาแพทย์หรือเภสัชกร
ปริมาณปกติของ Efient คือ 10 มก. ต่อวัน การรักษาจะเริ่มด้วยขนาดเดียว 60 มก. หากน้ำหนักตัวของคุณน้อยกว่า 60 กก. หรือหากคุณอายุมากกว่า 75 ปี ให้ใช้ยา Efient 5 มก. ต่อวัน
แพทย์ของคุณจะบอกให้คุณทานกรดอะซิติลซาลิไซลิกด้วย - เขาจะบอกคุณถึงขนาดยาที่แน่นอนที่จะต้องใช้ (โดยปกติระหว่าง 75 มก. ถึง 325 มก. ต่อวัน)
คุณสามารถทาน Efient โดยมีหรือไม่มีอาหารก็ได้ ใช้ Efient ในเวลาเดียวกันในแต่ละวัน อย่าบดขยี้หรือทำลายแท็บเล็ต
เป็นสิ่งสำคัญที่คุณจะต้องแจ้งให้แพทย์ เภสัชกร และทันตแพทย์ทราบว่าคุณกำลังใช้ยาอีไฟท์
ยาเกินขนาดจะทำอย่างไรถ้าคุณได้รับ Efient มากเกินไป
หากคุณใช้ Efient มากกว่าที่คุณควร
ติดต่อแพทย์ของคุณหรือโรงพยาบาลที่ใกล้ที่สุดทันทีเนื่องจากมีความเสี่ยงที่จะมีเลือดออกมากเกินไป แสดง Efient ของคุณแพ็คของคุณ
หากคุณลืมทานเอไฟท์
หากคุณลืมรับประทานยา ให้รับประทานหนึ่งเม็ดทันทีที่สังเกตเห็น หากคุณลืมรับประทานยาทั้งวัน ให้ทานยาอีไฟท์ตามปกติในวันรุ่งขึ้น อย่าใช้สองโดสในวันเดียวกัน สำหรับแพ็คขนาด 14, 28, 56, 84 และ 98 เม็ด คุณสามารถตรวจสอบวันที่คุณกินแท็บเล็ต Efient ล่าสุดโดยตรวจสอบปฏิทินที่พิมพ์บนตุ่ม
หากคุณหยุดทานเอไฟน์
อย่าหยุดใช้ Efient โดยไม่ได้ปรึกษาแพทย์ หากคุณหยุดใช้ Efient เร็วเกินไปความเสี่ยงของภาวะกล้ามเนื้อหัวใจตายอาจสูงขึ้น
หากคุณมีคำถามเพิ่มเติมเกี่ยวกับการใช้ยานี้ ให้สอบถามแพทย์หรือเภสัชกรของคุณ
ผลข้างเคียง ผลข้างเคียงของ Efient คืออะไร?
เช่นเดียวกับยาทั้งหมด Efient สามารถทำให้เกิดผลข้างเคียงได้แม้ว่าจะไม่ใช่ทุกคนที่ได้รับก็ตาม
คุณควรติดต่อแพทย์ทันทีหากสังเกตเห็นผลข้างเคียงใด ๆ ต่อไปนี้:
- ง่วงนอนกะทันหันหรืออ่อนแรงที่แขน ขา หรือใบหน้า โดยเฉพาะหากจำกัดอยู่เพียงซีกเดียวของร่างกาย
- สับสนกะทันหัน พูดลำบาก หรือเข้าใจสิ่งที่คนอื่นพูด
- มีปัญหาในการเดินกะทันหันหรือสูญเสียการทรงตัวหรือการประสานงาน
- อาการวิงเวียนศีรษะกะทันหันหรือปวดศีรษะรุนแรงกะทันหันโดยไม่ทราบสาเหตุ
จากทั้งหมดที่กล่าวมาอาจเป็นสัญญาณของโรคหลอดเลือดสมองได้ โรคหลอดเลือดสมองเป็นผลข้างเคียงที่ไม่ธรรมดาของ Efient ในผู้ป่วยที่ไม่เคยเป็นโรคหลอดเลือดสมองหรือขาดเลือดขาดเลือดชั่วคราว (TIA)
ติดต่อแพทย์ของคุณทันทีหากคุณสังเกตเห็นผลข้างเคียงใด ๆ ต่อไปนี้:
- ไข้และรอยฟกช้ำใต้ผิวหนังซึ่งอาจปรากฏเป็นจุดสีแดงเล็ก ๆ โดยไม่ทราบสาเหตุ มีอาการเหนื่อยล้า สับสน ผิวหรือตาเป็นสีเหลือง (โรคดีซ่าน) (ดูหัวข้อที่ 2 "ก่อนที่คุณจะทำการทดลอง")
- อาการ "ผื่นที่ผิวหนัง อาการคัน หรือบวมที่ใบหน้า ริมฝีปาก/ลิ้น หรือหายใจมีเสียงหวีด ทั้งหมดนี้อาจเป็นสัญญาณของอาการแพ้อย่างรุนแรง (ดูหัวข้อที่ 2" สิ่งที่คุณต้องรู้ก่อนใช้ยาอีเฟียนท์ ")
คุณควรติดต่อแพทย์ทันทีหากสังเกตเห็นผลข้างเคียงใด ๆ ต่อไปนี้:
- เลือดในปัสสาวะ
- มีเลือดออกทางทวารหนัก อุจจาระเป็นเลือดหรืออุจจาระสีดำ
- เลือดออกที่ควบคุมไม่ได้ เช่น จากบาดแผล
จากทั้งหมดที่กล่าวมาอาจเป็นสัญญาณของการมีเลือดออก ซึ่งเป็นผลข้างเคียงที่พบบ่อยที่สุดกับ Efient แม้ว่าเลือดออกรุนแรงอาจไม่ใช่เรื่องปกติ แต่อาจเป็นอันตรายถึงชีวิตได้
ผลข้างเคียงที่พบบ่อย (อาจส่งผลกระทบถึง 1 ใน 10 คน)
- เลือดออกในกระเพาะอาหารหรือลำไส้
- มีเลือดออกจากจุดทิ่มเข็ม
- เลือดกำเดาไหล
- ผื่นที่ผิวหนัง
- รอยฟกช้ำเล็ก ๆ บนผิวหนัง (ช้ำ)
- เลือดในปัสสาวะ
- ห้อ (เลือดออกใต้ผิวหนังบริเวณที่ฉีดหรือเข้าไปในกล้ามเนื้อทำให้เกิดอาการบวม)
- ฮีโมโกลบินต่ำหรือจำนวนเม็ดเลือดแดงต่ำ (โรคโลหิตจาง)
- รอยฟกช้ำ
ผลข้างเคียงที่ไม่ธรรมดา (อาจส่งผลกระทบถึง 1 ใน 100 คน)
- อาการแพ้ (ผื่น, คัน, บวมที่ริมฝีปาก / ลิ้นหรือหายใจดังเสียงฮืด ๆ)
- เลือดออกเองจากตา ทวารหนัก เหงือก หรือช่องท้องรอบอวัยวะภายใน
- เลือดออกหลังการผ่าตัด
- ไอเป็นเลือด
- เลือดในอุจจาระ
ผลข้างเคียงที่หายาก (อาจส่งผลกระทบมากถึง 1 ใน 1,000 คน)
- เกล็ดเลือดในเลือดต่ำ
- เลือดใต้ผิวหนัง (เลือดออกใต้ผิวหนังทำให้เกิดอาการบวม)
การรายงานผลข้างเคียง
หากมีผลข้างเคียงที่ร้ายแรง หรือหากคุณสังเกตเห็นผลข้างเคียงใดๆ ที่ไม่ได้ระบุไว้ในเอกสารฉบับนี้ โปรดแจ้งให้แพทย์หรือเภสัชกรทราบ คุณยังสามารถรายงานผลข้างเคียงได้โดยตรงผ่านระบบการรายงานระดับประเทศที่ระบุไว้ในภาคผนวก 5 โดยการรายงานผลข้างเคียง คุณสามารถช่วยให้ข้อมูลเพิ่มเติมเกี่ยวกับความปลอดภัยของยานี้ได้
การหมดอายุและการเก็บรักษา
เก็บ Efient ให้พ้นสายตาและมือเด็ก
อย่าใช้ Efient หลังจากวันหมดอายุซึ่งระบุไว้บนตุ่มและกล่องหลังจาก EXP วันหมดอายุหมายถึงวันสุดท้ายของเดือน
เก็บในบรรจุภัณฑ์เดิมเพื่อป้องกันอากาศและความชื้น
ยาไม่ควรทิ้งทางน้ำเสียหรือของเสียในครัวเรือน ถามเภสัชกรว่าจะทิ้งยาที่คุณไม่ใช้แล้วทิ้งอย่างไร ซึ่งจะช่วยปกป้องสิ่งแวดล้อม
สิ่งที่ Efient ประกอบด้วย
- สารออกฤทธิ์คือพราซูเกรล
มีประสิทธิภาพ 10 มก.: แต่ละเม็ดประกอบด้วย prasugrel 10 มก. (ในรูปของไฮโดรคลอไรด์)
มีประสิทธิภาพ 5 มก.: แต่ละเม็ดมี prasugrel 5 มก. (ในรูปของไฮโดรคลอไรด์)
- ส่วนผสมอื่นๆ ได้แก่ ไมโครคริสตัลลีน เซลลูโลส แมนนิทอล (E421) ครอสคาร์เมลโลสโซเดียม ไฮโปรเมลโลส (E464) แมกนีเซียมสเตียเรต แลคโตสโมโนไฮเดรต ไททาเนียมไดออกไซด์ (E171) ไตรอะซิติน (E1518) เหล็กออกไซด์สีแดง (เฉพาะยาเม็ดขนาด 10 มก.) ( E172) , ไอรอนออกไซด์สีเหลือง (E172) และแป้งโรยตัว
สิ่งที่ Efient ดูเหมือนและเนื้อหาของแพ็ค
Efient 10 มก.: เม็ดยามีสีเบจและมีรูปร่างเหมือนลูกศรคู่ แกะสลักด้วย "10 MG" ที่ด้านหนึ่งและ "4759" ที่อีกด้านหนึ่ง
Efient 5 มก.: เม็ดยามีสีเหลืองและรูปลูกศรคู่ สลัก "5 MG" ที่ด้านหนึ่งและ "4760" อีกด้านหนึ่ง
Efient มีจำหน่ายในแพ็ค 14, 28, 30, 56, 84, 90 และ 98 เม็ด
ขนาดของบรรจุภัณฑ์อาจไม่สามารถวางตลาดได้ทั้งหมด
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่นำเสนออาจไม่ใช่ข้อมูลล่าสุด
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
EFIENT 10 MG TABLETS เคลือบฟิล์ม
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
แต่ละเม็ดประกอบด้วย prasugrel 10 มก. (ในรูปของไฮโดรคลอไรด์)
สารเพิ่มปริมาณที่ทราบผลกระทบ: แต่ละเม็ดมีแลคโตส 2.1 มก.
สำหรับรายการสารปรุงแต่งทั้งหมด โปรดดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
แท็บเล็ตเคลือบฟิล์ม (แท็บเล็ต)
เม็ดรูปลูกศรคู่สีเบจ แกะลาย "10 MG" ด้านหนึ่งและ "4759" อีกด้านหนึ่ง
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
มีประสิทธิภาพเมื่อใช้ร่วมกับกรดอะซิติลซาลิไซลิก (ASA) เพื่อป้องกันเหตุการณ์ atherothrombotic ในผู้ป่วยผู้ใหญ่ที่เป็นโรคหลอดเลือดหัวใจเฉียบพลัน (ACS) (เช่น โรคหลอดเลือดหัวใจตีบที่ไม่เสถียร กล้ามเนื้อหัวใจตายโดยไม่มีส่วนสูงของ ST [UA / NSTEMI] หรือ ST-segment ภาวะกล้ามเนื้อหัวใจตายสูง (STEMI)) ระหว่างการแทรกแซงหลอดเลือดหัวใจหลักหรือล่าช้า (PCI)
สำหรับข้อมูลเพิ่มเติม โปรดดูหัวข้อ 5.1
04.2 วิทยาและวิธีการบริหาร
ปริมาณ
ผู้ใหญ่
Efient ควรเริ่มต้นด้วยขนาดบรรจุ 60 มก. เพียงครั้งเดียวแล้วให้ต่อเนื่องที่ 10 มก. วันละครั้ง ผู้ป่วยที่รับประทาน Efient ควรรับประทาน acetylsalicylic acid (ASA) 75 มก. - 325 มก. ต่อวัน
ในผู้ป่วยที่เป็นโรคหลอดเลือดหัวใจเฉียบพลัน (ACS) ที่ได้รับการแทรกแซงของหลอดเลือดหัวใจ การหยุดยาต้านเกล็ดเลือดตั้งแต่เนิ่นๆ ซึ่งรวมถึง Efient อาจนำไปสู่ความเสี่ยงที่เพิ่มขึ้นของการเกิดลิ่มเลือด กล้ามเนื้อหัวใจตาย หรือเสียชีวิตเนื่องจากภาวะทางการแพทย์พื้นฐานของผู้ป่วย แนะนำให้ใช้ระยะเวลาเดือนเว้นแต่จะมีการระบุไว้ทางคลินิก (ดูหัวข้อ 4.4 และ 5.1)
ผู้ป่วยอายุ ≥ อายุ 75 ปี
โดยทั่วไปไม่แนะนำให้ใช้ Efient ในผู้ป่วยที่มีอายุ≥ 75 ปี หากหลังจากการประเมินอย่างรอบคอบของผลประโยชน์ส่วนบุคคล/อัตราส่วนความเสี่ยงโดยแพทย์ผู้สั่งจ่าย (ดูหัวข้อ 4.4) การรักษาด้วย Efient ถือว่าจำเป็นในผู้ป่วยในกลุ่มอายุ ≥ 75 ปี จากนั้นควรกำหนดขนาดยาบำรุงรักษาที่ลดลง 5 มก. หลังจากรับประทานยา 60 มก. ผู้ป่วยที่อายุ≥ 75 ปีมีความไวต่อเลือดออกเพิ่มขึ้นและการได้รับสารออกฤทธิ์เมตาโบไลต์ของ prasugrel เพิ่มขึ้น (ดูหัวข้อ 4.4, 4.8, 5.1 และ 5.2)
ผู้ป่วยที่มีน้ำหนักตัว
ควรใช้ประสิทธิภาพเป็นขนาดบรรจุ 60 มก. เดียวตามด้วยขนาด 5 มก. วันละครั้ง ไม่แนะนำให้ใช้ขนาดยาบำรุง 10 มก. เนื่องจากการเพิ่มขึ้นของการสัมผัสกับสารที่ใช้งานของ prasugrel และความเสี่ยงที่เพิ่มขึ้นของการตกเลือดในผู้ป่วยที่มีน้ำหนัก
การด้อยค่าของไต
ไม่จำเป็นต้องปรับขนาดยาสำหรับผู้ป่วยที่มีภาวะไตวาย รวมทั้งผู้ป่วยที่เป็นโรคไตวายเรื้อรังระยะสุดท้าย (ดูหัวข้อ 5.2) มีประสบการณ์การรักษาที่จำกัดในผู้ป่วยที่มีภาวะไตวาย (ดูหัวข้อ 4.4)
การด้อยค่าของตับ
ไม่จำเป็นต้องปรับขนาดยาในอาสาสมัครที่มีความบกพร่องของตับเล็กน้อยถึงปานกลาง (Child-Pugh class A และ B) (ดูหัวข้อ 5.2) มีประสบการณ์การรักษาที่จำกัดในผู้ป่วยที่มีความบกพร่องทางตับในระดับเล็กน้อยและปานกลาง (ดูหัวข้อ 4.4) Efient ถูกห้ามใช้ในผู้ป่วยที่มีความบกพร่องทางตับอย่างรุนแรง (Child Pugh class C)
ประชากรเด็ก
ความปลอดภัยและประสิทธิภาพของ Efient ในเด็กอายุต่ำกว่า 18 ปียังไม่เป็นที่ยอมรับ ไม่มีข้อมูล
วิธีการบริหาร
สำหรับใช้ในช่องปาก สามารถให้ประสิทธิภาพได้โดยไม่คำนึงถึงอาหาร การใช้ prasugrel ขนาด 60 มก. ในสภาวะที่อดอาหารอาจส่งผลให้ผลิตภัณฑ์ยาเริ่มออกฤทธิ์เร็วขึ้น (ดูหัวข้อ 5.2) อย่าบดหรือทำลายแท็บเล็ต
04.3 ข้อห้าม
ภูมิไวเกินต่อสารออกฤทธิ์หรือสารเพิ่มปริมาณใด ๆ ที่ระบุไว้ในหัวข้อ 6.1
กำลังมีเลือดออกทางพยาธิวิทยา
ประวัติโรคหลอดเลือดสมองตีบหรือการโจมตีขาดเลือดชั่วคราว (TIA)
ความผิดปกติของตับอย่างรุนแรง (Child-Pugh class C)
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
เสี่ยงเลือดออก
ในการทดลองทางคลินิกระยะที่ 3 เกณฑ์การคัดออกที่สำคัญรวมถึงความเสี่ยงที่เพิ่มขึ้นของการตกเลือด โรคโลหิตจาง; ภาวะเกล็ดเลือดต่ำ; ประวัติการค้นพบที่บ่งบอกถึงพยาธิสภาพในกะโหลกศีรษะ
ผู้ป่วยที่เป็นโรคหลอดเลือดหัวใจเฉียบพลันที่ได้รับการแทรกแซงหลอดเลือดหัวใจด้วย Efient และ ASA พบว่ามีความเสี่ยงเพิ่มขึ้นที่จะมีเลือดออกมากหรือน้อยตามระบบการจำแนก TIMI
ดังนั้นควรใช้ Efient ในผู้ป่วยที่มีความเสี่ยงต่อการตกเลือดเพิ่มขึ้นก็ต่อเมื่อพิจารณาถึงประโยชน์ในแง่ของการป้องกันภาวะขาดเลือดมีมากกว่าความเสี่ยงของการมีเลือดออกรุนแรง ข้อควรระวังนี้ โดยเฉพาะกับผู้ป่วย:
• อายุ ≥75 ปี (ดูด้านล่าง)
• มีแนวโน้มที่จะตกเลือด (เช่น เนื่องจากการบาดเจ็บเมื่อเร็วๆ นี้ การผ่าตัดเมื่อเร็วๆ นี้ เลือดออกในทางเดินอาหารเมื่อเร็วๆ นี้หรือเกิดขึ้นอีก หรือโรคแผลในกระเพาะอาหารที่กำลังดำเนินอยู่)
• ด้วยน้ำหนักตัว
• ในการรักษาร่วมกับยาที่อาจเพิ่มความเสี่ยงต่อการตกเลือด ได้แก่ ยาต้านการแข็งตัวของเลือดในช่องปาก, clopidogrel, ยาต้านการอักเสบที่ไม่ใช่สเตียรอยด์ (NSAIDs) และยาละลายลิ่มเลือด
สำหรับผู้ป่วยที่มีเลือดออกอย่างต่อเนื่องซึ่งจำเป็นต้องย้อนกลับผลทางเภสัชวิทยาของ Efient การถ่ายเกล็ดเลือดอาจเหมาะสม
โดยทั่วไปไม่แนะนำให้ใช้ยา Efient แก่ผู้ป่วยที่อายุมากกว่า 75 ปีและควรทำด้วยความระมัดระวังหลังจาก "การประเมินผลประโยชน์ / ความเสี่ยงของแต่ละบุคคลอย่างระมัดระวังโดยแพทย์ที่สั่งจ่ายยาระบุว่าผลประโยชน์ในการป้องกันเหตุการณ์ขาดเลือดมีมากกว่าความเสี่ยงของการมีเลือดออกรุนแรง ในการทดลองทางคลินิกระยะที่ 3 ผู้ป่วยเหล่านี้มีความเสี่ยงต่อการตกเลือดรวมทั้งเลือดออกร้ายแรงเมื่อเทียบกับผู้ป่วยอายุ
ประสบการณ์การรักษากับ prasugrel นั้นจำกัดในผู้ป่วยที่มีความผิดปกติของไต (รวมถึงผู้ป่วยที่เป็นโรคไตวายเรื้อรังระยะสุดท้าย (ESRD)) และในผู้ป่วยที่มีความผิดปกติของตับในระดับปานกลาง ผู้ป่วยเหล่านี้อาจมีความเสี่ยงต่อการตกเลือด
ดังนั้นควรใช้ prasugrel ด้วยความระมัดระวังในผู้ป่วยเหล่านี้
ผู้ป่วยควรทราบว่าเมื่อใช้ prasugrel (ร่วมกับ ASA) อาจใช้เวลานานกว่าปกติในการหยุดเลือด และควรแจ้งให้แพทย์ทราบหากมีเลือดออกผิดปกติ (ตามสถานที่หรือระยะเวลา)
การแทรกแซงการผ่าตัด
ก่อนทำการผ่าตัดใดๆ และก่อนรับประทานยาใหม่ ผู้ป่วยควรแจ้งแพทย์และทันตแพทย์ว่ากำลังใช้ยาพราซูเกรล หากผู้ป่วยต้องได้รับการผ่าตัดแบบเลือกและพิจารณาว่ายาต้านเกล็ดเลือดไม่เหมาะสม ควรหยุดยา Efient อย่างน้อย 7 วันก่อนการผ่าตัด ผู้ป่วยอาจมีความถี่และความรุนแรงของการตกเลือดเพิ่มขึ้น (3 เท่า) 7 วันของการหยุด prasugrel (ดูหัวข้อ 4.8)ประโยชน์และความเสี่ยงของ prasugrel ควรได้รับการชั่งน้ำหนักอย่างรอบคอบในผู้ป่วยที่ไม่ได้กำหนดลักษณะทางกายวิภาคของหลอดเลือดหัวใจและอาจมีการแทรกแซง CABG อย่างเร่งด่วน
แพ้รวมทั้ง angioedema
มีรายงานผู้ป่วยที่ได้รับ prasugrel รวมทั้งผู้ป่วยที่มีประวัติแพ้ยา clopidogrel แนะนำให้ติดตามสัญญาณของภาวะภูมิไวเกินในผู้ป่วยที่มีประวัติแพ้ยา thienopyridines (ดูหัวข้อ 4.8)
Thrombotic Thrombocytopenic Purpura (ปตท.)
ปตท. ได้รับรายงานเกี่ยวกับการใช้ prasugrel ปตท. เป็นภาวะร้ายแรงที่ต้องรักษาทันที
แลคโตส
ผู้ป่วยที่มีปัญหาทางพันธุกรรมที่หายากของการแพ้กาแลคโตส, การขาดแลคเตส Lapp หรือการดูดซึมน้ำตาลกลูโคส - กาแลคโตส malabsorption ไม่ควรใช้ Efient.
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
วาร์ฟาริน: ยังไม่มีการศึกษาการบริหารอนุพันธ์ Efient และ coumarin ร่วมกันนอกเหนือจาก warfarin เนื่องจากมีโอกาสเสี่ยงต่อการตกเลือดมากขึ้น ควรใช้ความระมัดระวังในการใช้ยาวาร์ฟารินร่วมกัน (หรืออนุพันธ์ของคูมารินอื่นๆ) และพราซูเกรล (ดูหัวข้อ 4.4)
ยาต้านการอักเสบที่ไม่ใช่สเตียรอยด์ (NSAIDs):
ยังไม่มีการศึกษาการใช้ยากลุ่ม NSAID เรื้อรังร่วมกัน เนื่องจากมีความเป็นไปได้ที่จะมีความเสี่ยงต่อการตกเลือดมากขึ้น ควรใช้ NSAIDs เรื้อรังร่วมกัน (รวมถึงสารยับยั้ง COX-2) และ Efient ด้วยความระมัดระวัง (ดูหัวข้อ 4.4)
สามารถบริหารให้มีประสิทธิภาพร่วมกับผลิตภัณฑ์ยาที่เผาผลาญโดยเอนไซม์ไซโตโครม P450 (รวมถึงสแตติน) หรือผลิตภัณฑ์ยาที่เป็นตัวกระตุ้นหรือตัวยับยั้งของเอ็นไซม์ไซโตโครม P450 นอกจากนี้ยังสามารถให้ Efient ร่วมกับ ASA, heparin, digoxin และยาที่เพิ่ม pH ในกระเพาะอาหาร ซึ่งรวมถึงสารยับยั้งโปรตอนปั๊มและตัวบล็อก H2
แม้ว่าจะไม่ใช่เรื่องของการศึกษาปฏิสัมพันธ์ที่เฉพาะเจาะจง แต่ Efient ได้รับยาในการศึกษาทางคลินิกระยะที่ 3 ร่วมกับสารยับยั้ง heparin, bivalirudin และ GP IIb / IIIa ที่มีน้ำหนักโมเลกุลต่ำ (ไม่มีข้อมูลเกี่ยวกับชนิดของตัวยับยั้งของ GP IIb / IIIa ใช้) โดยไม่มีหลักฐานของการโต้ตอบที่ไม่พึงประสงค์ที่มีนัยสำคัญทางคลินิก
ผลของยาอื่นๆ ต่อ Efient:
กรดอะซิทิลซาลิไซลิก: ต้องใช้ประสิทธิภาพร่วมกับ ASA แม้ว่าปฏิกิริยาทางเภสัชพลศาสตร์กับ ASA กับความเสี่ยงที่เพิ่มขึ้นของการตกเลือดจะเป็นไปได้ แต่หลักฐานของประสิทธิภาพและความปลอดภัยของ prasugrel มาจากผู้ป่วยที่รักษาร่วมกับ ASA
เฮปาริน: การให้เฮปารินแบบไม่แยกส่วน (100 U / kg) ทางหลอดเลือดดำเพียงครั้งเดียวไม่ได้เปลี่ยนแปลงการยับยั้งการรวมตัวของเกล็ดเลือดที่ใช้ prasugrel อย่างมีนัยสำคัญ ในทำนองเดียวกัน prasugrel ไม่ได้เปลี่ยนแปลงผลของเฮปารินอย่างมีนัยสำคัญต่อพารามิเตอร์การแข็งตัวของเลือด
ดังนั้นจึงสามารถให้ยาทั้งสองชนิดร่วมกันได้ ความเสี่ยงที่เพิ่มขึ้นของการตกเลือดเป็นไปได้เมื่อให้ Efient ร่วมกับเฮปาริน
สแตติน: Atorvastatin (80 มก. ต่อวัน) ไม่ได้เปลี่ยนแปลงฤทธิ์ทางเภสัชพลศาสตร์ของ prasugrel หรือการยับยั้งการรวมตัวของเกล็ดเลือด ดังนั้น สแตติน CYP3A จึงไม่คาดว่าจะมีผลต่อเภสัชจลนศาสตร์ของ prasugrel หรือการยับยั้ง prasugrel.
ยาที่เพิ่มค่า pH ในกระเพาะอาหาร: การบริหารร่วมกันของ ranitidine (ตัวบล็อก H2) หรือ lansoprazole (ตัวยับยั้งโปรตอนปั๊ม) ทุกวันไม่ได้เปลี่ยน AUC และ Tmax ของสารออกฤทธิ์ของ prasugrel แต่ลดลง Cmax 14% และ 29% ในการทดลองทางคลินิกระยะที่ 3 , Efient ได้รับการบริหารโดยอิสระจากการใช้ proton pump inhibitor หรือ H2 blocker ร่วมกัน การใช้ prasugrel ขนาด 60 มก. โดยไม่ใช้ proton pump inhibitor ร่วมกัน อาจส่งผลให้ยาออกฤทธิ์เร็วขึ้น
สารยับยั้ง CYP3A: Ketoconazole (400 มก. ต่อวัน) ซึ่งเป็นตัวยับยั้ง CYP3A4 และ CYP3A5 ที่มีศักยภาพและคัดเลือกไม่ได้เปลี่ยนการยับยั้งการรวมตัวของเกล็ดเลือดที่อาศัย prasugrel หรือ AUC และ T ของสารออกฤทธิ์ของ prasugrel แต่ลด Cmax 34% เป็น 46% ดังนั้น สารยับยั้ง CYP3A เช่น azole antifungals, HIV protease inhibitors, clarithromycin, telithromycin, verapamil, diltiazem, indinavir, ciprofloxacin และน้ำเกรพฟรุตจึงไม่คาดว่าจะส่งผลกระทบอย่างมีนัยสำคัญต่อเภสัชจลนศาสตร์ของ metabolite
ตัวเหนี่ยวนำของไซโตโครม P450: Rifampicin (600 มก. ต่อวัน) ซึ่งเป็นตัวกระตุ้นที่มีศักยภาพของ CYP3A และ CYP2B6 รวมทั้งตัวกระตุ้น CYP2C9, CYP2C19 และ CYP2C8 ไม่ได้เปลี่ยนแปลงเภสัชจลนศาสตร์ของ prasugrel อย่างมีนัยสำคัญ ดังนั้น สารกระตุ้นที่เป็นที่รู้จักของ CYP3A เช่น rifampicin, carbamazepine และตัวกระตุ้นอื่นๆ ของ cytochromes P450 จึงไม่คาดว่าจะส่งผลกระทบอย่างมีนัยสำคัญต่อเภสัชจลนศาสตร์ของสารออกฤทธิ์
ผลของ Efient ต่อผลิตภัณฑ์ยาอื่นๆ:
ดิจอกซิน: Prasugrel ไม่มีผลต่อเภสัชจลนศาสตร์ของดิจอกซินอย่างมีนัยสำคัญทางคลินิก
ผลิตภัณฑ์ยาที่เผาผลาญโดย CYP2C9: Prasugrel ไม่ได้ยับยั้ง CYP2C9 เนื่องจากไม่ส่งผลต่อเภสัชจลนศาสตร์ของ warfarin-S เนื่องจากอาจมีความเสี่ยงที่จะมีเลือดออกเพิ่มขึ้น ควรใช้ความระมัดระวังในการใช้ยาวาร์ฟารินและเอไฟน์ร่วมกัน (ดูหัวข้อ 4.4)
ผลิตภัณฑ์ยาที่เผาผลาญโดย CYP2B6: Prasugrel เป็นตัวยับยั้ง CYP2B6 ที่อ่อนแอ ในคนที่มีสุขภาพดี prasugrel ลดการสัมผัสกับ hydroxybupropion ซึ่งเป็นเมตาโบไลต์ของ bupropion ที่อาศัย CYP2B6 ของ bupropion ลง 23% ผลกระทบนี้น่าจะเป็นเรื่องที่น่ากังวลทางคลินิกเฉพาะเมื่อมีการให้ prasugrel ร่วมกับผลิตภัณฑ์ยาที่ CYP2B6 เป็นวิถีทางเมแทบอลิซึมเดียวและมีหน้าต่างการรักษาที่จำกัด (เช่น cyclophosphamide, efavirenz)
04.6 การตั้งครรภ์และให้นมบุตร
ไม่มีการศึกษาทางคลินิกในสตรีมีครรภ์หรือให้นมบุตร
การตั้งครรภ์
การศึกษาในสัตว์ทดลองไม่ได้บ่งชี้ถึงผลร้ายโดยตรงต่อการตั้งครรภ์ พัฒนาการของตัวอ่อน/ทารกในครรภ์ การคลอด หรือพัฒนาการหลังคลอด (ดูหัวข้อ 5.3) เนื่องจากการศึกษากิจกรรมการสืบพันธุ์ในสัตว์ไม่ได้คาดการณ์ถึงผลกระทบในมนุษย์เสมอไป ควรใช้ Efient ในการตั้งครรภ์ก็ต่อเมื่อผลประโยชน์ที่เป็นตัวกำหนดความเสี่ยงที่อาจเกิดขึ้นกับทารกในครรภ์
เวลาให้อาหาร
ไม่ทราบว่า prasugrel ถูกขับออกมาในนมของมนุษย์หรือไม่ การศึกษาในสัตว์ทดลองแสดงให้เห็นว่ามีการกำจัด prasugrel ในน้ำนมแม่ ไม่แนะนำให้ใช้ prasugrel ระหว่างเลี้ยงลูกด้วยนม
ภาวะเจริญพันธุ์
Prasugrel ไม่มีผลต่อภาวะเจริญพันธุ์ของเพศชายและเพศหญิงในหนูที่ได้รับยาทางปากถึง 240 เท่าของปริมาณที่แนะนำต่อวันของมนุษย์ (ประเมินเป็นมิลลิกรัมต่อตารางเมตร)
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
Prasugrel ไม่คาดว่าจะส่งผลกระทบหรือส่งผลกระทบเพียงเล็กน้อยต่อความสามารถในการขับหรือใช้เครื่องจักร
04.8 ผลกระทบที่ไม่พึงประสงค์
สรุปข้อมูลความปลอดภัย
ความปลอดภัยในผู้ป่วยโรคหลอดเลือดหัวใจเฉียบพลันที่ได้รับการแทรกแซงหลอดเลือดผ่านผิวหนังได้รับการประเมินในการทดลองทางคลินิกที่ควบคุมด้วย clopidogrel (TRITON) ซึ่งผู้ป่วย 6,741 รายได้รับการรักษาด้วย prasugrel (ด้วยขนาด 60 มก. และปริมาณการบำรุงรักษา 10 มก. ต่อวัน) สำหรับ ค่ามัธยฐาน 14.5 เดือน (ผู้ป่วย 5,802 รายได้รับการรักษานานกว่า 6 เดือน, ผู้ป่วย 4,136 รายได้รับการรักษานานกว่า 1 ปี) อัตราการหยุดยาที่ใช้ในการศึกษาเนื่องจากเหตุการณ์ไม่พึงประสงค์คือ 7.2% สำหรับ prasugrel และ 6.3% สำหรับ clopidogrel ในจำนวนนี้ การตกเลือดเป็นอาการไม่พึงประสงค์ที่พบบ่อยที่สุดที่นำไปสู่การหยุดยาในการศึกษาสำหรับยาทั้งสองชนิด (2.5% สำหรับ prasugrel และ 1.4% สำหรับ clopidogrel)
เลือดออก
เลือดออกไม่เกี่ยวข้องกับการปลูกถ่ายบายพาสหลอดเลือดหัวใจ (CABG)
ในการศึกษาของ TRITON ความถี่ของผู้ป่วยที่มีภาวะเลือดออกที่ไม่เกี่ยวข้องกับการปลูกถ่ายหลอดเลือดหัวใจ (CABG) แสดงไว้ในตารางที่ 1 อุบัติการณ์ของการตกเลือดที่สำคัญ (ตามคำจำกัดความของ TIMI) ที่ไม่เกี่ยวข้องกับการปลูกถ่ายหลอดเลือดหัวใจ (CABG) รวมทั้งผู้ที่มีความเสี่ยงต่อการเสียชีวิตและเสียชีวิต รวมถึงการมีเลือดออกเล็กน้อย (ตามคำจำกัดความของ TIMI) อย่างมีนัยสำคัญทางสถิติในผู้ป่วยที่ได้รับ prasugrel เมื่อเทียบกับกลุ่มที่ได้รับ clopidogrel ทั้งใน UA / NSTEMI มากกว่าในกลุ่ม ACS ทั้งหมด . ไม่พบความแตกต่างอย่างมีนัยสำคัญในประชากร STEMI บริเวณที่พบบ่อยที่สุดของเลือดออกเองคือทางเดินอาหาร (1.7% กับ prasugrel และ 1.3% กับ clopidogrel); ตำแหน่งที่เกิดการตกเลือดบ่อยที่สุดคือบริเวณเข้าถึงหลอดเลือด (1.3% กับ prasugrel และ 1.2% กับ clopidogrel)
ตารางที่ 1: อุบัติการณ์เลือดออกที่ไม่เกี่ยวข้องกับการผ่าตัดบายพาสหลอดเลือดหัวใจ (CABG) a (% ของผู้ป่วย)
เหตุการณ์ที่กำหนดโดยเกณฑ์ของกลุ่มศึกษาการอุดตันของลิ่มเลือดในกล้ามเนื้อหัวใจตาย (TIMI) ที่อยู่ระหว่างการประเมิน รวมศูนย์
b การรักษามาตรฐานอื่น ๆ ได้รับการบริหารตามความเหมาะสม
c เลือดออกในกะโหลกศีรษะหรือมีเลือดออกที่เห็นได้ชัดทางคลินิกที่เกี่ยวข้องกับการลดลง ของฮีโมโกลบิน ≥5 g / dl.
d เลือดออกที่เสี่ยงต่อการเสียชีวิตเป็นกลุ่มย่อยของการตกเลือดที่สำคัญ (ตามคำจำกัดความของ TIMI) e รวมถึงประเภทที่ระบุไว้ด้านล่าง ผู้ป่วยสามารถนับได้มากกว่าหนึ่งแถว
และ ICH = การตกเลือดในกะโหลกศีรษะ
ฉ มีเลือดออกชัดเจนทางคลินิกที่เกี่ยวข้องกับการลดลงของฮีโมโกลบิน ≥3 g / dl และ
ผู้ป่วยอายุ ≥ อายุ 75 ปี
อัตราการตกเลือดที่สำคัญหรือเล็กน้อย (TIMI) ที่ไม่เกี่ยวข้องกับการปลูกถ่ายหลอดเลือดหัวใจ (CABG):
* การศึกษาของ TRITON ในผู้ป่วย ACS ที่ได้รับ PCI
** การศึกษา TRILOGY-ACS ในผู้ป่วยที่ไม่ได้รับ PCI (ดูหัวข้อ 5.1):
ถึง prasugrel 10 มก.; prasugrel 5 มก. ถ้า
ผู้ป่วยที่มีน้ำหนักตัว
อัตราการตกเลือดที่สำคัญหรือเล็กน้อย (TIMI) ที่ไม่เกี่ยวข้องกับการปลูกถ่ายหลอดเลือดหัวใจ (CABG):
* การศึกษาของ TRITON ในผู้ป่วย ACS ที่ได้รับ PCI
** การศึกษา TRILOGY-ACS ในผู้ป่วยที่ไม่ได้รับ PCI (ดูหัวข้อ 5.1):
ถึง prasugrel 10 มก.; prasugrel 5 มก. ถ้า≥75 ปี
ผู้ป่วยที่มีน้ำหนัก ≥60 กก. และอายุ
ในผู้ป่วยที่มีน้ำหนัก ≥60 กก. และ อายุ
เลือดออกที่เกี่ยวข้องกับการปลูกถ่ายบายพาสหลอดเลือดหัวใจ (CABG)
ในการทดลองทางคลินิกระยะที่ 3 มีผู้ป่วย 437 รายเข้ารับการปลูกถ่ายหลอดเลือดหัวใจตีบ (CABG) ในผู้ป่วยเหล่านี้ อัตราการเลือดออกมากหรือน้อย (TIMI) ที่เกี่ยวข้องกับการปลูกถ่ายหลอดเลือดหัวใจตีบ (CABG) เท่ากับ 14.1% สำหรับกลุ่ม prasugrel และ 4.5% สำหรับกลุ่ม clopidogrel ความเสี่ยงสูงสุดสำหรับภาวะเลือดออกในอาสาสมัครที่ได้รับการรักษาด้วย prasugrel ยังคงมีอยู่นานถึง 7 วันหลังจากรับประทานยาที่ใช้ในการศึกษาครั้งล่าสุด สำหรับผู้ป่วยที่ได้รับ thienopyridine ภายใน 3 วันก่อนการปลูกถ่ายหลอดเลือดหัวใจ (CABG) อัตราการเลือดออกที่สำคัญหรือเล็กน้อย (TIMI) เท่ากับ 26.7% (12 ใน 45 ราย) ในกลุ่ม prasugrel เทียบกับ 5.0% (3 ของ ผู้ป่วย 60 ราย) ในกลุ่ม clopidogrel สำหรับผู้ป่วยที่ได้รับยา thienopyridine ครั้งสุดท้ายภายใน 4 ถึง 7 วันก่อนการปลูกถ่ายหลอดเลือดหัวใจ (CABG) ความถี่ลดลงเหลือ 11.3% (9 จาก 80 ราย) ในกลุ่ม prasugrel และ 3.4 % (3 จาก 89 ราย) ในกลุ่มที่ได้รับ clopidogrel มากกว่า 7 วันหลังจากหยุดยา อัตราการตกเลือดที่สังเกตพบที่เกี่ยวข้องกับการปลูกถ่ายหลอดเลือดหัวใจตีบ (CABG) มีความคล้ายคลึงกันระหว่าง 2 กลุ่มการรักษา (ดูหัวข้อ 4.4)
ตารางสรุปอาการไม่พึงประสงค์
ตารางที่ 2 สรุปอาการไม่พึงประสงค์จากการตกเลือดและไม่มีเลือดออกในการศึกษาของ TRITON หรือจากรายงานที่เกิดขึ้นเองซึ่งจำแนกตามความถี่และตามอวัยวะของระบบ ความถี่ถูกกำหนดโดยใช้อนุสัญญาต่อไปนี้: ธรรมดามาก (≥ 1/10); ทั่วไป (≥ 1/100,
ตารางที่ 2: อาการไม่พึงประสงค์จากเลือดออกและไม่ใช่เลือดออก
ในผู้ป่วยที่มีหรือไม่มีประวัติการโจมตีขาดเลือดชั่วคราว (TIA) หรือโรคหลอดเลือดสมอง อุบัติการณ์ของโรคหลอดเลือดสมองในการศึกษาระยะที่ 3 มีดังนี้ (ดูหัวข้อ 4.4):
* ICH = การตกเลือดในกะโหลกศีรษะ
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยซึ่งเกิดขึ้นหลังจากการอนุมัติผลิตภัณฑ์ยามีความสำคัญเนื่องจากช่วยให้สามารถตรวจสอบความสมดุลของผลประโยชน์/ความเสี่ยงของผลิตภัณฑ์ยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านสุขภาพรายงานอาการไม่พึงประสงค์ที่น่าสงสัยผ่านระบบการรายงานระดับประเทศ ในภาคผนวก 5 .
04.9 ใช้ยาเกินขนาด
การใช้ยาเกินขนาดของ Efient อาจทำให้เลือดออกเป็นเวลานานและทำให้เกิดภาวะแทรกซ้อนเลือดออกได้ ไม่มีข้อมูลเกี่ยวกับ "การยกเลิก" กิจกรรมทางเภสัชวิทยาของ prasugrel; อย่างไรก็ตาม เมื่อจำเป็นต้องมีการแก้ไขอย่างรวดเร็วของการมีเลือดออกเป็นเวลานาน อาจพิจารณาการถ่ายเกล็ดเลือดหรือผลิตภัณฑ์เลือดอื่นๆ
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
กลุ่มยารักษาโรค: ยาต้านเกล็ดเลือด ยกเว้นเฮปาริน
รหัส ATC: B01AC22
ผลทางเภสัชพลศาสตร์
Prasugrel เป็นตัวยับยั้งการกระตุ้นและการรวมตัวของเกล็ดเลือดซึ่งทำหน้าที่ผ่านการผูกมัดที่ไม่สามารถย้อนกลับของสารออกฤทธิ์กับตัวรับเกล็ดเลือด ADP คลาส P2Y12 การทำงานของเกล็ดเลือดอาจทำให้ความถี่ของเหตุการณ์หัวใจและหลอดเลือดลดลงเช่นความตายกล้ามเนื้อหัวใจตายหรือโรคหลอดเลือดสมอง
หลังจากให้ยา Prasugrel ขนาด 60 มก. การยับยั้งการรวมตัวของเกล็ดเลือดที่เกิดจาก ADP จะเกิดขึ้นที่ 15 นาทีด้วย ADP 5 mcM และที่ 30 นาทีด้วย ADP 20 mcM การยับยั้งการรวมตัวของเกล็ดเลือดสูงสุด เกิดจาก ADP ที่ได้รับด้วย prasugrel คือ 83% ด้วย ADP 5 mcM และ 79% ด้วย ADP 20 mcM ในทั้งสองกรณีที่มี 89% ของอาสาสมัครที่มีสุขภาพดีและผู้ป่วยที่มีภาวะหลอดเลือดที่เสถียรถึงอย่างน้อย 50% ของการยับยั้งการรวมตัวของเกล็ดเลือดภายใน 1 ชั่วโมง การยับยั้งการรวมตัวของเกล็ดเลือดที่ทำได้ด้วย Prasugrel แสดงความแปรปรวนระหว่าง (9%) และภายในบุคคล (12%) ที่ลดลงด้วย ADP ทั้ง 5 mcM และ 20 mcM ค่าเฉลี่ยการยับยั้งการรวมตัวของเกล็ดเลือดที่สมดุลคือ 74% และ 69% โดยมี ADP 5 mcM และ 20 mcM ของ ADP ตามลำดับและเกิดขึ้นได้หลังจากระยะเวลา 3 ถึง 5 วันของการบริหารครั้งเดียว ปริมาณการบำรุงรักษา 10 prasugrel มก. นำหน้าด้วยขนาดยา 60 มก. กว่า 98% ของผู้ป่วยมีการยับยั้งการรวมตัวของเกล็ดเลือด≥ 20% ระหว่างปริมาณการบำรุงรักษา
หลังการรักษา การรวมตัวของเกล็ดเลือดจะค่อยๆ กลับสู่การตรวจวัดพื้นฐานในช่วง 7 ถึง 9 วันหลังจากให้ยา Prasugrel ขนาด 60 มก. แบบใส่ครั้งเดียว และมากกว่า 5 วันหลังจากหยุดการให้ยาเพื่อการรักษาสมดุล
ข้อมูลการเปลี่ยนจาก clopidogrel เป็น prasugrel: หลังจากได้รับ clopidogrel 75 มก. วันละครั้งเป็นเวลา 10 วัน ผู้ป่วยที่มีสุขภาพดี 40 คนถูกเปลี่ยนเป็น prasugrel 10 มก. วันละครั้ง โดยมีหรือไม่มีขนาดยา 60 มก. พบว่ามีการยับยั้งการรวมตัวของเกล็ดเลือดที่คล้ายกันหรือสูงกว่าด้วย prasugrel การเปลี่ยนไปใช้ขนาด 60 มก. ของ prasugrel โดยตรงส่งผลให้การยับยั้งเกล็ดเลือดเพิ่มขึ้นเร็วขึ้นหลังจากได้รับ clopidogrel ขนาด 900 มก. (ร่วมกับ ASA) ผู้ป่วยที่ได้รับ ACS จำนวน 56 คนได้รับการรักษาเป็นเวลา 14 วันด้วย prasugrel 10 มก. วันละครั้งหรือ clopidogrel 150 มก. วันละครั้งและอยู่ระหว่างการเปลี่ยนแปลงการรักษาเป็น clopidogrel 150 มก. หรือ prasugrel 10 มก. เป็นเวลา 14 วันเพิ่มเติมตามลำดับ ("สวิตช์") การยับยั้งการรวมตัวของเกล็ดเลือดที่ใหญ่ที่สุดพบได้ในผู้ป่วยที่เปลี่ยนมาใช้ prasugrel 10 มก. เมื่อเทียบกับผู้ที่ได้รับ clopidogrel 150 มก. ในการศึกษาผู้ป่วย ACS 276 คนที่ได้รับ PCI โดยเปลี่ยนจากขนาดยาเริ่มต้นของ clopidogrel หรือ placebo ขนาด 600 มก. ในการเข้ารับการรักษาในโรงพยาบาล ก่อนทำการตรวจหลอดเลือดหัวใจด้วยขนาดยา Prasugrel 60 มก. ที่ได้รับในช่วงเวลาของการแทรกแซงของหลอดเลือดหัวใจผ่านผิวหนัง ส่งผลให้จำนวนเกล็ดเลือดที่ยับยั้งการรวมกลุ่มเพิ่มขึ้นในทำนองเดียวกันในระหว่างระยะเวลาการศึกษา 72 ชั่วโมง
ประสิทธิภาพและความปลอดภัยในโรคหลอดเลือดหัวใจเฉียบพลัน
ในการศึกษา TRITON ระยะที่ 3 เปรียบเทียบ Efient (prasugrel) กับ clopidogrel โดยทั้งสองให้ร่วมกับ ASA และการรักษามาตรฐานอื่นๆ TRITON คือการศึกษาแบบหลายศูนย์แบบหลายศูนย์แบบสุ่ม สุ่มสองทาง สุ่มคู่ ระดับนานาชาติ ซึ่งมีผู้ป่วย 13,608 ราย ผู้ป่วยมี ACS ที่มีความเสี่ยงปานกลางถึงสูง UA และ NSTEMI หรือ STEMI และได้รับการจัดการด้วย PCI
ผู้ป่วย UA / NSTEMI ภายใน 72 ชั่วโมงหลังจากเริ่มมีอาการหรือมี STEMI ตั้งแต่ 12 ชั่วโมงถึง 14 วันที่เริ่มมีอาการได้รับการสุ่มตัวอย่างหลังจากทราบลักษณะทางกายวิภาคของหลอดเลือดหัวใจ ผู้ป่วย STEMI ภายใน 12 ชั่วโมงหลังจากเริ่มมีอาการและกำหนดไว้สำหรับ PCI หลัก สามารถสุ่มได้โดยไม่มีความรู้เกี่ยวกับภาพหัวใจ ในผู้ป่วยทุกราย สามารถให้ขนาดยาเมื่อใดก็ได้ตั้งแต่การสุ่มไปจนถึง 1 ชั่วโมงหลังจากที่ผู้ป่วยออกจากห้องปฏิบัติการที่มีการสวนหัวใจ
ผู้ป่วยที่สุ่มรับยา prasugrel (ขนาดบรรจุ 60 มก. ตามด้วย 10 มก. วันละครั้ง) หรือ clopidogrel (ขนาดยา 300 มก. ตามด้วย 75 มก. วันละครั้ง) ได้รับการรักษาเป็นเวลามัธยฐาน 14.5 เดือน (สูงสุด 15 เดือนโดยมีค่าต่ำสุด ติดตามผล 6 เดือน) ผู้ป่วยยังได้รับ ASA (75 มก. ถึง 325 มก. วันละครั้ง)
การใช้ thienopyridine ในช่วง 5 วันก่อนการลงทะเบียนเป็นเกณฑ์การยกเว้น การรักษาอื่นๆ เช่น heparin และ GPIIb / IIIa inhibitors ได้รับการดูแลตามดุลยพินิจของแพทย์ ประมาณ 40% ของผู้ป่วย (ในแต่ละกลุ่มการรักษา) ได้รับ GPIIb / IIIa inhibitors เพื่อสนับสนุน PCI (ไม่มีข้อมูลเกี่ยวกับประเภทของ GP IIb / ใช้ตัวยับยั้ง IIIa) ผู้ป่วยประมาณ 98% (ในแต่ละกลุ่มการรักษา) ได้รับ antithrombins โดยตรง (heparin, heparin ที่มีน้ำหนักโมเลกุลต่ำ, bivalirudin หรือยาอื่น ๆ ) เพื่อสนับสนุน PCI
ตัวชี้วัดหลักของผลการศึกษาคือเวลาที่จะเกิดขึ้นของเหตุการณ์แรกของการเสียชีวิตจากโรคหัวใจและหลอดเลือด (CV) กล้ามเนื้อหัวใจตายที่ไม่ร้ายแรง (MI) หรือโรคหลอดเลือดสมองที่ไม่ร้ายแรง การวิเคราะห์เป้าหมายแบบผสมในกลุ่มประชากร ACS ทั้งหมด (รวมถึงกลุ่ม UA / NSTEMI และ STEMI) มีเงื่อนไขในการสาธิตความเหนือกว่าทางสถิติของ prasugrel เหนือ clopidogrel ในกลุ่ม UA / NSTEMI (p
ประชากรโดยรวมของ ACS: Efient แสดงให้เห็นถึงประสิทธิภาพที่เหนือกว่า clopidogrel ในการลดจุดยุติคอมโพสิตหลักและจุดยุติทุติยภูมิที่กำหนดไว้ล่วงหน้า ซึ่งรวมถึง stent thrombosis (ดูตารางที่ 3) ประโยชน์ของ Prasugrel ปรากฏชัดภายใน 3 วันแรกและดำเนินต่อไปจนถึงสิ้นสุดการศึกษา ประสิทธิภาพที่เหนือกว่ามาพร้อมกับการตกเลือดที่สำคัญเพิ่มขึ้น (ดูหัวข้อ 4.4 และ 4.8) ประชากรผู้ป่วยเป็นชาวคอเคเชียน 92% โดยเป็นผู้หญิง 26% และ 39% อายุ≥ 65 ปี ประโยชน์ที่เกี่ยวข้องกับ prasugrel นั้นไม่ขึ้นอยู่กับการใช้การรักษาโรคหัวใจและหลอดเลือดแบบเฉียบพลันและระยะยาวอื่น ๆ รวมถึงเฮปาริน / เฮปารินที่มีน้ำหนักโมเลกุลต่ำ, ไบวาลิรูดิน, สารยับยั้ง GPIIb / IIIa ทางหลอดเลือดดำ, ยาลดไขมัน, ตัวบล็อคเบต้าและสารยับยั้งเอนไซม์ที่ทำให้เกิด angiotensin ประสิทธิภาพของ prasugrel ไม่ขึ้นกับขนาดยา ASA (75-325 มก. วันละครั้ง) ไม่อนุญาตให้ใช้ยาต้านการแข็งตัวของเลือดในช่องปาก ยาต้านเกล็ดเลือดอื่น ๆ นอกเหนือจากที่อยู่ภายใต้การศึกษา และ NSAIDs เรื้อรังไม่ได้รับอนุญาตในการศึกษาของ TRITON ในประชากร ACS โดยรวม prasugrel มีความสัมพันธ์กับอัตราการเสียชีวิตของ CV ที่ลดลง ของ AMI ที่ไม่ร้ายแรง และ ของโรคหลอดเลือดสมองที่ไม่ร้ายแรงเมื่อเปรียบเทียบกับ clopidogrel โดยไม่คำนึงถึงลักษณะพื้นฐาน เช่น อายุ เพศ น้ำหนักตัว พื้นที่ทางภูมิศาสตร์ การใช้สารยับยั้ง GPIIb / IIIa และประเภทของ stent ประโยชน์ส่วนใหญ่เกิดจากการลดลงอย่างมีนัยสำคัญในที่ไม่เป็นอันตราย กรณีของ AMI (ดูตารางที่ 3) ผู้ป่วยโรคเบาหวานนำเสนอการลดลงอย่างมีนัยสำคัญในจุดยุติผสมปฐมภูมิและทุติยภูมิทั้งหมด
ประโยชน์ของ prasugrel ที่พบในผู้ป่วยที่อายุมากกว่า 75 ปีนั้นน้อยกว่าที่พบในผู้ป่วยโรคเบาหวาน STEMI ความเสี่ยงที่เพิ่มขึ้นของการเกิดลิ่มเลือดอุดตันในหลอดเลือดหรือเหตุการณ์ที่เกิดขึ้นอีก
ผู้ป่วยที่มีประวัติ TIA หรือมีประวัติการโจมตีขาดเลือดย้อนหลังไปมากกว่า 3 เดือนก่อนการรักษาด้วย prasugrel ไม่ได้มีเป้าหมายหลักที่ลดลง
ตารางที่ 3: ผู้ป่วยที่มีผลลัพธ์ทางคลินิกในการวิเคราะห์เบื้องต้นของการศึกษา TRITON
ในประชากร ACS โดยรวม การวิเคราะห์จุดยุติทุติยภูมิแต่ละจุดแสดงให้เห็นถึงประโยชน์ที่มีนัยสำคัญ (p
Prasugrel สัมพันธ์กับการลดการเกิดลิ่มเลือดในขดลวด 50% ในช่วงติดตามผล 15 เดือน การลดการเกิดลิ่มเลือดในสเตนท์ด้วย Efient นั้นพบได้ทั้งในระยะเริ่มต้นและเกิน 30 วันสำหรับทั้งขดลวดโลหะและยา
ในการวิเคราะห์ผู้ป่วยที่รอดชีวิตจากเหตุการณ์ขาดเลือด prasugrel มีความสัมพันธ์กับการลดอุบัติการณ์ของเหตุการณ์ปลายทางหลักที่ตามมา (7.8% กับ prasugrel เทียบกับ 11.9% กับ clopidogrel)
แม้ว่าการตกเลือดจะเพิ่มขึ้นด้วย prasugrel แต่ "การวิเคราะห์เป้าหมาย" แบบรวมประกอบด้วยการเสียชีวิตจากสาเหตุทั้งหมด กล้ามเนื้อหัวใจตายที่ไม่ร้ายแรง โรคหลอดเลือดสมองที่ไม่ร้ายแรง และเลือดออกที่สำคัญที่ไม่เกี่ยวกับ CABG ของ TIMI เป็นผลดีสำหรับ Efient เมื่อเทียบกับ clopidogrel (HR 0.87 ; 95% CI, 0.79 ถึง 0.95; p = 0.004) ในการศึกษาของ TRITON ในผู้ป่วยทุก 1, 000 รายที่รักษาด้วย Efient มีผู้ป่วยโรคกล้ามเนื้อหัวใจตายน้อยกว่า 22 รายและอีก 5 รายที่มีภาวะเลือดออกที่สำคัญที่ไม่เกี่ยวกับ CABG ของ TIMI เมื่อเทียบกับผู้ป่วยที่ได้รับ clopidogrel
ผลลัพธ์จากการศึกษาเภสัชพลศาสตร์/เภสัชพันธุศาสตร์ในผู้ป่วย ACS ในเอเชียจำนวน 720 รายที่ได้รับ PCI แสดงให้เห็นว่าสามารถยับยั้งเกล็ดเลือดในระดับที่สูงกว่าได้ด้วย prasugrel มากกว่าการใช้ clopidogrel และขนาดยา prasugrel 60 มก. / ปริมาณการบำรุงรักษา 10 มก. เป็นขนาดยาที่เหมาะสมในอาสาสมัครชาวเอเชียที่มีน้ำหนัก อย่างน้อย 60 กก. และอายุน้อยกว่า 75 ปี (ดูหัวข้อ 4.2)
ในการศึกษา 30 เดือน (TRILOGY-ACS) ดำเนินการในผู้ป่วยที่รักษาด้วย ACS UA / NSTEMI จำนวน 9326 ราย โดยไม่มีการปรับหลอดเลือดใหม่ (ข้อบ่งชี้ที่ไม่ได้ลงทะเบียน) prasugrel ไม่ได้ลดความถี่ของเป้าหมายการเสียชีวิตแบบผสมของ CV ของ MI หรือโรคหลอดเลือดสมองเมื่อเทียบกับ กับ clopidogrel อัตราเลือดออกมาก (TIMI) (รวมถึงความเสี่ยงต่อการเสียชีวิต เสียชีวิต และเลือดออกในกะโหลกศีรษะ) มีความคล้ายคลึงกันในผู้ป่วยที่ได้รับ prasugrel และ clopidogrel ≥ 75 ปีหรือมีน้ำหนักน้อยกว่า 60 กก. (N = 3022) สุ่มให้ prasugrel 5 มก. เช่นเดียวกับในผู้ป่วยสูงอายุ
05.2 คุณสมบัติทางเภสัชจลนศาสตร์
Prasugrel เป็น prodrug และได้รับการเผาผลาญอย่างรวดเร็ว ในร่างกาย กับสารออกฤทธิ์และสารที่ไม่ออกฤทธิ์ การได้รับเมตาโบไลต์แบบแอคทีฟ (AUC) มีความแปรปรวนระหว่างอาสาสมัครในระดับปานกลางถึงต่ำ (27%) และความแปรปรวนภายในกลุ่ม (19%) เภสัชจลนศาสตร์ของ prasugrel มีความคล้ายคลึงกันในคนที่มีสุขภาพดี ผู้ป่วยที่มีภาวะหลอดเลือดแข็งและผู้ป่วยที่ได้รับการแทรกแซงของหลอดเลือดหัวใจ
การดูดซึม
การดูดซึมและเมแทบอลิซึมของ prasugrel นั้นรวดเร็ว โดยความเข้มข้นสูงสุดของพลาสมาในพลาสมา (Cmax) ของสารออกฤทธิ์จะถึงในเวลาประมาณ 30 นาทีการสัมผัสกับสารออกฤทธิ์ (AUC) จะเพิ่มขึ้นตามสัดส่วนในช่วงขนาดยาที่ใช้ในการรักษา ในการศึกษาในคนที่มีสุขภาพดี AUC ของสารออกฤทธิ์ไม่ได้ถูกเปลี่ยนแปลงโดยอาหารที่มีไขมันสูงและมีแคลอรีสูง แต่ Cmax ลดลง 49% และเวลาที่จะไปถึง Cmax (Tmax) เพิ่มขึ้น 0.5 ถึง 1.5 ชั่วโมง ในการศึกษาของ TRITON ให้ Efient โดยไม่คำนึงถึงการบริโภคอาหาร ดังนั้น สามารถให้ Efient ได้โดยไม่คำนึงถึงอาหาร อย่างไรก็ตาม การให้ยา Prasugrel ในสภาวะที่อดอาหารอาจทำให้ออกฤทธิ์เร็วขึ้น (ดูหัวข้อ 4.2)
การกระจาย
เมแทบอไลต์ที่ออกฤทธิ์จับกับอัลบูมินในซีรัมของมนุษย์ (สารละลายบัฟเฟอร์ 4%) คือ 98%
เมแทบอลิซึม
Prasugrel ไม่ปรากฏในพลาสมาหลังการบริหารช่องปาก มันถูกไฮโดรไลซ์อย่างรวดเร็วในลำไส้เป็น thiolactone ซึ่งจะถูกแปลงเป็นสารออกฤทธิ์ในขั้นตอนการเผาผลาญเดียวโดย cytochrome P450 ส่วนใหญ่เป็น CYP3A4 และ CYP2B6 และในระดับที่น้อยกว่าโดย CYP2C9 และ CYP2C19 เมแทบอไลต์ที่ใช้งานจะถูกเผาผลาญเป็นสารประกอบสองชนิดในเวลาต่อมา . ไม่ทำงานโดย S-methylation หรือการผันคำกริยากับซิสเทอีน
ในคนที่มีสุขภาพดี ผู้ป่วยที่มีภาวะหลอดเลือดแข็งและผู้ป่วย ACS ที่ได้รับ Efient ไม่มีผลต่อการเปลี่ยนแปลงทางพันธุกรรมของ CYP3A5, CYP2B6, CYP2C9 หรือ CYP2C19 ต่อเภสัชจลนศาสตร์ของ prasugrel หรือการยับยั้งการรวมตัวของเกล็ดเลือด
การกำจัด
ประมาณ 68% ของขนาดยา prasugrel จะถูกกำจัดในปัสสาวะและ 27% ในอุจจาระเป็นสารที่ไม่ออกฤทธิ์ เมแทบอไลต์ที่ออกฤทธิ์มีครึ่งชีวิตในการกำจัดประมาณ 7.4 ชั่วโมง (2 ถึง 15 ชั่วโมง)
ประชากรเฉพาะ:
พลเมืองอาวุโส: ในการศึกษาในอาสาสมัครที่มีสุขภาพดีที่มีอายุระหว่าง 20 ถึง 80 ปี อายุไม่มีผลอย่างมีนัยสำคัญต่อเภสัชจลนศาสตร์ของ prasugrel หรือการยับยั้งการรวมตัวของเกล็ดเลือดที่เกิดขึ้น ใน "การทดลองทางคลินิกระยะที่ 3 ขนาดใหญ่" การได้รับสารออกฤทธิ์ (AUC) เพิ่มขึ้น 19% ในผู้ป่วยสูงอายุมาก (อายุ≥ 75 ปี) เมื่อเทียบกับผู้ที่มีอายุ
ควรใช้ Prasugrel ด้วยความระมัดระวังในผู้ป่วยที่อายุมากกว่า 75 ปี เนื่องจากอาจมีความเสี่ยงต่อการตกเลือดในประชากรกลุ่มนี้ (ดูหัวข้อ 4.2 และ 4.4) ในการศึกษาในอาสาสมัครที่มีภาวะหลอดเลือดแข็งตัว การได้รับสาร AUC เฉลี่ย (AUC) ต่อสารออกฤทธิ์ในผู้ป่วยที่อายุ≥ 75 ปีที่ได้รับ prasugrel 5 มก. นั้นประมาณครึ่งหนึ่งในผู้ป่วยที่อายุมากกว่า 75 ปี
ตับไม่เพียงพอ: ไม่จำเป็นต้องปรับขนาดยาสำหรับผู้ป่วยที่มีความบกพร่องของตับเล็กน้อยถึงปานกลาง (Child-Pugh class A หรือ B) เภสัชจลนศาสตร์ของ prasugrel และการยับยั้งการรวมตัวของเกล็ดเลือดมีความคล้ายคลึงกันในผู้ที่มีความบกพร่องทางตับในระดับเล็กน้อยถึงปานกลางเมื่อเปรียบเทียบกับคนที่มีสุขภาพดี ไม่ได้มีการศึกษาเภสัชจลนศาสตร์และเภสัชพลศาสตร์ของ prasugrel ในผู้ป่วยที่มีความบกพร่องทางตับอย่างรุนแรง ไม่ควรใช้ในผู้ป่วยที่มีอาการ การด้อยค่าของตับอย่างรุนแรง (ดูหัวข้อ 4. 3)
ไตล้มเหลว: ไม่จำเป็นต้องปรับขนาดยาสำหรับผู้ป่วยที่มีภาวะไตวาย ซึ่งรวมถึงผู้ป่วยที่เป็นโรคไตวายเรื้อรังระยะสุดท้าย (ESRD) เภสัชจลนศาสตร์ของ prasugrel และการยับยั้งการรวมตัวของเกล็ดเลือดมีความคล้ายคลึงกันในผู้ป่วยที่มีความบกพร่องทางไตในระดับปานกลาง (GFR) 30-2 และคนที่มีสุขภาพดี การยับยั้งการรวมตัวของเกล็ดเลือดด้วย prasugrel มีความคล้ายคลึงกัน นอกจากนี้ในผู้ป่วย ESRD ที่ต้องการการฟอกไต เมื่อเทียบกับคนที่มีสุขภาพดี แม้ว่า Cmax และ AUC ของสารออกฤทธิ์จะลดลง 51% และ 42% ตามลำดับในผู้ป่วย ESRD
น้ำหนักตัว: การได้รับสารที่ใช้งาน (AUC) ของ prasugrel สูงขึ้นประมาณ 30 ถึง 40% ในคนที่มีสุขภาพดีและผู้ป่วยที่มีน้ำหนักตัว
เชื้อชาติ: ในการศึกษาเภสัชวิทยาทางคลินิก หลังจากปรับน้ำหนักตัวแล้ว AUC ของสารออกฤทธิ์จะสูงขึ้นประมาณ 19% ในชาวจีน ญี่ปุ่น และเกาหลี เมื่อเทียบกับคนผิวขาว โดยส่วนใหญ่สัมพันธ์กับการได้รับสารในกลุ่มเอเชียที่มีน้ำหนักตัว
เพศ: ในคนที่มีสุขภาพดีและผู้ป่วย เภสัชจลนศาสตร์ของ prasugrel ในผู้หญิงและผู้ชายมีความคล้ายคลึงกัน
ประชากรเด็ก: เภสัชจลนศาสตร์และเภสัชพลศาสตร์ของ prasugrel ยังไม่ได้รับการประเมินในกลุ่มเด็ก (ดูหัวข้อ 4.2 )
05.3 ข้อมูลความปลอดภัยพรีคลินิก
ข้อมูลที่ไม่ใช่ทางคลินิกเผยให้เห็นว่าไม่มีอันตรายเป็นพิเศษสำหรับมนุษย์จากการศึกษาทั่วไปของเภสัชวิทยาด้านความปลอดภัย ความเป็นพิษของยาซ้ำ ความเป็นพิษต่อพันธุกรรม ศักยภาพในการก่อมะเร็ง หรือความเป็นพิษต่อการสืบพันธุ์ สังเกตผลในการศึกษาที่ไม่ใช่ทางคลินิก เฉพาะเมื่อได้รับสารที่พิจารณาว่าเพียงพอแล้วมากกว่า การสัมผัสสูงสุดของมนุษย์บ่งชี้ว่ามีความเกี่ยวข้องต่ำสำหรับการใช้งานทางคลินิก
การศึกษาทางพิษวิทยาเกี่ยวกับพัฒนาการของตัวอ่อนและทารกในครรภ์ในหนูและกระต่ายไม่พบหลักฐานของความผิดปกติที่เกิดจากพราซูเกรล ในปริมาณที่สูงมาก (> 240 เท่าของปริมาณที่แนะนำสำหรับการบำรุงรักษาของมนุษย์ต่อวันในหน่วยมก. / ตร.ม. ) ที่ส่งผลต่อน้ำหนักตัวของมารดาและ / หรือการบริโภคอาหาร ทำให้ลูกหลานมีน้ำหนักตัวลดลงเล็กน้อย (เมื่อเทียบกับกลุ่มควบคุม) ใน การศึกษาก่อนและหลังคลอดในหนู การรักษามารดาไม่มีผลต่อการพัฒนาพฤติกรรมหรือการสืบพันธุ์ของลูกหลานในปริมาณที่สูงถึง 240 เท่าของปริมาณที่แนะนำต่อวันของมนุษย์ (แสดงเป็นมิลลิกรัมต่อตารางเมตร)
ไม่พบเนื้องอกที่เกี่ยวข้องกับสารประกอบในการศึกษา 2 ปีในหนูที่ได้รับ prasugrel ตั้งแต่มากกว่า 75 เท่าของการสัมผัสการรักษาของมนุษย์ที่แนะนำ ในหนูที่ได้รับยาในปริมาณสูงเป็นเวลา 2 ปี (> 75 เท่าของการสัมผัสของมนุษย์) มี "อุบัติการณ์ของเนื้องอกที่เพิ่มขึ้น (adenomas เซลล์ตับ) แต่ถือว่ารองจากการเหนี่ยวนำของเอนไซม์ prasugrel" L "การเชื่อมโยงเฉพาะของหนูของตับ เนื้องอกและการเหนี่ยวนำของเอนไซม์ที่เกิดจากยาได้รับการบันทึกไว้อย่างดีในวรรณกรรม การเพิ่มขึ้นของเนื้องอกในตับด้วยการบริหาร prasugrel ในหนูไม่ถือเป็นความเสี่ยงที่เกี่ยวข้องกับมนุษย์
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
แกนหลักของแท็บเล็ต:
ไมโครคริสตัลลีน เซลลูโลส
แมนนิทอล (E421)
ครอสคาร์เมลโลสโซเดียม
ไฮโปรเมลโลส (E464)
แมกนีเซียมสเตียเรต
การเคลือบผิว:
แลคโตสโมโนไฮเดรต
ไฮโปรเมลโลส (E464)
ไทเทเนียมไดออกไซด์ (E171)
ไตรอะซิติน (E1518)
เหล็กออกไซด์แดง (E172)
เหล็กออกไซด์สีเหลือง (E172)
แป้ง
6.2 ความไม่ลงรอยกัน
ไม่สามารถใช้ได้.
06.2 ความเข้ากันไม่ได้
2 ปี.
06.3 ระยะเวลาที่ใช้ได้
2 ปี.
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
ยานี้ไม่ต้องการอุณหภูมิในการเก็บรักษาเป็นพิเศษ เก็บในบรรจุภัณฑ์เดิมเพื่อป้องกันอากาศและความชื้น
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
กล่องอลูมิเนียมพองขนาด 14, 28, 30, 30 (x1), 56, 84, 90 (x1) และ 98 เม็ด
ขนาดของบรรจุภัณฑ์อาจไม่สามารถวางตลาดได้ทั้งหมด
06.6 คำแนะนำในการใช้งานและการจัดการ
ไม่มีคำแนะนำพิเศษ
07.0 ผู้ทรงอำนาจการตลาด
Eli Lilly Nederland BV, Grootslag 1-5, NL-3991 RA Houten, เนเธอร์แลนด์
08.0 หมายเลขอนุญาตการตลาด
EU / 1/08/503/008
039055088
EU / 1/08/503/009
039055090
EU / 1/08/503/010
039055102
EU / 1/08/503/011
039055114
สหภาพยุโรป / 1/08/503/012
039055126
EU / 1/08/503/013
039055138
EU / 1/08/503/014
039055140
EU / 1/08/503/016
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
วันที่ได้รับอนุญาตครั้งแรก: 25 กุมภาพันธ์ 2009
วันที่ต่ออายุล่าสุด:
10.0 วันที่แก้ไขข้อความ
11.0 สำหรับยาวิทยุ กรอกข้อมูลเกี่ยวกับปริมาณรังสีภายในให้ครบถ้วน
12.0 สำหรับยาวิทยุ คำแนะนำเพิ่มเติมโดยละเอียดเกี่ยวกับการเตรียมที่เป็นแบบอย่างและการควบคุมคุณภาพ
ตกลงกับหน่วยงานด้านการแพทย์แห่งยุโรป (EMA) และหน่วยงานด้านยาของอิตาลี (AIFA)
ธันวาคม 2556
เพิ่มความเสี่ยงของการมีเลือดออกรุนแรงในผู้ป่วยที่เป็นโรคหลอดเลือดหัวใจตีบที่ไม่เสถียร / กล้ามเนื้อหัวใจตายระดับ non-ST-segment (UA) / NSTEMI เมื่อใช้ EFIENT (prasugrel) ก่อนการตรวจวินิจฉัยหลอดเลือดหัวใจตีบ
คุณหมอที่รัก คุณหมอที่รัก
"European Medicines Agency and the Italian Medicines Agency - AIFA ตามข้อตกลงกับ Daiichi-Sankyo และ Eli Lilly Italia ต้องการแจ้งให้คุณทราบเกี่ยวกับคำแนะนำต่อไปนี้เกี่ยวกับการใช้ EFIENT (prasugrel) ซึ่งเป็นยาต้านเกล็ดเลือดที่ระบุไว้สำหรับการรักษาภาวะเฉียบพลัน โรคหลอดเลือดหัวใจ (ACS) ในผู้ป่วยที่ได้รับการแทรกแซงหลอดเลือดผ่านผิวหนัง (PCI):
ในผู้ป่วยที่เป็นโรคหลอดเลือดหัวใจตีบที่ไม่เสถียร / กล้ามเนื้อหัวใจตายส่วนสูงที่ไม่ใช่ ST (UA) / NSTEMI เมื่อทำการตรวจหลอดเลือดหัวใจภายใน 48 ชั่วโมงของการรักษาในโรงพยาบาล ควรให้ขนาดยา EFIENT ในเวลาที่ทำ PCI เพื่อลดความเสี่ยง ของการมีเลือดออก
คำแนะนำนี้อิงจากผลการศึกษาทางคลินิกที่เพิ่งเสร็จสิ้นไปในผู้ป่วย NSTEMI ซึ่งกำหนดให้เข้ารับการตรวจหลอดเลือดหัวใจ 2 ถึง 48 ชั่วโมงหลังจากการสุ่มตัวอย่าง การศึกษาเปรียบเทียบผลของการให้ยา prasugrel เริ่มต้น 30 มก. ก่อนการตรวจหลอดเลือดหัวใจ (โดยเฉลี่ย 4 ชั่วโมง) ตามด้วย "ขนาดยาเพิ่มเติม 30 มก. ในช่วงเวลาของ PCI โดยมีผลมาจากการให้ยาเต็มรูปแบบ ขนาดบรรจุ 60 มก. ในเวลาที่ทำ PCI ผลการศึกษาพบว่ามีความเสี่ยงที่จะมีเลือดออกมากขึ้นซึ่งสัมพันธ์กับการใช้ขนาดยาเริ่มต้นก่อนการทำหลอดเลือดหัวใจตีบตามด้วยการให้ยาเพิ่มเติมในเวลาที่ทำ PCI เมื่อเทียบกับการให้ยา prasugrel เพียงครั้งเดียวในช่วงเวลาที่ทำ PCI ไม่มีความแตกต่างในด้านประสิทธิภาพ สังเกตได้ระหว่างสูตรการให้ยาทั้งสองแบบ
การศึกษา "ACCOST" มีชื่อว่า: การเปรียบเทียบ Prasugrel ในช่วงเวลาของการแทรกแซงหลอดเลือดหัวใจหรือเป็นการรักษาก่อนในช่วงเวลาของการวินิจฉัยในผู้ป่วยที่มีภาวะกล้ามเนื้อหัวใจตายที่ไม่ใช่ระดับ ST
เรียนรู้เพิ่มเติมเกี่ยวกับประเด็นด้านความปลอดภัย
ACCOAST เป็นการศึกษา 30 วันที่ดำเนินการในผู้ป่วย 4,033 รายที่มี NSTEMI และ troponin ที่ยกระดับซึ่งถูกกำหนดให้รับการตรวจหลอดเลือดหัวใจตามด้วย PCI 2 ถึง 48 ชั่วโมงหลังจากการสุ่ม ผู้ที่ได้รับยา Prasugrel ขนาด 30 มก. โดยเฉลี่ย 4 ชั่วโมงก่อนการตรวจหลอดเลือดหัวใจ ตามด้วยขนาด 30 มก. ในขณะที่ทำ PCI (n = 2037) มีความเสี่ยงต่อการตกเลือดระหว่างขั้นตอนมากขึ้น (ไม่เกี่ยวข้องกับการผ่าตัดบายพาสหลอดเลือดหัวใจ) และไม่มีประโยชน์เพิ่มเติมเมื่อเปรียบเทียบกับผู้ป่วยที่ได้รับขนาดยา 60 มก. ในขณะที่ทำ PCI (n = 1996) โดยเฉพาะอย่างยิ่ง ความถี่ของเป้าหมายรวมของการเสียชีวิตจากโรคหัวใจและหลอดเลือด กล้ามเนื้อหัวใจตาย โรคหลอดเลือดสมอง หลอดเลือดแดงโดยด่วน หรือการใช้ตัวยับยั้งไกลโคโปรตีน (GP) IIb / IIIa "ในการบำบัดด้วยการประกันตัว" ภายใน 7 วันหลังจากการสุ่มตัวอย่างไม่ลดลงอย่างมีนัยสำคัญ ที่ได้รับ prasugrel ก่อนทำ angiography หลอดเลือดหัวใจ เปรียบเทียบกับผู้ป่วยที่ได้รับ prasugrel ขนาดเต็มในขณะที่ทำ PCI นอกจากนี้ ความถี่ของวัตถุประสงค์ด้านความปลอดภัยหลัก ซึ่งมีเลือดออกที่สำคัญทั้งหมดตาม TIMI (CABG และเหตุการณ์ที่ไม่ใช่ CABG) ภายใน 7 วันหลังจากการสุ่มตัวอย่างในทุกวิชาที่ได้รับการรักษา สูงขึ้นอย่างมีนัยสำคัญในผู้ที่ได้รับ prasugrel ในสองโดส (4 ชั่วโมงก่อนการทำหลอดเลือดหัวใจตีบและในเวลาที่ทำ PCI) เทียบกับผู้ป่วยที่ได้รับยา Prasugrel ขนาดเต็มในการให้ยาครั้งเดียวในขณะที่ทำ PCI
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
แพทย์และบุคลากรทางการแพทย์อื่น ๆ จะต้องรายงานอาการข้างเคียงที่น่าสงสัยที่เกี่ยวข้องกับยาที่มี prasugrel
ตามกฎหมายแล้ว แพทย์และผู้เชี่ยวชาญด้านสุขภาพต้องส่งรายงานอาการไม่พึงประสงค์ที่น่าสงสัย โดยใช้แบบฟอร์มกระดาษพิเศษ (มีอยู่ในเว็บไซต์ http://www.agenziafarmaco.gov.it/sites/default/files/tipo_filecb84.pdf) หรือโดยการกรอกแบบฟอร์มอิเล็กทรอนิกส์ทางออนไลน์ (http://www.agenziafarmaco.gov.it/sites/default/files/scheda_aifa_oper_sanitario16.07.2 012.doc) ทันที ต่อผู้จัดการด้านเภสัชภัณฑ์ของสถานพยาบาลที่พวกเขาสังกัดหรือ หากดำเนินการในสถานบริการสุขภาพเอกชน ผ่านกรมอนามัย ให้ผู้จัดการดูแลยาของ ASL ที่มีอำนาจสำหรับพื้นที่นั้น
ข้อมูลเพิ่มเติม
สำหรับคำถามและ/หรือข้อมูลเพิ่มเติม โปรดติดต่อสำนักงาน "ข้อมูลทางการแพทย์" ของ Eli Lilly โดยโทรไปที่หมายเลขโทรฟรีต่อไปนี้: 800117678 หรือเขียนถึงที่อยู่ต่อไปนี้: [email protected]
ต้องส่งรายงานอาการไม่พึงประสงค์ที่น่าสงสัยจากยาไปยังหัวหน้าแผนกควบคุมยาของโครงสร้างที่ผู้ปฏิบัติงานอยู่
หมายเหตุข้อมูลนี้ยังเผยแพร่บนเว็บไซต์ AIFA (www.agenziafarmaco.it) ซึ่งแนะนำให้ปรึกษาอย่างสม่ำเสมอสำหรับข้อมูลด้านอาชีพและการบริการที่ดีที่สุดแก่พลเมือง