สารออกฤทธิ์: Degarelix
FIRMAGON 80 มก. ผงและตัวทำละลายสำหรับสารละลายสำหรับฉีด
เม็ดมีดแพ็คเกจ Firmagon มีจำหน่ายสำหรับขนาดบรรจุภัณฑ์:- FIRMAGON 80 มก. ผงและตัวทำละลายสำหรับสารละลายสำหรับฉีด
- FIRMAGON 120 มก. ผงและตัวทำละลายสำหรับสารละลายสำหรับฉีด
ทำไมถึงใช้ Firmagon? มีไว้เพื่ออะไร?
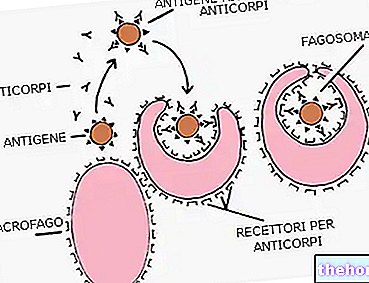
FIRMAGON มีสารเดกาเรลิกซ์ Degarelix เป็นตัวบล็อกฮอร์โมนสังเคราะห์ทางเคมีที่ใช้ในการรักษามะเร็งต่อมลูกหมากในผู้ป่วยชายที่เป็นผู้ใหญ่ Degarelix เลียนแบบฮอร์โมนธรรมชาติ (gonadotropin ปล่อยฮอร์โมน GnRH) และบล็อกผลกระทบของมันโดยตรง ด้วยการทำเช่นนี้ degarelix จะลดระดับฮอร์โมนเพศชายฮอร์โมนเพศชายซึ่งกระตุ้นมะเร็งต่อมลูกหมากทันที
ข้อห้าม เมื่อไม่ควรใช้ Firmagon
อย่าใช้ FIRMAGON - หากคุณแพ้ degarelix หรือส่วนผสมอื่น ๆ ของยานี้
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนใช้ Firmagon
บอกแพทย์หากคุณมีอาการดังต่อไปนี้:
- คุณมีปัญหาเกี่ยวกับจังหวะการเต้นของหัวใจหรือหัวใจ (arrhythmia) หรือกำลังใช้ยาเพื่อรักษาปัญหานี้ ปัญหาจังหวะการเต้นของหัวใจอาจรุนแรงขึ้นได้ด้วยการใช้ FIRMAGON
- คุณป่วยเป็นโรคเบาหวาน อาจเลวลงหรือเริ่มเป็นเบาหวานได้ หากคุณเป็นเบาหวาน คุณต้องตรวจระดับน้ำตาลในเลือดให้บ่อยขึ้น
- ทุกข์ทรมานจากปัญหาตับ คุณอาจต้องตรวจสอบการทำงานของตับ
- คุณเป็นโรคไต ยังไม่มีการศึกษาการใช้ FIRMAGON ในผู้ป่วยโรคไตอย่างรุนแรง
- คุณเป็นโรคกระดูกพรุนหรืออาการอื่นๆ ที่ส่งผลต่อความแข็งแรงของกระดูก ระดับฮอร์โมนเทสโทสเตอโรนที่ลดลงอาจทำให้แคลเซียมในกระดูกลดลง (ทำให้กระดูกบางลง)
- ทนทุกข์ทรมานจากอาการแพ้อย่างรุนแรง ยังไม่มีการศึกษาการใช้ FIRMAGON ในผู้ป่วยที่มีปฏิกิริยาภูมิไวเกินอย่างรุนแรง
เด็กและวัยรุ่น
อย่าให้ยานี้แก่เด็กหรือวัยรุ่น
ปฏิกิริยา ยาหรืออาหารชนิดใดที่สามารถปรับเปลี่ยนผลของ Firmagon
FIRMAGON อาจรบกวนยาบางชนิดที่ใช้สำหรับปัญหาจังหวะการเต้นของหัวใจ (เช่น quinidine, procainamide, amiodarone และ sotalol) หรือยาอื่นๆ ที่อาจส่งผลต่อจังหวะการเต้นของหัวใจ (เช่น เมทาโดน (ใช้สำหรับบรรเทาอาการปวดและเป็นส่วนหนึ่งของการรักษาดีท็อกซ์การติดยา) ม็อกซิฟลอกซาซิน ( ยาปฏิชีวนะ) ยารักษาโรคจิต)
แจ้งให้แพทย์ทราบหากคุณกำลังรับประทานหรือเพิ่งรับประทานยาหรืออาจใช้ยาอื่น ๆ รวมทั้งยาที่ได้รับโดยไม่มีใบสั่งยา
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
สำหรับผู้ที่ทำกิจกรรมกีฬา
การใช้ยาโดยไม่จำเป็นต้องมีการรักษาถือเป็นการให้ยาสลบ และสามารถระบุการทดสอบการต่อต้านยาสลบในเชิงบวกไม่ว่ากรณีใดๆ
การขับรถและการใช้เครื่องจักร
อาการเหนื่อยล้าและเวียนศีรษะเป็นผลข้างเคียงที่พบได้บ่อยที่อาจส่งผลต่อความสามารถในการขับขี่และการใช้เครื่องจักร ผลกระทบเหล่านี้อาจเกิดจากการรักษาหรือตัวโรคเอง
ปริมาณ วิธีการ และระยะเวลาในการบริหาร วิธีใช้ Firmagon: Posology
ยานี้มักจะต้องได้รับการบริหารโดยแพทย์หรือพยาบาล
ปริมาณเริ่มต้นที่แนะนำคือการฉีด 120 มก. สองครั้งติดต่อกัน จากนั้นคุณจะได้รับการฉีด 80 มก. ต่อเดือน ของเหลวที่ฉีดจะสร้างเจลซึ่งปล่อยสารดีกาเรลิกส์ออกมาในช่วงหนึ่งเดือน
FIRMAGON ควรฉีดเข้าใต้ผิวหนังเท่านั้น (ใต้ผิวหนัง) ห้ามฉีด FIRMAGON เข้าไปในเส้นเลือด (ทางหลอดเลือดดำ) ควรใช้ข้อควรระวังเพื่อหลีกเลี่ยงการฉีดเข้าเส้นเลือดโดยไม่ได้ตั้งใจ จุดฉีดจะต้องเปลี่ยนแปลงภายในบริเวณช่องท้อง
หากคุณลืมใช้ FIRMAGON
หากคุณคิดว่าคุณลืมยา FIRMAGON รายเดือน โปรดแจ้งให้แพทย์ทราบ หากคุณมีคำถามเพิ่มเติมเกี่ยวกับการใช้ยานี้ ให้ปรึกษาแพทย์ของคุณ
คำแนะนำสำหรับการใช้งานที่เหมาะสม
บันทึก:
อย่าเขย่าขวด
ชุดประกอบด้วยขวดผงและเข็มฉีดยาตัวทำละลายที่เติมไว้ล่วงหน้าซึ่งต้องเตรียมสำหรับการฉีดใต้ผิวหนัง
- ถอดฝาครอบออกจากแพ็คเกจ vial adapter แนบ adapter กับขวด powder โดยกดลงจนปลายผ่านจุกยางและอะแดปเตอร์คลิกเข้าที่
- เตรียมกระบอกฉีดยาที่เติมไว้ล่วงหน้าโดยใส่ลูกสูบ
- ถอดฝากระบอกฉีดยาที่บรรจุไว้ล่วงหน้าออก แนบกระบอกฉีดยาเข้ากับขวดผงโดยขันสกรูเข้ากับอะแดปเตอร์ โอนตัวทำละลายทั้งหมดไปยังขวดผง
- ใส่กระบอกฉีดยาลงในอะแดปเตอร์หมุนเบา ๆ จนของเหลวใสและปราศจากอนุภาคหรือผงที่ไม่ละลายน้ำหากผงยึดติดกับขวดที่อยู่เหนือพื้นผิวของของเหลวขวดสามารถเอียงเล็กน้อยได้ เขย่าเพื่อป้องกันไม่ให้เกิดฟอง สามารถใช้วงแหวนฟองอากาศขนาดเล็กบนพื้นผิวของเหลวได้ ขั้นตอนการคืนสภาพมักจะใช้เวลาสองสามนาที แต่ในบางกรณีอาจใช้เวลานานถึง 15 นาที
- พลิกขวดคว่ำลงแล้วลากขึ้นไปที่เส้นการทำเครื่องหมายของเข็มฉีดยา ตรวจสอบให้แน่ใจเสมอว่าได้ดูดปริมาตรที่แน่นอนและปรับให้เข้ากับฟองอากาศ
- ถอดกระบอกฉีดยาออกจากอะแดปเตอร์และสอดเข็มฉีดยาใต้ผิวหนังลึกเข้าไปในกระบอกฉีดยา
- ให้ฉีดเข้าใต้ผิวหนังลึก. เมื่อต้องการทำเช่นนี้: จับผิวหนังของช่องท้อง ยกเนื้อเยื่อใต้ผิวหนัง และสอดเข็มเข้าไปลึก ๆ ที่มุมไม่น้อยกว่า 45 องศา ฉีด FIRMAGON 80 มก. ช้าๆ 4 มล. ทันทีหลังทำใหม่ *
- ไม่ควรฉีดยาในบริเวณที่ผู้ป่วยอาจได้รับแรงกด เช่น ในบริเวณสายพาน ที่มีแถบรัดหรือใกล้ซี่โครง ห้ามฉีดเข้าเส้นเลือดโดยตรง ค่อย ๆ ดึงลูกสูบกระบอกฉีดกลับเพื่อตรวจดูว่าเลือดถูกดูดเข้าไปหรือไม่ หากมีเลือดอยู่ในหลอดฉีดยา จะต้องใช้ยานี้อีกต่อไป หยุดขั้นตอนและทิ้งเข็มฉีดยาและเข็ม (เตรียมยาใหม่สำหรับผู้ป่วย)
* แสดงให้เห็นถึงความเสถียรทางเคมีและกายภาพระหว่างการใช้งานเป็นเวลา 2 ชั่วโมงที่ 25 ° C จากมุมมองทางจุลชีววิทยา ควรใช้ผลิตภัณฑ์ทันทีเว้นแต่วิธีการคืนสภาพไม่รวมความเสี่ยงของการปนเปื้อนของแบคทีเรีย หากไม่ได้ใช้ทันที เวลาและเงื่อนไขการใช้งานถือเป็นความรับผิดชอบของผู้ใช้
ผลข้างเคียง ผลข้างเคียงของ Firmagon คืออะไร?
เช่นเดียวกับยาอื่นๆ ยานี้อาจทำให้เกิดผลข้างเคียงได้ แม้ว่าจะไม่ใช่ทุกคนที่ได้รับก็ตาม
อาการแพ้อย่างรุนแรงต่อยานี้หาได้ยาก ติดต่อแพทย์ของคุณโดยด่วนถ้าคุณมีผื่นรุนแรง คัน หรือหายใจลำบากหรือลำบาก อาการเหล่านี้อาจเป็นอาการแพ้อย่างรุนแรง
พบบ่อยมาก (อาจส่งผลกระทบมากกว่า 1 ใน 10 ผู้ใช้)
หน้าแดง ปวดและแดงบริเวณที่ฉีด ผลข้างเคียงที่บริเวณที่ฉีดพบได้บ่อยในขนาดเริ่มต้นและพบได้น้อยกับขนาดยาบำรุงรักษา
ทั่วไป (อาจส่งผลกระทบถึง 1 ใน 10 ผู้ใช้)
- บวม ก้อน และแข็งตัวที่บริเวณที่ฉีด
- หนาวสั่น มีไข้ หรืออาการคล้ายไข้หวัดใหญ่หลังฉีด
- รบกวนการนอนหลับ, อ่อนเพลีย, เวียนศีรษะ, ปวดหัว
- น้ำหนักขึ้น คลื่นไส้ ท้องเสีย เอนไซม์ตับบางชนิดสูง
- เหงื่อออกมากเกินไป (รวมถึงเหงื่อออกตอนกลางคืน) ผื่น
- โรคโลหิตจาง
- ปวดและความผิดปกติของกล้ามเนื้อและกระดูก
- ลดปริมาณอัณฑะ, เต้านมบวม, ความอ่อนแอ
ผิดปกติ (อาจส่งผลกระทบถึง 1 ใน 100 ผู้ใช้)
- สูญเสียความต้องการทางเพศ, ปวดอัณฑะ, ปวดกระดูกเชิงกราน, หลั่งล้มเหลว, ระคายเคืองที่อวัยวะเพศ, เจ็บเต้านม
- ภาวะซึมเศร้า, การเปลี่ยนแปลงทางจิต
- ผิวแดง, ผมร่วง, ก้อนผิว, ชา
- อาการแพ้ ลมพิษ อาการคัน
- ความอยากอาหารลดลง, ท้องผูก, อาเจียน, ปากแห้ง, ปวดท้องและไม่สบาย, น้ำตาลในเลือดเพิ่มขึ้น / เบาหวาน, คอเลสเตอรอลเพิ่มขึ้น, แคลเซียมในเลือดเปลี่ยนแปลง, น้ำหนักลดลง
- ความดันโลหิตเพิ่มขึ้น, การเปลี่ยนแปลงของจังหวะการเต้นของหัวใจ, การเปลี่ยนแปลงของ ECG (การยืด QT), ความรู้สึกของการเต้นของหัวใจผิดปกติ, หายใจลำบาก, อาการบวมน้ำที่ส่วนปลาย
- กล้ามเนื้ออ่อนแรง, กล้ามเนื้อกระตุก, ข้อต่อบวม / ตึง, โรคกระดูกพรุน / ภาวะกระดูกพรุน, ปวดข้อ
- ปัสสาวะบ่อย กระตุ้นให้ปัสสาวะ ปัสสาวะลำบากหรือปวด ปัสสาวะตอนกลางคืน ไตบกพร่อง กลั้นปัสสาวะไม่อยู่
- มองเห็นภาพซ้อน
- ความรู้สึกไม่สบายที่บริเวณที่ฉีดรวมถึงความดันโลหิตลดลงและอัตราการเต้นของหัวใจ (ปฏิกิริยา vasovagal)
- ไม่สบาย
หายาก (อาจส่งผลกระทบมากถึง 1 ใน 1,000 ผู้ใช้)
- Febrile neutropenia (จำนวนเม็ดเลือดขาวต่ำมากร่วมกับไข้) หัวใจวาย หัวใจล้มเหลว
หายากมาก (อาจส่งผลกระทบมากถึง 1 ใน 10,000 ผู้ใช้)
- การติดเชื้อ ฝี และเนื้อร้ายบริเวณที่ฉีด
การรายงานผลข้างเคียง
หากคุณได้รับผลข้างเคียงใดๆ ให้ปรึกษาแพทย์ ซึ่งรวมถึงผลข้างเคียงที่อาจเกิดขึ้นซึ่งไม่ได้ระบุไว้ในเอกสารฉบับนี้ คุณสามารถรายงานผลข้างเคียงได้โดยตรงผ่านระบบการรายงานระดับประเทศ
โดยการรายงานผลข้างเคียง คุณสามารถช่วยให้ข้อมูลเพิ่มเติมเกี่ยวกับความปลอดภัยของยานี้ได้
การหมดอายุและการเก็บรักษา
เก็บยานี้ให้พ้นสายตาและมือเด็ก
ห้ามใช้ยานี้หลังจากวันหมดอายุซึ่งระบุไว้ในขวด กระบอกฉีดยา และกล่องบรรจุ วันหมดอายุหมายถึงวันสุดท้ายของเดือนนั้น
ยานี้ไม่ต้องการข้อควรระวังในการเก็บรักษาเป็นพิเศษ
หลังจากสร้างใหม่
ยานี้มีความเสถียร 2 ชั่วโมงที่อุณหภูมิ 25 องศาเซลเซียส
เนื่องจากเสี่ยงต่อการปนเปื้อนของจุลินทรีย์ จึงควรใช้ยานี้ทันที หากไม่ได้ใช้ทันที การใช้ยานี้เป็นความรับผิดชอบของผู้ใช้
ห้ามทิ้งยาลงในน้ำเสียหรือของเสียในครัวเรือน ถามเภสัชกรว่าจะทิ้งยาที่ไม่ได้ใช้แล้วอย่างไร ซึ่งจะช่วยปกป้องสิ่งแวดล้อม
ข้อมูลอื่น ๆ
FIRMAGON ประกอบด้วยอะไรบ้าง
- สารออกฤทธิ์คือเดกาเรลิกซ์ ขวดแต่ละขวดประกอบด้วย degarelix 80 มก. (ในรูปของอะซิเตท) หลังจากคืนสภาพแล้ว 1 มล. ของสารละลายที่สร้างขึ้นใหม่ประกอบด้วย degarelix . 20 มก
- ส่วนประกอบอื่นๆ ในผงคือแมนนิทอล (E421)
- ตัวทำละลายคือน้ำสำหรับฉีด
กล่อง FIRMAGON มีลักษณะอย่างไรและมีอะไรบ้าง
FIRMAGON เป็นผงและตัวทำละลายสำหรับสารละลายสำหรับฉีด แป้งมีลักษณะเป็นสีขาวถึงขาว ตัวทำละลายเป็นสารละลายใสไม่มีสี
FIRMAGON มีจำหน่ายในสองชุด
แพ็ค 1 ถาดประกอบด้วย: ผง 1 ขวดบรรจุเดอกาเรลิกซ์ 80 มก. และเข็มฉีดยาที่เติมไว้ล่วงหน้า 1 อันที่มีตัวทำละลาย 4.2 มล. ลูกสูบ 1 อัน อะแดปเตอร์ 1 ขวดและเข็มฉีดยา 1 เข็ม
ถาด 3 ถาดประกอบด้วย: ผง 3 ขวดที่มีเดกาเรลิกซ์ 80 มก. และเข็มฉีดยาที่เติมไว้ล่วงหน้า 3 อันที่มีตัวทำละลาย 4.2 มล. ลูกสูบ 3 อัน อะแดปเตอร์ขวด 3 อัน และเข็มฉีดยา 3 อัน
แพ็คทั้งหมดอาจไม่ขาย
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่แสดงอาจไม่ทันสมัย
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
FIRMAGON 80 มก. ผงและตัวทำละลายสำหรับสารละลายแบบฉีด
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
ขวดแต่ละขวดมี degarelix 80 มก. (ในรูปแบบอะซิเตท)
หลังจากคืนสภาพแล้ว สารละลายแต่ละมล.จะมีดีแกเรลิกซ์ 20 มก.
สำหรับรายการสารปรุงแต่งทั้งหมด ดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
ผงและตัวทำละลายสำหรับสารละลายสำหรับฉีด
ผง: ผงสีขาวถึงผงสีขาว
ตัวทำละลาย: สารละลายใสไม่มีสี
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
FIRMAGON เป็นสารต้านการปลดปล่อยฮอร์โมน gonadotropin (GnRH) ที่ระบุไว้สำหรับการรักษาผู้ป่วยชายที่เป็นผู้ใหญ่ที่เป็นมะเร็งต่อมลูกหมากที่ขึ้นกับฮอร์โมนขั้นสูง
04.2 วิทยาและวิธีการบริหาร
ปริมาณ
ควรให้ยาบำรุงครั้งแรกหนึ่งเดือนหลังจากให้ยาเริ่มแรก
ผลการรักษาของ degarelix ควรได้รับการตรวจสอบโดยใช้พารามิเตอร์ทางคลินิกและระดับแอนติเจนที่จำเพาะต่อมลูกหมาก (PSA) ในซีรัม การศึกษาทางคลินิกแสดงให้เห็นว่าการปราบปรามระดับฮอร์โมนเทสโทสเตอโรน (T) เกิดขึ้นทันทีหลังจากให้ยาเริ่มแรก โดยมีระดับฮอร์โมนเทสโทสเตอโรนในซีรัมที่สอดคล้องกับระดับของการตัดอัณฑะในทางการแพทย์ (Ttestosterone (T)
ในกรณีของผู้ป่วยที่มีการตอบสนองที่ต่ำกว่าปกติ จะต้องได้รับการยืนยันว่าระดับฮอร์โมนเทสโทสเตอโรนในซีรัมยังคงถูกระงับอย่างเพียงพอ
เนื่องจาก degarelix ไม่กระตุ้นให้ฮอร์โมนเทสโทสเตอโรนเพิ่มขึ้น จึงไม่จำเป็นต้องรวมแอนโดรเจนเพื่อป้องกันการเพิ่มขึ้นในช่วงเริ่มต้นของการรักษา
ประชากรพิเศษ
ผู้สูงอายุ ผู้ป่วยตับหรือไตบกพร่อง:
ไม่จำเป็นต้องปรับขนาดยาในผู้สูงอายุหรือในผู้ป่วยที่มีความบกพร่องทางตับหรือไตเล็กน้อยถึงปานกลาง (ดูหัวข้อ 5.2) ไม่มีการศึกษาในผู้ป่วยที่มีความบกพร่องทางตับหรือไตอย่างรุนแรง ดังนั้นจึงแนะนำให้ใช้ความระมัดระวังในการรักษา (ดูหัวข้อ 4.4)
ประชากรเด็ก
ไม่มีการใช้ FIRMAGON เฉพาะในเด็กและวัยรุ่นในการรักษาผู้ใหญ่ชายที่เป็นมะเร็งต่อมลูกหมากที่ขึ้นกับฮอร์โมน
วิธีการบริหาร
ต้องสร้าง FIRMAGON ขึ้นใหม่ก่อนการบริหาร ดูหัวข้อ 6.6 สำหรับคำแนะนำในการสร้างใหม่และการบริหาร
FIRMAGON ใช้สำหรับฉีดเข้าใต้ผิวหนังเท่านั้น ห้ามฉีดเข้าเส้นเลือดดำ
ไม่แนะนำให้ฉีดเข้ากล้ามเนื่องจากยังไม่มีการศึกษา
FIRMAGON บริหารโดยการฉีดใต้ผิวหนังบริเวณหน้าท้อง ควรเปลี่ยนบริเวณที่ฉีดเป็นระยะ ควรฉีดยาในบริเวณที่ไม่มีแรงกด เช่น ห่างจากเข็มขัดหรือแถบยางยืด และไม่ใกล้ซี่โครง
04.3 ข้อห้าม
ภูมิไวเกินต่อสารออกฤทธิ์หรือสารเพิ่มปริมาณใด ๆ ที่ระบุไว้ในหัวข้อที่ 6
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
ผลกระทบต่อช่วง QT / QTc
การบำบัดด้วยการกีดกันแอนโดรเจนในระยะยาวอาจยืดช่วง QT ได้ การตรวจคลื่นไฟฟ้าหัวใจ (ECGs) ติดตามผลเป็นระยะ (ทุกเดือน) ในการศึกษายืนยันเปรียบเทียบ FIRMAGON กับ leuprorelin โดยสังเกตช่วงเวลาระหว่างการรักษาทั้งสองวิธี QT / QTc มากกว่า 450 มิลลิวินาทีใน ผู้ป่วยประมาณ 20% และมากกว่า 500 มิลลิวินาทีใน 1% และ 2% ของผู้ป่วยในกลุ่ม degarelix และ leuprorelin ตามลำดับ (ดูหัวข้อ 5.1)
FIRMAGON ไม่ได้รับการศึกษาในผู้ป่วยที่มีประวัติของช่วง QT ที่ถูกแก้ไขมากกว่า 450 มิลลิวินาที ในผู้ป่วยที่มีประวัติหรือปัจจัยเสี่ยงต่อ torsades de pointes และในผู้ป่วยที่รักษาร่วมกับยาที่สามารถยืดช่วงเวลา QT ได้ ดังนั้น อัตราส่วนประโยชน์/ความเสี่ยงของการรักษาด้วย FIRMAGON ควรพิจารณาอย่างรอบคอบในผู้ป่วยดังกล่าว (ดูหัวข้อ 4.5 และ 4.8)
การศึกษา QT อย่างละเอียดพบว่าไม่มีผลที่แท้จริงของ degarelix ในช่วงเวลา QT / QTc (ดูหัวข้อ 4.8)
การด้อยค่าของตับ
ผู้ป่วยที่มีปัญหาตับที่ทราบหรือสงสัยไม่รวมอยู่ในการศึกษาทางคลินิกระยะยาวกับ degarelix สังเกตการยกระดับ ALT และ AST ในระดับปานกลางและชั่วคราว ไม่ได้มาพร้อมกับระดับบิลิรูบินหรืออาการทางคลินิก แนะนำให้ติดตามการทำงานของตับในผู้ป่วยที่ทราบหรือสงสัยว่ามีความผิดปกติของตับระหว่างการรักษา เภสัชจลนศาสตร์ของ degarelix ได้รับการศึกษาหลังจากได้รับการฉีดเข้าเส้นเลือดดำเพียงครั้งเดียวในผู้ป่วยที่มีความบกพร่องทางตับในระดับเล็กน้อยถึงปานกลาง (ดูหัวข้อ 5.2)
การด้อยค่าของไต
Degarelix ไม่ได้รับการศึกษาในผู้ป่วยที่มีความบกพร่องทางไตอย่างรุนแรง ดังนั้นจึงควรให้ความระมัดระวังในผู้ป่วยดังกล่าว
ภูมิไวเกิน
Degarelix ไม่ได้รับการศึกษาในผู้ป่วยที่มีประวัติโรคหอบหืดที่ไม่ได้รับการรักษาอย่างรุนแรง ปฏิกิริยาตอบสนองแบบแอนาไฟแล็กติก หรือลมพิษรุนแรงหรือภาวะแองจิโออีดีมา
การเปลี่ยนแปลงความหนาแน่นของกระดูก
มีรายงานกรณีของความหนาแน่นของกระดูกที่ลดลงในเอกสารทางการแพทย์ในผู้ชายที่ได้รับ orchiectomy หรือรับการรักษาด้วย GnRH agonists สันนิษฐานได้ว่าการปราบปรามระดับฮอร์โมนเทสโทสเตอโรนในมนุษย์เป็นเวลานานอาจส่งผลต่อความหนาแน่นของกระดูก ไม่ได้วัดความหนาแน่นของกระดูกในระหว่างการรักษาด้วยเดกาเรลิกซ์
ความทนทานต่อกลูโคส
ความทนทานต่อกลูโคสลดลงในผู้ชายที่ได้รับ orchiectomy หรือรับการรักษาด้วย GnRH agonists การพัฒนาหรือการเสื่อมสภาพของโรคเบาหวานอาจสังเกตได้ดังนั้นผู้ป่วยโรคเบาหวานควรได้รับการติดตามระดับน้ำตาลในเลือดบ่อยครั้งมากขึ้นเมื่อได้รับการบำบัดด้วยการกีดกันแอนโดรเจน ผลของ degarelix ต่อระดับอินซูลินและกลูโคสยังไม่ได้รับการศึกษา
โรคหัวใจและหลอดเลือด
ในผู้ป่วยที่ได้รับการบำบัดด้วยการกีดกันแอนโดรเจน มีรายงานเกี่ยวกับโรคหลอดเลือดหัวใจ เช่น โรคหลอดเลือดสมองและกล้ามเนื้อหัวใจตาย ดังนั้นต้องพิจารณาปัจจัยเสี่ยงโรคหัวใจและหลอดเลือดทั้งหมด
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
ไม่มีการศึกษาปฏิสัมพันธ์ระหว่างยาอย่างเป็นทางการ
เนื่องจากการบำบัดด้วยการกีดกันแอนโดรเจนสามารถยืดช่วง QTc ได้ ควรพิจารณาการใช้ degarelix ร่วมกับยาที่ทราบว่ายืดระยะเวลาของ QTc หรือยาที่สามารถกระตุ้น torsade de pointes เช่น ยาลดความดันโลหิตในกลุ่ม IA อย่างระมัดระวัง เช่น quinidine, disopyramide) หรือ class III (เช่น amiodarone, sotalol, dofetilide, ibutilide), methadone, moxifloxacin, antipsychotics เป็นต้น (ดูหัวข้อ 4.4)
Degarelix ไม่ใช่สารตั้งต้นของระบบ CYP450 ของมนุษย์และไม่แสดงการเหนี่ยวนำหรือการยับยั้งใดๆ ในหลอดทดลอง ของ CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 หรือ CYP3A4 / 5. ดังนั้นปฏิกิริยาทางเภสัชจลนศาสตร์ที่มีนัยสำคัญทางคลินิกระหว่างยาที่เชื่อมโยงกับไอโซไซม์ดังกล่าวจึงไม่น่าเป็นไปได้
04.6 การตั้งครรภ์และให้นมบุตร
การตั้งครรภ์และให้นมบุตร
ไม่มีข้อบ่งชี้สำหรับการใช้ FIRMAGON ในสตรี
ภาวะเจริญพันธุ์
FIRMAGON สามารถยับยั้งภาวะเจริญพันธุ์ของเพศชายได้ตราบเท่าที่ฮอร์โมนเพศชายถูกระงับ
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
FIRMAGON ไม่มีหรือมีอิทธิพลเล็กน้อยต่อความสามารถในการขับขี่และการใช้เครื่องจักร ความเหนื่อยล้าและการโยกเยกเป็นผลข้างเคียงทั่วไปที่อาจส่งผลต่อความสามารถในการขับขี่หรือใช้เครื่องจักร
04.8 ผลกระทบที่ไม่พึงประสงค์
สรุปข้อมูลความปลอดภัย
ผลกระทบที่ไม่พึงประสงค์ที่สังเกตพบบ่อยที่สุดระหว่างการรักษาด้วยยา degarelix ในการศึกษาระยะที่ 3 ที่ยืนยันได้ (N = 409) เกิดจากผลทางสรีรวิทยาที่คาดหวังจากการปราบปรามฮอร์โมนเพศชาย และรวมถึงการหน้าแดงและการเพิ่มของน้ำหนัก (สังเกตใน 25% และ 7% ตามลำดับของผู้ป่วยที่รับการรักษา เป็นเวลาหนึ่งปี) หรืออาการไม่พึงประสงค์ที่บริเวณที่ฉีด มีรายงานการเริ่มมีอาการหนาวสั่น มีไข้ หรือมีอาการคล้ายไข้หวัดใหญ่ชั่วคราว (ใน 3%, 2% และ 1% ของผู้ป่วยตามลำดับ) ภายในไม่กี่ชั่วโมงหลังการให้ยา
อาการไม่พึงประสงค์จากการฉีดที่รายงานส่วนใหญ่เป็นอาการปวดและเกิดผื่นแดงซึ่งรายงานในผู้ป่วย 28% และ 17% ตามลำดับอาการบวม (6%) การแข็งตัว (4%) และการเกิดก้อน (3) พบไม่บ่อยนัก %) เหตุการณ์เหล่านี้ส่วนใหญ่เกิดขึ้นกับขนาดยาเริ่มต้นในขณะที่การรักษาด้วยขนาดยา 80 มก. อุบัติการณ์ของเหตุการณ์เหล่านี้ต่อการฉีด 100 ครั้งคือ: 3 สำหรับอาการปวดและฝีที่บริเวณที่ฉีดหรือเนื้อร้ายบริเวณที่ฉีดซึ่งอาจต้องได้รับการผ่าตัด / การระบายน้ำ
ตารางอาการไม่พึงประสงค์
ความถี่ของผลกระทบที่ไม่พึงประสงค์ตามรายการด้านล่างถูกกำหนดตามอนุสัญญาต่อไปนี้:
พบบ่อยมาก (≥ 1/10); ทั่วไป (≥ 1/100 e
ตารางที่ 1: ความถี่ของอาการไม่พึงประสงค์ที่รายงานในผู้ป่วย 1259 รายที่รักษาผู้ป่วยทั้งหมด 1781 รายในระยะเวลาหนึ่งปี (การศึกษาระยะที่ II และ III) และจากรายงานหลังการขาย
* ผลทางสรีรวิทยาที่เป็นที่รู้จักของการปราบปรามฮอร์โมนเพศชาย
คำอธิบายของอาการไม่พึงประสงค์ที่เลือก
ตัวแปรในห้องปฏิบัติการพารามิเตอร์
การเปลี่ยนแปลงของพารามิเตอร์ทางห้องปฏิบัติการที่สังเกตพบในระหว่างหนึ่งปีของการรักษาในการศึกษาระยะที่ 3 เพื่อยืนยัน (N = 409) อยู่ในช่วงเดียวกันทั้งในกลุ่มเปรียบเทียบ degarelix และ GnRH agonist (leuprorelin) ค่าผิดปกติที่เด่นชัด (> 3 * ULN) ของ transaminases ตับ (ALT, AST และ GGT) พบได้ในผู้ป่วย 2-6% ที่มีค่าปกติในช่วงเริ่มต้นของการรักษาหลังการรักษาด้วยยาทั้งสองชนิด ในผู้ป่วยที่มีภาวะปกติ ค่าก่อนการรักษาลดลงอย่างเห็นได้ชัดในค่าโลหิตวิทยา hematocrit (≤0.37) และฮีโมโกลบิน (≤115 g / l) ใน 40% และ 13-15% ตามลำดับหลังการรักษาด้วยยาทั้งสองชนิด ไม่เป็นที่รู้จักใน ซึ่งวัดค่าทางโลหิตวิทยาที่ลดลงนี้เป็นผลมาจากพยาธิสภาพพื้นฐานหรือเป็นผลมาจากการบำบัดด้วยการกีดกันแอนโดรเจน
(≥5.8 mmol / L), creatinine (≥177 μmol / L) และ BUN (≥10.7 mmol / L) ในผู้ป่วยที่มีค่าก่อนการรักษาปกติพบใน 6%, 2% และ 15% ตามลำดับ % ของผู้ป่วยที่ได้รับการรักษาด้วย degarelix และ in
3%, 2% และ 14% ของผู้ป่วยที่ได้รับ leuprorelin
การเปลี่ยนแปลงค่า ECG
การเปลี่ยนแปลงในการวัด ECG ที่สังเกตพบในระหว่างหนึ่งปีของการรักษาในการศึกษาระยะที่ 3 เพื่อยืนยัน (N = 409) อยู่ในช่วงเดียวกันทั้งใน degarelix และ
รับการรักษาด้วย GnRH agonist (leuprorelin) เป็นตัวเปรียบเทียบ ผู้ป่วย 3 ราย (500 มิลลิวินาที จากการตรวจวัดพื้นฐานจนถึงสิ้นสุดการศึกษา การเปลี่ยนแปลง QTcF เฉลี่ยอยู่ที่ 12.0 มิลลิวินาทีในกลุ่ม degarelix และ 16.7 มิลลิวินาทีในกลุ่ม leuprorelin
การขาดผลโดยธรรมชาติของ degarelix ต่อการเกิดซ้ำของหัวใจ (QTcF), อัตราการเต้นของหัวใจ, การนำ AV, การสลับขั้วของหัวใจ หรือลักษณะทางสัณฐานวิทยาของคลื่น T หรือ U ได้รับการยืนยันโดยการศึกษา QT อย่างละเอียดในอาสาสมัครที่มีสุขภาพดี (N = 80) ซึ่งได้รับ "การฉีดเข้าเส้นเลือดดำ" ของ degarelix มากกว่า 60 นาที ถึง Cmax เฉลี่ย 222 ng / ml ประมาณ 3-4 เท่าของ Cmax ที่ได้รับในระหว่างการรักษามะเร็งต่อมลูกหมาก
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยหลังจากการอนุมัติผลิตภัณฑ์ยามีความสำคัญ เนื่องจากช่วยให้สามารถตรวจสอบความสมดุลของผลประโยชน์/ความเสี่ยงของผลิตภัณฑ์ยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านสุขภาพรายงานอาการไม่พึงประสงค์ที่น่าสงสัยผ่านระบบการรายงานระดับประเทศ "ภาคผนวก 5 .
04.9 ใช้ยาเกินขนาด
ไม่มีประสบการณ์ทางคลินิกเกี่ยวกับผลของการให้ยาเกินขนาดเฉียบพลัน degarelix ในกรณีที่ให้ยาเกินขนาดผู้ป่วยควรได้รับการตรวจสอบอย่างใกล้ชิดและหากจำเป็นควรให้การบำบัดแบบประคับประคอง
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
กลุ่มเภสัชบำบัด: การรักษาต่อมไร้ท่อ ฮอร์โมนคู่อริอื่นๆ และสารที่เกี่ยวข้อง
รหัส ATC: L02BX02
กลไกการออกฤทธิ์
Degarelix เป็นสารต้านการหลั่งฮอร์โมน gonadotropin (GnRH) ที่คัดเลือกมาซึ่งผูกมัดกับตัวรับ GnRH ของต่อมใต้สมองได้อย่างแข่งขันและย้อนกลับได้ จึงช่วยลดการหลั่งของ gonadotropins, luteinizing hormone (LH) และฮอร์โมนกระตุ้นรูขุมขน (FSH) อย่างรวดเร็วส่งผลให้การหลั่งฮอร์โมนเทสโทสเตอโรนลดลง (T) โดยอัณฑะ เป็นที่ทราบกันดีว่ามะเร็งต่อมลูกหมากมีความอ่อนไหวและตอบสนองต่อการรักษาที่ขจัดแหล่งที่มาของแอนโดรเจน ซึ่งแตกต่างจากตัวเร่งปฏิกิริยา GnRH ตัวต้าน GnRH ไม่กระตุ้นให้เกิดการเพิ่มขึ้นของ LH ส่งผลให้เกิดการกระตุ้นฮอร์โมนเพศชาย / เนื้องอกและอาการที่อาจเกิดขึ้น ลุกเป็นไฟหลังจากเริ่มการรักษา
เดกาเรลิกซ์ขนาด 240 มก. ครั้งเดียว ตามด้วยขนาดยาบำรุงรายเดือน 80 มก. ทำให้ความเข้มข้นของ LH และ FSH ลดลงอย่างรวดเร็ว และส่งผลให้ฮอร์โมนเทสโทสเตอโรนลดลง ความเข้มข้นในซีรัมของไดไฮโดรเทสโทสเตอโรน (DHT) ลดลงในลักษณะเดียวกับฮอร์โมนเทสโทสเตอโรน Degarelix มีประสิทธิภาพในการบรรลุและรักษาระดับการปราบปรามฮอร์โมนเพศชายต่ำกว่าระดับการตัดตอนทางการแพทย์ 0.5 ng / mL ปริมาณการบำรุงรักษารายเดือน 80 มก. ช่วยให้สามารถระงับฮอร์โมนเทสโทสเตอโรนในผู้ป่วย 97% เป็นเวลาอย่างน้อยหนึ่งปี ไม่พบยอดฮอร์โมนเทสโทสเตอโรนหลังการฉีดหลังจากครั้งแรกระหว่างการรักษาด้วย degarelix ระดับฮอร์โมนเทสโทสเตอโรนเฉลี่ยหลังการรักษาหนึ่งปีเท่ากับ 0.087 ng / mL (พิสัยระหว่างควอไทล์ 0.06-0.15) N = 167
ผลการศึกษาระยะที่ 3 ยืนยัน
ประสิทธิภาพและความปลอดภัยของ degarelix ได้รับการประเมินในการศึกษาแบบกลุ่มคู่ขนานแบบเปิด หลายศูนย์ สุ่มตัวอย่าง กลุ่มควบคุม โดยการศึกษาได้ประเมินประสิทธิภาพและความปลอดภัยของสูตรการให้ยา degarelix สองชุดต่อเดือนด้วยขนาดยาเริ่มต้น 240 มก. (40 มก. / มล.) ตาม โดยการฉีดเข้าใต้ผิวหนังรายเดือน 160 มก. (40 มก. / มล.) หรือ 80 มก. (20 มก. / มล.) เทียบกับการให้ leuprorelin เข้ากล้ามเนื้อรายเดือน 7.5 มก. ในผู้ป่วยมะเร็งต่อมลูกหมากที่ต้องการการบำบัดด้วยการกีดกันแอนโดรเจน ผู้ป่วยทั้งหมด 620 รายได้รับการสุ่มให้อยู่ในกลุ่มการรักษา 3 กลุ่ม โดยผู้ป่วย 504 คน (81%) เสร็จสิ้นการศึกษา ในกลุ่ม degarelix 240/80 มก. ผู้ป่วย 41 คน (20%) หยุดการศึกษา เทียบกับผู้ป่วย 32 คน (16%) ในกลุ่ม leuprorelin
จากผู้ป่วย 610 รายที่รักษา:
• 31% มีมะเร็งต่อมลูกหมากเฉพาะที่
• 29% มีมะเร็งต่อมลูกหมากขั้นสูงในพื้นที่
• 20% มีมะเร็งต่อมลูกหมากระยะแพร่กระจาย
• 7% มีสถานะการแพร่กระจายที่ไม่ทราบสาเหตุ
• 13% เคยได้รับการรักษาด้วยการผ่าตัดหรือการฉายรังสีหรือมี PSA เพิ่มขึ้น
ข้อมูลประชากรพื้นฐานมีความคล้ายคลึงกันสำหรับทุกกลุ่ม อายุเฉลี่ย 74 ปี (ช่วง 47 ถึง 98 ปี) วัตถุประสงค์หลักคือการแสดงให้เห็นถึงประสิทธิภาพของ degarelix ในการบรรลุและรักษาระดับการปราบปรามฮอร์โมนเพศชายต่ำกว่า 0.5 ng / ml ในช่วง 12 เดือนของการรักษา: ปริมาณการบำรุงรักษาที่มีประสิทธิภาพต่ำสุด 80 มก. เดอกาเรลิกซ์ได้รับเลือก
ความสำเร็จของระดับฮอร์โมนเพศชายในซีรัม (T) ≤0.5 ng / ml
FIRMAGON มีประสิทธิภาพในการบรรลุการปราบปรามฮอร์โมนเทสโทสเตอโรนอย่างรวดเร็ว ดูตารางที่ 2
ตารางที่ 2: ร้อยละของผู้ป่วยที่ได้รับT≤0.5 ng / mL หลังเริ่มการรักษา
หลีกเลี่ยงการเพิ่มฮอร์โมนเทสโทสเตอโรนอย่างกะทันหัน
การเพิ่มขึ้นอย่างกะทันหันหมายถึงเกินระดับฮอร์โมนเทสโทสเตอโรนพื้นฐานที่≥15% ในช่วงสองสัปดาห์แรก
ไม่พบการเพิ่มขึ้นของฮอร์โมนเพศชายในผู้ป่วยที่ได้รับการรักษาด้วย degarelix; มีฮอร์โมนเทสโทสเตอโรนลดลงโดยเฉลี่ย 94% ในวันที่ 3 ผู้ป่วยส่วนใหญ่ที่ได้รับ leuprorelin มีระดับฮอร์โมนเทสโทสเตอโรนเพิ่มขึ้นโดยเฉลี่ย 65% ในวันที่ 3 ความแตกต่างเหล่านี้มีนัยสำคัญทางสถิติ (p
จุดสิ้นสุดหลักของการศึกษาคืออัตราการปราบปรามฮอร์โมนเทสโทสเตอโรนหลังการรักษาด้วย degarelix หรือ leuprorelin เป็นเวลา 1 ปี ไม่ได้แสดงให้เห็นประโยชน์ทางคลินิกของ degarelix เมื่อเทียบกับ leuprorelin ที่เกี่ยวข้องกับการต่อต้านแอนโดรเจนในการรักษาในระยะแรก
ฟื้นฟูระดับเทสโทสเตอโรน
ในการศึกษาเกี่ยวกับผู้ป่วยที่มี PSA สูงหลังการรักษาเฉพาะที่ (ส่วนใหญ่เป็นการผ่าตัดต่อมลูกหมากและการฉายรังสี) FIRMAGON ได้รับการบริหารเป็นระยะเวลาเจ็ดเดือนตามด้วยระยะเวลาการตรวจสอบเจ็ดเดือน เวลามัธยฐานในการฟื้นตัวของระดับฮอร์โมนเทสโทสเตอโรน (> 0.5 ng / mL เกินระดับการตัดอัณฑะ) หลังจากหยุดการรักษาคือ 112 วัน (คำนวณจากการเริ่มต้นของระยะเวลาการติดตาม เช่น 28 วันหลังจากการฉีดครั้งสุดท้าย ) เวลามัธยฐานในการเข้าถึงระดับฮอร์โมนเพศชาย> 1.5 ng / mL (เหนือขีดจำกัดล่างของช่วงปกติ) คือ 168 วัน
ประสิทธิภาพในระยะยาว
ความสำเร็จในการรักษาถูกกำหนดในการศึกษาโดยบรรลุระดับการตัดตอนทางการแพทย์ในวันที่ 28 และรักษาระดับความเข้มข้นของฮอร์โมนเพศชายไม่เกิน 0.5 ng / ml ในวันที่ 364 ของการรักษา
ตารางที่ 3: ความน่าจะเป็นสะสมของฮอร์โมนเพศชาย ≤0.5 ng / mL จากวันที่ 28 ถึงวันที่ 364
* Kaplan Meier ประมาณการสำหรับกลุ่ม
ผลสัมฤทธิ์ของการลดแอนติเจนจำเพาะต่อมลูกหมาก (PSA)
ขนาดของเนื้องอกไม่ได้วัดโดยตรงในระหว่างการศึกษาทางคลินิก แต่มีการตอบสนองของเนื้องอกในเชิงบวกทางอ้อมที่แสดงให้เห็นเป็นค่ามัธยฐาน PSA ที่ลดลง 95% ด้วย degarelix หลังจาก 12 เดือน
ค่ามัธยฐาน PSA ในการศึกษาพื้นฐานคือ:
• 19.8 ng / mL (พิสัยระหว่างควอไทล์: P25 9.4 ng / mL, P75 46.4 ng / mL) ในกลุ่ม degarelix 240/80 มก.
• 17.4 ng / mL (พิสัยระหว่างควอไทล์: P25 8.4 ng / mL, P75 56.5 ng / mL) ในกลุ่ม leuprorelin 7.5 มก.
ความแตกต่างมีนัยสำคัญทางสถิติ (p
ระดับแอนติเจนจำเพาะต่อมลูกหมาก (PSA) ลดลง 64% หลังจากให้ยา degarelix สองสัปดาห์ โดย 85% หลังจากหนึ่งเดือนและ 95% หลังจากสามเดือน ยังคงถูกระงับ (ประมาณ 97%) เป็นระยะเวลาการรักษาหนึ่งช่วง หนึ่งปี
ตั้งแต่วันที่ 56 ถึงวันที่ 364 ไม่มีความแตกต่างอย่างมีนัยสำคัญในอัตราการเปลี่ยนแปลงจากเส้นฐานระหว่างเดกาเรลิกซ์กับตัวเปรียบเทียบ
ผลกระทบต่อปริมาณต่อมลูกหมาก
การรักษาด้วย degarelix เป็นเวลา 3 เดือน (ขนาดยา 240/80 มก.) ส่งผลให้ปริมาตรต่อมลูกหมากลดลง 37% โดยวัดโดยอัลตราซาวนด์ทางทวารหนักในผู้ป่วยที่ต้องใช้ฮอร์โมนบำบัดก่อนการฉายรังสีและในผู้ป่วยที่เข้ารับการตัดอัณฑะทางการแพทย์ ปริมาณต่อมลูกหมากที่ลดลงนั้นคล้ายกับที่ได้รับจาก goserelin บวกกับการป้องกันแอนโดรเจน
ผลกระทบต่อช่วง QT / QTc
การตรวจคลื่นไฟฟ้าหัวใจควบคุมเป็นระยะในการศึกษายืนยันเปรียบเทียบ FIRMAGON กับ leuprorelin ด้วยการรักษาทั้งสองแบบ ผู้ป่วยประมาณ 20% ของผู้ป่วยจะสังเกตเห็นช่วง QT / QTc มากกว่า 450 มิลลิวินาที จากการตรวจวัดพื้นฐานจนถึงสิ้นสุดการศึกษา การเปลี่ยนแปลงค่ามัธยฐานที่วัดด้วย FIRMAGON เท่ากับ 12.0 มิลลิวินาที และด้วย leuprorelin เท่ากับ 16.7 มิลลิวินาที
แอนติบอดีต่อต้าน degarelix
การพัฒนาแอนติบอดีต่อต้าน degarelix พบได้ในผู้ป่วย 10% หลังการรักษาด้วย FIRMAGON หนึ่งปีและในผู้ป่วย 29% หลังการรักษาด้วย FIRMAGON นานถึง 5.5 ปี ไม่มีข้อบ่งชี้ว่าการก่อตัวของแอนติบอดีเหล่านี้ส่งผลต่อประสิทธิภาพและความปลอดภัยของ FIRMAGON นานถึง 5.5 ปีของการรักษา
ประชากรเด็ก
European Medicines Agency ได้ปลด FIRMAGON จากภาระหน้าที่ในการส่งผลการศึกษาในกลุ่มย่อยทั้งหมดของประชากรเด็ก (ดูหัวข้อ 4.2 สำหรับข้อมูลเกี่ยวกับการใช้ในเด็ก)
05.2 คุณสมบัติทางเภสัชจลนศาสตร์
การดูดซึม
หลังจากได้รับ degarelix 240 มก. ใต้ผิวหนังที่ความเข้มข้น 40 มก. / มล. ให้กับผู้ป่วยมะเร็งต่อมลูกหมากในการศึกษาการพิจาณา CS21 AUC0-28 วันคือ 635 (602-668) วัน * ng / ml, Cmax คือ 66.0 (61.0- 71.0) ng / mL และถึง Tmax 40 (37-42) ชั่วโมง ค่าเฉลี่ยอยู่ที่ประมาณ 11-12 ng / mL หลังจากเริ่มยาและ 11-16 ng / ml หลังจากปริมาณการบำรุงรักษา 80 มก. ที่ความเข้มข้นของ 20 มก. / มล. หลังจาก Cmax ความเข้มข้นในพลาสมาของ degarelix จะลดลงในลักษณะ biphasic โดยมีครึ่งชีวิตสุดท้ายเฉลี่ย (t½) ที่ 29 วันด้วยปริมาณการบำรุงรักษา สำหรับการบริหารใต้ผิวหนังเป็นผลมาจากการปลดปล่อย degarelix ที่ช้ามาก ตะกอนที่เกิดขึ้นบริเวณที่ฉีด พฤติกรรมทางเภสัชจลนศาสตร์ของยาได้รับอิทธิพลจากความเข้มข้นของยาในสารละลายสำหรับการฉีด ดังนั้น Cmax และการดูดซึมมักจะลดลงเมื่อความเข้มข้นของยาเพิ่มขึ้นในขณะที่ค่าครึ่งชีวิตมีแนวโน้มลดลง ง เพิ่มขึ้น ดังนั้นจึงไม่ควรใช้ความแรงของขนาดยาอื่นนอกเหนือจากที่แนะนำ
การกระจาย
ปริมาณการกระจายในชายสูงอายุที่มีสุขภาพดีอยู่ที่ประมาณ 1 ลิตรต่อกิโลกรัม การจับโปรตีนในพลาสมาคาดว่าจะอยู่ที่ประมาณ 90%
การเปลี่ยนแปลงทางชีวภาพ
Degarelix ผ่านการย่อยสลายเปปไทด์ทั่วไประหว่างทางเดินผ่านระบบตับและน้ำดี และส่วนใหญ่ถูกขับออกมาเป็นเศษเปปไทด์ในอุจจาระ ไม่พบเมแทบอไลต์ที่มีนัยสำคัญในตัวอย่างพลาสมาหลังการให้ยาใต้ผิวหนัง การศึกษา ในหลอดทดลอง แสดงให้เห็นว่า degarelix ไม่ใช่สารตั้งต้นของระบบ CYP450 ของมนุษย์
การกำจัด
ในผู้ชายที่มีสุขภาพดี ประมาณ 20-30% ของการฉีดเข้าเส้นเลือดดำเพียงครั้งเดียวจะถูกขับออกทางปัสสาวะ ซึ่งบ่งบอกว่า 70-80% จะถูกขับออกทางระบบตับและน้ำดี การกวาดล้างของ degarelix ที่ฉีดเข้าเส้นเลือดดำครั้งเดียว (0.864-49.4 mcg / kg) ในชายสูงอายุที่มีสุขภาพดีคือ 35-50 มล. / ชม. / กก.
ประชากรพิเศษ:
ผู้ป่วยไตเสื่อม
ไม่ได้มีการศึกษาเภสัชจลนศาสตร์ในผู้ป่วยที่มีความผิดปกติของไต ประมาณ 20-30% ของขนาดยา degarelix ที่ถูกขับออกทางไตไม่เปลี่ยนแปลง การวิเคราะห์ทางเภสัชจลนศาสตร์ของประชากรของการศึกษายืนยันระยะที่ 3 แสดงให้เห็นว่าการขจัด degarelix ในผู้ป่วยไตวายเล็กน้อยหรือปานกลางลดลงประมาณ 23% ดังนั้นจึงไม่แนะนำให้ปรับขนาดยาในผู้ป่วยดังกล่าว ดังนั้นจึงแนะนำให้ใช้ความระมัดระวังในผู้ป่วยเหล่านี้
ผู้ป่วยโรคตับ
Degarelix ได้รับการประเมินในการศึกษาเภสัชจลนศาสตร์ในผู้ป่วยที่มีความบกพร่องทางตับในระดับเล็กน้อยถึงปานกลาง ไม่พบสัญญาณของการเปิดรับแสงมากเกินไปในผู้ป่วยที่มีความผิดปกติของตับเมื่อเปรียบเทียบกับคนที่มีสุขภาพดี ไม่จำเป็นต้องปรับขนาดยาในผู้ป่วยที่มีความผิดปกติของตับเล็กน้อยถึงปานกลาง ผู้ป่วยที่มีความผิดปกติของตับอย่างรุนแรงยังไม่ได้รับการศึกษา ดังนั้นจึงควรให้ความระมัดระวังในกลุ่มนี้
05.3 ข้อมูลความปลอดภัยพรีคลินิก
การศึกษาการสืบพันธุ์ของสัตว์แสดงให้เห็นว่าเดกาเรลิกซ์ทำให้เกิดภาวะมีบุตรยากในสัตว์เพศผู้ นี่เป็นเพราะผลทางเภสัชวิทยาที่สามารถย้อนกลับได้
ในการศึกษาความเป็นพิษต่อระบบสืบพันธุ์ในเพศหญิง degarelix ให้ผลลัพธ์ที่คาดหวังเนื่องจากลักษณะทางเภสัชวิทยา มันทำให้เกิดการยืดเวลาของการผสมพันธุ์และการตั้งครรภ์ขึ้นอยู่กับปริมาณยา corpora luteaและการเพิ่มขึ้นของการสูญเสียก่อนและหลังการปลูกถ่าย การทำแท้ง การตายของตัวอ่อน / ทารกในครรภ์ การคลอดก่อนกำหนด และระยะเวลาของการคลอด
การศึกษาความปลอดภัยทางเภสัชวิทยาพรีคลินิก การศึกษาความเป็นพิษซ้ำ ความเป็นพิษต่อพันธุกรรม และศักยภาพในการก่อมะเร็ง ไม่ได้แสดงความเสี่ยงเฉพาะสำหรับสายพันธุ์มนุษย์ โดยเฉพาะทั้งการศึกษา ในหลอดทดลอง นั่น ในร่างกาย ไม่พบการยืด QT
ไม่พบความเป็นพิษเฉพาะอวัยวะในการศึกษาแบบเฉียบพลัน กึ่งเฉียบพลัน หรือเรื้อรังในหนูและลิงหลังการให้ยา degarelix ฉีดเข้าใต้ผิวหนัง การระคายเคืองเฉพาะที่ที่เกี่ยวข้องกับยาถูกบันทึกไว้เมื่อให้ degarelix ฉีดเข้าใต้ผิวหนังในปริมาณที่สูงแก่สัตว์
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
ฝุ่น
แมนนิทอล (E421)
ตัวทำละลาย
น้ำสำหรับฉีด
06.2 ความเข้ากันไม่ได้
ในกรณีที่ไม่มีการศึกษาความเข้ากันได้ ห้ามผสมผลิตภัณฑ์นี้กับยาอื่น
06.3 ระยะเวลาที่มีผลบังคับใช้
3 ปี
หลังจากสร้างใหม่
มีการแสดงความเสถียรทางเคมีและกายภาพระหว่างการใช้งานเป็นเวลา 2 ชั่วโมงที่อุณหภูมิ 25 องศาเซลเซียส จากมุมมองของจุลชีววิทยา เว้นแต่วิธีการสร้างใหม่ไม่รวมความเสี่ยงของการปนเปื้อนของแบคทีเรีย ควรใช้ผลิตภัณฑ์ทันที ถ้าไม่ใช้ ทันที เวลาและเงื่อนไขการใช้งานเป็นความรับผิดชอบของผู้ใช้
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
ไม่มีข้อควรระวังพิเศษ
สำหรับสภาวะการเก็บรักษาของผลิตภัณฑ์ที่สร้างใหม่ ดูหัวข้อ 6.3
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
ขวดแก้ว (แบบที่ 1) พร้อมจุกยางโบรโมบิวทิลและซีลแบบพลิกปิดอะลูมิเนียมที่มีผง 80 มก. สำหรับสารละลายสำหรับฉีด
กระบอกฉีดยาแก้วที่เติมไว้ล่วงหน้า (ประเภท I) พร้อมลูกสูบอีลาสโตเมอร์ ฝาและเส้นทำเครื่องหมาย 4 มล. ที่มีตัวทำละลาย 4.2 มล.
ลูกสูบ
อะแดปเตอร์ขวด
เข็มฉีดยา (25G 0.5 x 25mm)
บรรจุภัณฑ์ FIRMAGON มีให้เลือกสองแพ็คเกจ:
แพ็ค 1 ถาดประกอบด้วย: ผง 1 ขวด, กระบอกฉีดยาตัวทำละลาย 1 กระบอก, ลูกสูบ 1 อัน, อะแดปเตอร์ 1 ขวดและ 1 เข็ม
แพ็ค 3 ถาดประกอบด้วย: ผง 3 ขวด, กระบอกฉีดยาตัวทำละลาย 3 หลอด, ลูกสูบ 3 ชิ้น, อะแดปเตอร์ขวด 3 ชิ้น และ 3 เข็ม
ขนาดบรรจุภัณฑ์บางขนาดอาจไม่มีอยู่ในท้องตลาด
06.6 คำแนะนำในการใช้งานและการจัดการ
ทำตามคำแนะนำสำหรับการคืนสภาพอย่างระมัดระวัง
ไม่แนะนำให้ใช้ยาที่มีความเข้มข้นต่างกัน เนื่องจากความเข้มข้นของเจลจะก่อตัว สารละลายที่สร้างใหม่ควรเป็นของเหลวใส ปราศจากอนุภาคที่ไม่ละลายน้ำ
บันทึก:
• ห้ามเขย่าขวด
ชุดประกอบด้วยขวดผงและเข็มฉีดยาตัวทำละลายที่เติมไว้ล่วงหน้าซึ่งจะต้องเตรียมสำหรับการฉีดใต้ผิวหนัง
1. ถอดฝาครอบออกจากแพ็คเกจอะแดปเตอร์ขวด แนบอะแดปเตอร์เข้ากับขวดผงโดยกดลงจนปลายผ่านจุกยางและอะแดปเตอร์คลิกเข้าที่
2. เตรียมกระบอกฉีดยาที่เติมไว้ล่วงหน้าโดยใส่ลูกสูบ
3. ถอดฝากระบอกฉีดยาที่บรรจุไว้ล่วงหน้าออก แนบกระบอกฉีดยาเข้ากับขวดผงโดยขันสกรูเข้ากับอะแดปเตอร์ โอนตัวทำละลายทั้งหมดไปยังขวดผง
4. ใส่กระบอกฉีดยาลงในอะแดปเตอร์ หมุนเบา ๆ จนของเหลวใสและปราศจากอนุภาคหรือผงที่ไม่ละลายน้ำ หากผงยึดติดกับขวดเหนือพื้นผิวของของเหลว ขวดสามารถเอียงเล็กน้อย หลีกเลี่ยงการเขย่าเพื่อป้องกัน เกิดฟอง
การก่อตัวของวงแหวนของฟองอากาศขนาดเล็กบนพื้นผิวของของเหลวนั้นเป็นที่ยอมรับได้ โดยปกติ ขั้นตอนการคืนสภาพจะใช้เวลาสองสามนาทีแต่ในบางกรณีอาจใช้เวลานานถึง 15 นาที
5. พลิกขวดคว่ำลงแล้วลากขึ้นไปที่เส้นการทำเครื่องหมายของเข็มฉีดยา
ตรวจสอบให้แน่ใจเสมอว่าได้ดูดปริมาตรที่แน่นอนและปรับให้เข้ากับฟองอากาศ
6. ถอดกระบอกฉีดยาออกจากอะแดปเตอร์แล้วสอดเข็มฉีดยาเข้าใต้ผิวหนังลึกเข้าไปในกระบอกฉีดยา
7. ฉีดเข้าใต้ผิวหนังลึก เมื่อต้องการทำเช่นนี้: จับผิวหนังของช่องท้อง ยกเนื้อเยื่อใต้ผิวหนัง และสอดเข็มเข้าไปลึก ๆ ที่มุมไม่น้อยกว่า 45 องศา
ค่อยๆ ฉีด FIRMAGON 80 มก. 4 มล. ทันทีหลังจากคืนสภาพ
ไม่ควรฉีดยาในบริเวณที่ผู้ป่วยอาจได้รับแรงกด เช่น ในบริเวณเข็มขัด ที่มีแถบคาดหรือใกล้ซี่โครง
ห้ามฉีดเข้าเส้นเลือดโดยตรง ค่อย ๆ ดึงลูกสูบกระบอกฉีดกลับเพื่อตรวจดูว่าเลือดถูกดูดเข้าไปหรือไม่ หากมีเลือดอยู่ในหลอดฉีดยา จะต้องใช้ยานี้อีกต่อไป หยุดขั้นตอนและทิ้งเข็มฉีดยาและเข็ม (เตรียมยาใหม่สำหรับผู้ป่วย)
ไม่มีข้อกำหนดพิเศษสำหรับการกำจัด
07.0 ผู้ทรงอำนาจการตลาด
Ferring Pharmaceuticals A / S
Kay Fiskers Plads 11
DK-2300 โคเปนเฮเกน S
เดนมาร์ก
08.0 หมายเลขอนุญาตการตลาด
EU / 1/08/504/001
039232018
EU / 1/08/504/003
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
วันที่ได้รับอนุญาตครั้งแรก: 17/02/2009
วันที่ต่ออายุครั้งล่าสุด: 19/09/2013
10.0 วันที่แก้ไขข้อความ
DCE พฤศจิกายน 2014