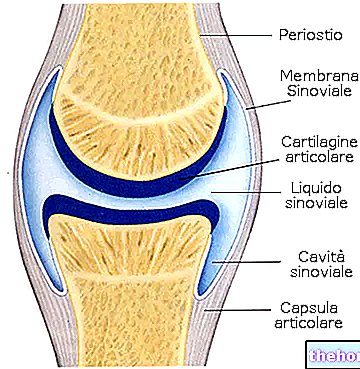
คำนิยาม
เอ็นไซม์เป็นโปรตีนที่ผลิตขึ้นในเซลล์พืชและสัตว์ ซึ่งทำหน้าที่เป็นตัวเร่งปฏิกิริยาที่เร่งปฏิกิริยาทางชีวภาพโดยไม่ถูกดัดแปลง
เอ็นไซม์ทำงานโดยการรวมตัวกับสารเฉพาะเพื่อเปลี่ยนเป็นสารที่แตกต่างกัน ตัวอย่างคลาสสิกได้รับจากเอ็นไซม์ย่อยอาหารที่มีอยู่ในน้ำลาย กระเพาะอาหาร ตับอ่อน และลำไส้เล็ก ซึ่งทำหน้าที่สำคัญในการย่อยอาหารและช่วยย่อยอาหารให้เป็นองค์ประกอบพื้นฐาน ซึ่งร่างกายสามารถดูดซึมและนำไปใช้ได้ แปรรูปโดยเอนไซม์อื่นหรือ ถูกขับออกมาเป็นของเสีย
เอนไซม์แต่ละตัวมีหน้าที่เฉพาะ: เอนไซม์ที่สลายไขมัน เช่น ไม่ทำปฏิกิริยากับโปรตีนหรือคาร์โบไฮเดรต เอ็นไซม์มีความจำเป็นสำหรับความเป็นอยู่ที่ดีของสิ่งมีชีวิต การขาด แม้แต่เอ็นไซม์ตัวเดียวก็สามารถทำให้เกิดการรบกวนที่รุนแรงได้ ตัวอย่างที่รู้จักกันดีคือ ฟีนิลคีโตนูเรีย (PKU) โรคที่มีลักษณะเฉพาะโดยไม่สามารถเผาผลาญกรดอะมิโนที่จำเป็น ฟีนิลอะลานีนซึ่งสะสมไว้อาจทำให้เกิดความผิดปกติทางร่างกายและความเจ็บป่วยทางจิต
การศึกษาทางชีวเคมี
เอ็นไซม์เป็นโปรตีนเฉพาะที่มีคุณสมบัติเป็นตัวเร่งปฏิกิริยาทางชีวภาพ กล่าวคือ พวกมันมีความสามารถในการทำลายพลังงานกระตุ้น (Eatt) ของปฏิกิริยา ปรับเปลี่ยนเส้นทางของมันเพื่อให้กระบวนการทางจลนศาสตร์เร็วขึ้น
เอ็นไซม์เพิ่มจลนพลศาสตร์ของปฏิกิริยาที่เป็นไปได้ทางอุณหพลศาสตร์ และไม่เหมือนกับตัวเร่งปฏิกิริยา พวกมันมีความเฉพาะเจาะจงมากหรือน้อย: พวกมันจึงมีความจำเพาะของซับสเตรต
เอนไซม์ไม่เกี่ยวข้องกับปริมาณสารสัมพันธ์ของปฏิกิริยา: สำหรับสิ่งนี้ที่จะเกิดขึ้น ตำแหน่งเร่งปฏิกิริยาขั้นสุดท้ายจะต้องเหมือนกันกับจุดเริ่มต้น
ในการเร่งปฏิกิริยามักจะมีเฟสที่ช้าซึ่งกำหนดความเร็วของกระบวนการ
เมื่อเราพูดถึงเอนไซม์ การพูดถึงปฏิกิริยาสมดุลนั้นไม่ถูกต้อง เราพูดแทน สภาวะคงตัว (สถานะที่เมตาโบไลต์บางชนิดถูกสร้างขึ้นและบริโภคอย่างต่อเนื่อง โดยรักษาความเข้มข้นของเมตาโบไลต์ให้คงที่ตลอดเวลา) ผลคูณของปฏิกิริยาที่เร่งปฏิกิริยาโดยเอนไซม์ตัวหนึ่งมักจะเป็นตัวทำปฏิกิริยาสำหรับปฏิกิริยาที่ตามมา เร่งด้วยเอนไซม์อื่น เป็นต้น
กระบวนการที่เร่งปฏิกิริยาด้วยเอนไซม์มักจะประกอบด้วยลำดับของปฏิกิริยา
ปฏิกิริยาทั่วไปที่กระตุ้นโดยเอนไซม์ (E) สามารถสรุปได้ดังนี้:

E คือเอนไซม์
S คือสารตั้งต้น
ES แสดงถึง adduct ระหว่างเอนไซม์และซับสเตรต
P คือผลิตภัณฑ์
K คือค่าคงที่อัตราของปฏิกิริยา
เอนไซม์ทั่วไป (E) รวมกับสารตั้งต้น (S) เพื่อสร้าง adduct (ES) ที่มีอัตราคงที่ K1 มันสามารถแยกกลับเป็น E + S โดยมีอัตราคงที่ K2 หรือ (ถ้า "ชีวิต" นานพอ ) สามารถดำเนินการในรูปแบบ P ด้วยความเร็วคงที่ K3
ในทางกลับกัน ผลิตภัณฑ์ (P) สามารถรวมกันใหม่กับเอนไซม์และปฏิรูป adduct ด้วยอัตราคงที่ K4
เมื่อเอนไซม์และซับสเตรตผสมกัน จะมีเวลาเพียงเศษเสี้ยวที่ยังไม่มีการบรรจบกันระหว่างสองสปีชีส์ นั่นคือ มีช่วงเวลาสั้นมาก (ซึ่งขึ้นอยู่กับปฏิกิริยา) ซึ่งเอ็นไซม์และซับสเตรตมี ยังไม่พบ หลังจากช่วงเวลานี้ เอ็นไซม์และซับสเตรตจะสัมผัสกันในปริมาณที่เพิ่มขึ้นและเกิด ES adduct ต่อมา เอ็นไซม์ทำหน้าที่บนซับสเตรตและผลิตภัณฑ์ถูกปล่อยออกมา กล่าวได้ว่า c "เป็นช่วงเวลาเริ่มต้นซึ่งไม่สามารถกำหนดความเข้มข้นของ ES adduct ได้ หลังจากช่วงเวลานี้ถือว่าอยู่ในสถานะคงตัว กำหนดขึ้น กล่าวคือ ความเร็วของกระบวนการที่นำไปสู่การรับแอดดักต์นั้นเท่ากับความเร็วของกระบวนการที่นำไปสู่การทำลายแอดดักต์
ค่าคงที่ Michaelis-Menten (KM) เป็นค่าคงที่สมดุล (อ้างอิงถึงสมดุลแรกที่อธิบายข้างต้น); สามารถพูดได้ด้วยการประมาณที่ดี (เพราะควรพิจารณา K3 ด้วย) ว่า KM นั้นแสดงด้วยอัตราส่วนระหว่างค่าคงที่จลนศาสตร์ K2 และ K1 (อ้างอิงถึงการทำลายและการก่อตัวของ adduct ES ในสมดุลแรกที่อธิบายข้างต้น) .
จากค่าคงที่ Michaelis-Menten เรามี "การบ่งชี้ความสัมพันธ์ระหว่างเอนไซม์และสารตั้งต้น: ถ้า KM มีค่าน้อย c" คือ "ความสัมพันธ์สูงระหว่างเอนไซม์และสารตั้งต้น ดังนั้น ES adduct จะเสถียร
เอนไซม์อยู่ภายใต้การควบคุม (หรือการปรับ)
ในอดีตมีการพูดถึงการปรับเชิงลบเป็นหลัก กล่าวคือ การยับยั้งความสามารถในการเร่งปฏิกิริยาของเอนไซม์ แต่อาจมีการปรับเชิงบวกด้วย นั่นคือ มีสายพันธุ์ที่สามารถเพิ่มความสามารถในการเร่งปฏิกิริยาของเอนไซม์ได้
การยับยั้งมี 4 ประเภท (ได้จากการประมาณที่ทำกับแบบจำลองเพื่อจับคู่ข้อมูลการทดลองกับสมการทางคณิตศาสตร์):
- การยับยั้งการแข่งขัน
- การยับยั้งที่ไม่แข่งขัน
- การยับยั้งที่ไม่สามารถแข่งขันได้
- การยับยั้งการแข่งขัน
เราพูดถึงการยับยั้งการแข่งขันเมื่อโมเลกุล (ตัวยับยั้ง) สามารถแข่งขันกับสารตั้งต้นได้ สำหรับความคล้ายคลึงของโครงสร้าง ตัวยับยั้งสามารถทำปฏิกิริยาแทนสารตั้งต้น ดังนั้น คำศัพท์ "การยับยั้งการแข่งขัน" ความน่าจะเป็นที่เอนไซม์จับกับสารยับยั้งหรือสารตั้งต้นขึ้นอยู่กับความเข้มข้นของทั้งสองอย่างและความใกล้ชิดกับเอนไซม์ อัตราการเกิดปฏิกิริยาจึงขึ้นอยู่กับปัจจัยเหล่านี้
เพื่อให้ได้อัตราการเกิดปฏิกิริยาเดียวกันกับที่ไม่มีตัวยับยั้ง จำเป็นต้องมีความเข้มข้นของซับสเตรตที่สูงขึ้น
จากการทดลองแสดงให้เห็นว่า เมื่อมีสารยับยั้ง ค่าคงที่ของ Michaelis-Menten จะเพิ่มขึ้น
ในทางกลับกัน "การยับยั้งที่ไม่ใช่การแข่งขัน อันตรกิริยาระหว่างโมเลกุลที่ควรทำหน้าที่เป็นโมดูเลเตอร์ (ตัวยับยั้งเชิงบวกหรือเชิงลบ) กับ" เอ็นไซม์ เกิดขึ้นในบริเวณที่แตกต่างจากที่ปฏิสัมพันธ์ เกิดขึ้นระหว่างเอนไซม์กับสารตั้งต้น ดังนั้นเราจึงพูดถึงการปรับอัลโลสเตอริก (จากภาษากรีก อัลโลสเตอส → เว็บไซต์อื่น)
ถ้าตัวยับยั้งจับกับเอนไซม์ ก็สามารถทำให้เกิดการเปลี่ยนแปลงในโครงสร้างของเอนไซม์ และทำให้ประสิทธิภาพในการจับกับเอนไซม์ลดลง
ในกระบวนการประเภทนี้ ค่าคงที่ Michaelis-Menten จะคงที่เนื่องจากค่านี้ขึ้นอยู่กับสมดุลระหว่างเอนไซม์กับซับสเตรต และแม้ในที่ที่มีตัวยับยั้ง สมดุลเหล่านี้จะไม่เปลี่ยนแปลง
ปรากฏการณ์ของการยับยั้งที่ไม่สามารถแข่งขันได้นั้นหายาก ตัวยับยั้งที่ไม่สามารถแข่งขันได้โดยทั่วไปคือสารที่ผูกกลับกับ ES adduct ทำให้เกิด ESI:

การยับยั้งจากซับสเตรตส่วนเกินในบางครั้งอาจไม่สามารถแข่งขันได้ เนื่องจากสิ่งนี้เกิดขึ้นเมื่อโมเลกุลซับสเตรตที่สองจับกับสารเชิงซ้อน ES ทำให้เกิดสารเชิงซ้อน ESS
ในทางกลับกัน ตัวยับยั้งการแข่งขันสามารถจับกับเอนไซม์แอดดักต์ของซับสเตรตเท่านั้นเช่นเดียวกับในกรณีก่อนหน้านี้: การจับของซับสเตรตกับเอ็นไซม์อิสระทำให้เกิดการดัดแปลงโครงสร้างซึ่งทำให้ไซต์สามารถเข้าถึงได้สำหรับตัวยับยั้ง
ค่าคงที่ของ Michaelis Menten ลดลงเมื่อความเข้มข้นของตัวยับยั้งเพิ่มขึ้น: เห็นได้ชัดว่าความสัมพันธ์ของเอนไซม์กับสารตั้งต้นเพิ่มขึ้น
ซีรีนโปรตีเอส
พวกเขาเป็นตระกูลของเอนไซม์ที่มีไคโมทริปซินและทริปซินอยู่
Chymotrypsin เป็นเอนไซม์ย่อยโปรตีนและไฮโดรไลติกที่ตัดไปทางขวาของกรดอะมิโนที่ไม่ชอบน้ำและอะโรมาติก
ผลิตภัณฑ์ของยีนที่เข้ารหัสไคโมทริปซินไม่ทำงาน (เปิดใช้งานด้วยคำสั่ง); รูปแบบที่ไม่ใช้งานของ chymotrypsin นั้นแสดงด้วยสายโซ่โพลีเปปไทด์ที่มีกรดอะมิโน 245 ตัว Chymotrypsin มีรูปร่างเป็นทรงกลมเนื่องจากสะพานไดซัลไฟด์ห้าสะพานและปฏิกิริยาเล็กน้อยอื่นๆ (ไฟฟ้าสถิต แรง Van der Waals พันธะไฮโดรเจน ฯลฯ)
Chymotrypsin ผลิตโดยเซลล์ chymose ของตับอ่อนซึ่งมีอยู่ในเยื่อหุ้มพิเศษและขับออกทางท่อตับอ่อนเข้าสู่ลำไส้ในขณะที่ย่อยอาหาร: จริง ๆ แล้ว chymotrypsin เป็นเอนไซม์ย่อยอาหาร โปรตีนและสารอาหารที่เรากินเข้าไปจะถูกย่อยให้ย่อยเป็นโซ่เล็กๆ และถูกดูดซึมและเปลี่ยนเป็นพลังงาน (เช่น อะไมเลสและโปรตีเอสจะย่อยสารอาหารเป็นกลูโคสและกรดอะมิโนที่ไปถึงเซลล์ ผ่านทางหลอดเลือด พวกเขาไปถึงหลอดเลือดดำพอร์ทัลและจากนั้นจะถูกส่งไปยังตับซึ่งพวกเขาได้รับการรักษาต่อไป)
เอ็นไซม์ถูกผลิตขึ้นในรูปแบบที่ไม่ออกฤทธิ์และเปิดใช้งานก็ต่อเมื่อพวกมันไปถึง "ไซต์ที่พวกมันต้องทำงาน" เท่านั้น เมื่อการกระทำของพวกเขาเสร็จสิ้น พวกเขาจะปิดการใช้งาน เอ็นไซม์เมื่อปิดใช้งานแล้วจะไม่สามารถเปิดใช้งานได้อีก: เพื่อให้มี "การเร่งปฏิกิริยาเพิ่มเติม จะต้องถูกแทนที่ด้วย" โมเลกุลของเอ็นไซม์อื่น หาก chimitrypsin ถูกผลิตขึ้นในรูปแบบที่ใช้งานอยู่แล้วในตับอ่อน มันจะโจมตีอย่างหลัง: ตับอ่อนอักเสบเป็นพยาธิสภาพเนื่องจากเอนไซม์ย่อยอาหารที่ถูกกระตุ้นแล้วในตับอ่อน (และไม่ได้อยู่ในไซต์ที่ต้องการ) บางส่วนหากไม่ได้รับการรักษาทันเวลา นำไปสู่ความตาย
ในไคโมทริปซินและในซีรีนโปรตีเอสทั้งหมด ปฏิกิริยาเร่งปฏิกิริยาเกิดจากการมีอยู่ของแอลกอฮอล์แอนไอออน (-CH2O-) ในสายโซ่ด้านข้างของซีรีน
โปรตีเอสซีรีนใช้ชื่อนี้อย่างแม่นยำเพราะการเร่งปฏิกิริยาเกิดจากซีรีน
เมื่อเอนไซม์ทั้งหมดได้ทำหน้าที่ของมันแล้ว ก่อนจึงจะสามารถทำงานบนซับสเตรทได้อีกครั้ง จะต้องคืนสภาพด้วยน้ำ การ "ปลดปล่อย" ของซีรีนโดยน้ำเป็นขั้นตอนที่ช้าที่สุดของกระบวนการ และอยู่ในระยะนี้ ซึ่งกำหนดความเร็วของตัวเร่งปฏิกิริยา
การกระทำของตัวเร่งปฏิกิริยาเกิดขึ้นในสองขั้นตอน:
- การก่อตัวของประจุลบที่มีคุณสมบัติเร่งปฏิกิริยา (anion alcoholate) และการโจมตีของนิวคลีโอฟิลิกที่ตามมาในคาร์บอนิลคาร์บอน (C = O) โดยมีความแตกแยกของพันธะเปปไทด์และการก่อตัวของเอสเทอร์
- การโจมตีด้วยน้ำด้วยการฟื้นฟูตัวเร่งปฏิกิริยา (สามารถออกแรงเร่งปฏิกิริยาได้อีกครั้ง)
เอนไซม์ต่างๆ ที่อยู่ในตระกูลซีรีนโปรตีเอสสามารถประกอบขึ้นจากกรดอะมิโนที่แตกต่างกัน แต่สำหรับพวกมันทั้งหมด ไซต์ตัวเร่งปฏิกิริยาจะแสดงด้วยไอออนแอลกอฮอล์ของสายโซ่ด้านข้างของซีรีน
อนุวงศ์ของโปรตีเอสซีรีนคือเอ็นไซม์ที่เกี่ยวข้องกับการแข็งตัวของเลือด (ซึ่งประกอบด้วยการเปลี่ยนแปลงของโปรตีนจากรูปแบบที่ไม่ใช้งานของพวกมันไปเป็น "รูปแบบอื่นที่ทำงานอยู่) เอนไซม์เหล่านี้ช่วยให้แน่ใจว่าการแข็งตัวของเลือดมีประสิทธิภาพมากที่สุดและถูกจำกัดใน พื้นที่และเวลา (การแข็งตัวของเลือดจะต้องเกิดขึ้นอย่างรวดเร็วและต้องเกิดขึ้นเฉพาะในบริเวณที่ได้รับบาดเจ็บ) เอนไซม์ที่เกี่ยวข้องกับการแข็งตัวของเลือดจะถูกกระตุ้นในน้ำตก กระตุ้นเอนไซม์อื่นๆ อีกมากมาย)
การเกิดลิ่มเลือดเป็นพยาธิสภาพเนื่องจากความผิดปกติของเอนไซม์การแข็งตัวของเลือด: เกิดจากการกระตุ้นโดยไม่จำเป็น (เพราะไม่มีการบาดเจ็บ) ของเอนไซม์ที่ใช้ในการจับตัวเป็นก้อน
มีเอ็นไซม์ควบคุม (ควบคุม) และเอ็นไซม์ยับยั้งสำหรับเอ็นไซม์อื่น ๆ : โต้ตอบกับหลัง ควบคุม หรือยับยั้งกิจกรรมของพวกเขา แม้แต่ผลิตภัณฑ์ของเอ็นไซม์ก็สามารถเป็นตัวยับยั้งการทำงานของเอ็นไซม์ได้ นอกจากนี้ ยังมีเอ็นไซม์ที่ออกฤทธิ์มากขึ้น
ไลโซไซม์
ลุยจิ ปาสเตอร์ ค้นพบโดยการจามบนจานเพาะเชื้อ ว่าในน้ำมูกมีเอนไซม์ที่สามารถฆ่าเชื้อแบคทีเรียได้: ไลโซไซม์; จากภาษากรีก: ลิโซ = ขนาด; zimo = เอ็นไซม์
ไลโซไซม์สามารถทำลายผนังเซลล์ของแบคทีเรียได้ แบคทีเรียและสิ่งมีชีวิตที่มีเซลล์เดียวโดยทั่วไปต้องการโครงสร้างต้านทานทางกลไกที่จำกัดรูปร่างของพวกมัน ภายในแบคทีเรียมีแรงดันออสโมติกสูงมากจึงดึงดูดน้ำ พลาสมาเมมเบรนจะระเบิดหากไม่มีผนังเซลล์ที่ขวางทางน้ำและจำกัดปริมาตรของแบคทีเรีย
ผนังเซลล์ประกอบด้วยสายโซ่โพลีแซ็กคาไรด์ซึ่งโมเลกุลของ N-acetyl-glucosamine (NAG) และโมเลกุลของกรด N-acetyl-muramic (NAM) สลับกัน พันธะระหว่าง NAG และ NAM ถูกทำลายโดยการไฮโดรไลซิสกลุ่มคาร์บอกซิลของ NAM ในผนังเซลล์ มีพันธะเปปไทด์กับกรดอะมิโน
ระหว่างสายโซ่ต่างๆ สะพานถูกสร้างขึ้นประกอบด้วยพันธะเทียมเปปไทด์: การแตกแขนงเกิดจากโมเลกุลไลซีน โครงสร้างโดยรวมนั้นแตกแขนงออกมากและทำให้มีความเสถียรสูง
ไลโซไซม์เป็นยาปฏิชีวนะ (ฆ่าเชื้อแบคทีเรีย): ทำงานโดยทำให้เกิดรอยร้าวในผนังแบคทีเรีย เมื่อโครงสร้างนี้ (ซึ่งมีความทนทานต่อกลไก) แตก แบคทีเรียจะดึงน้ำออกมาจนกว่าจะแตกออก ไลโซไซม์สามารถทำลายพันธะกลูโคซิดิก β-1,4 ระหว่าง NAM และ NAG
ไซต์ตัวเร่งปฏิกิริยาของไลโซไซม์แสดงโดยร่องที่ไหลไปตามเอ็นไซม์ซึ่งสอดสายโพลีแซ็กคาไรด์เข้าไป: วงแหวนกลูโคซิดิกหกวงของโซ่วางอยู่ในร่อง
ในตำแหน่งที่สามของร่อง c "เป็นโช้ค: ในตำแหน่งนี้สามารถวาง NAG ได้เพียงอันเดียวเนื่องจาก NAM ซึ่งมีมิติสูงกว่าไม่สามารถเข้าได้ ไซต์ตัวเร่งปฏิกิริยาจริงอยู่ระหว่างตำแหน่งที่สี่และห้า: เนื่องจากมี NAG ในตำแหน่งที่สาม การตัดจะเกิดขึ้นระหว่าง NAM และ NAG (และไม่ใช่ในทางกลับกัน) การตัดจึงเป็นแบบเฉพาะเจาะจง
pH ที่เหมาะสมที่สุดสำหรับไลโซไซม์ในการทำงานคือห้า ในตำแหน่งเร่งปฏิกิริยาของเอนไซม์ กล่าวคือ ระหว่างตำแหน่งที่สี่และห้า มีสายโซ่ด้านข้างของกรดแอสปาร์ติกและกรดกลูตามิก
ระดับความคล้ายคลึงกัน: วัดความสัมพันธ์ (เช่น ความคล้ายคลึงกัน) ระหว่างโครงสร้างโปรตีน
มีความสัมพันธ์ที่แน่นแฟ้นระหว่างไลโซไซม์และแลคโตส-ซินเทส
แลคโตสซินธิเทสสังเคราะห์แลคโตส (ซึ่งเป็นน้ำตาลในนมหลัก): แลคโตสเป็นกาแลคโตซิลกลูโคไซด์ซึ่งค "เป็นพันธะกลูโคซิดิกβ-1,4 ระหว่างกาแลคโตสและกลูโคส
ดังนั้น แลคโตส synthetase เร่งปฏิกิริยาที่ตรงกันข้ามกับที่เร่งปฏิกิริยาโดยไลโซไซม์ (ซึ่งจะแยกพันธะกลูโคซิดิก β-1,4) แทน
แลคโตสซินธิเทสเป็นไดเมอร์ กล่าวคือ มันประกอบด้วยโปรตีนสองสาย ซึ่งหนึ่งในนั้นมีคุณสมบัติในการเร่งปฏิกิริยาและเปรียบได้กับไลโซไซม์ และอีกอันเป็นหน่วยย่อยด้านกฎระเบียบ
ในระหว่างตั้งครรภ์ glycoproteins จะถูกสังเคราะห์โดยเซลล์ของต่อมน้ำนมโดยการกระทำของ galatosyl-tranferase (มี "ความคล้ายคลึงลำดับ 40% กับไลโซไซม์): เอนไซม์นี้สามารถถ่ายโอนกลุ่มกาแลคโตซิลจากโครงสร้างพลังงานสูงไปยัง โครงสร้างของ glycoprotein ในระหว่างตั้งครรภ์ การแสดงออกของยีนที่เป็นรหัสของ ต่อมน้ำนม (ก่อนหน้านี้ไม่ทำงาน) ซึ่งต้องผลิตน้ำนม ในระหว่างการคลอดบุตร α-lactalbumin ถูกผลิตซึ่งเป็นโปรตีนควบคุม: สามารถควบคุมความสามารถในการเร่งปฏิกิริยาของกาแลคโตซิล-ทรานสเฟอเรส (โดยการเลือกปฏิบัติของสารตั้งต้น) . กาแลคโตซิล-ทรานสเฟอเรสดัดแปลงโดย α-lactalalbumin สามารถถ่ายโอนกาแลคโตซิลไปยังโมเลกุลกลูโคส: สร้างพันธะไกลโคซิดิก β-1,4 และให้แลคโตส (แลคโตสสังเคราะห์)
ดังนั้นกาแลคโตสทรานสเฟอร์เอสจึงเตรียมต่อมน้ำนมก่อนคลอดและผลิตน้ำนมหลังคลอด
ในการผลิตไกลโคโปรตีน กาแลคโตซิลทรานสเฟอร์เรสจับกับกาแลคโตซิลและ NAG; ในระหว่างการคลอดบุตร lactal albumin จับกับ galactosyltransferase ทำให้คนหลังรู้จักกลูโคสและไม่ให้ NAG ให้แลคโตสอีกต่อไป