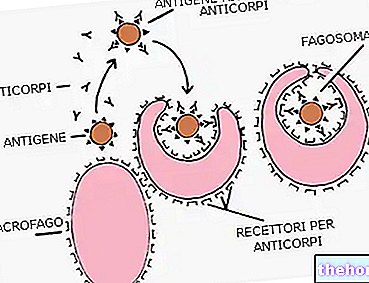
สารออกฤทธิ์: ออกซาโตไมด์
Tinset ผู้ใหญ่ 30 มก. เม็ด
เม็ดมีดแพ็คเกจ Tinset มีจำหน่ายสำหรับขนาดแพ็ค:- Tinset ผู้ใหญ่ 30 มก. เม็ด
- Tinset 25 มก. / มล. ระงับช่องปาก
- ทินเซ็ต 5% เจล
เหตุใดจึงใช้ Tinset มีไว้เพื่ออะไร?
หมวดหมู่เภสัชบำบัด
ยาต้านฮีสตามีนสำหรับการใช้งานอย่างเป็นระบบ
ตัวชี้วัดการรักษา
การป้องกันและการรักษาพื้นฐานของโรคภูมิแพ้ ส่วนใหญ่ในกรณีของโรคจมูกอักเสบ โรคหอบหืดภายนอก เยื่อบุตาอักเสบจากรูขุมขน ลมพิษเรื้อรัง โรคผิวหนังภูมิแพ้ การแพ้อาหารหากจำเป็น TINSET สามารถใช้ร่วมกับผลิตภัณฑ์ยาอื่น ๆ ที่สอดคล้องกับข้อบ่งชี้เหล่านี้โดยมีเงื่อนไขว่ากลไกการทำงานแตกต่างจาก TINSET TINSET ไม่ได้ระบุไว้ในการรักษาภาวะภูมิแพ้เฉียบพลันเช่นโรคหอบหืด
ข้อห้าม เมื่อไม่ควรใช้ Tinset
แพ้สารออกฤทธิ์ ซินนาริซีนหรือสารเพิ่มปริมาณใด ๆ ตับวาย
ข้อควรระวังในการใช้งาน สิ่งที่คุณต้องรู้ก่อนรับประทาน Tinset
อย่ากินเครื่องดื่มแอลกอฮอล์และอย่าใช้ยาที่มีแอลกอฮอล์ในขณะที่ทาน Tinset
ออกซาโตไมด์เช่นเดียวกับยาต้านฮีสตามีนอื่นๆ อาจรบกวนการทดสอบการแพ้ทางผิวหนัง ดังนั้นควรหยุดการรักษาอย่างน้อย 3 วันก่อนการทดสอบผิวหนัง
ปฏิกิริยา ยาหรืออาหารชนิดใดที่สามารถปรับเปลี่ยนผลกระทบของ Tinset
แจ้งให้แพทย์หรือเภสัชกรทราบ หากคุณเพิ่งใช้ยาอื่นใด แม้แต่ยาที่ไม่มีใบสั่งยา
จากการศึกษาเมแทบอลิซึมของ oxatomide อาจมีปฏิสัมพันธ์ระหว่าง Oxatomide และ CYP450 inhibitors เช่น itraconazole, ketoconazole และ cimetidine Tinset อาจเพิ่มผลกดประสาทของ depressants CNS รวมทั้งแอลกอฮอล์ barbiturates hypnotics ยาแก้ปวดยาเสพติด sedatives anxiolytics และยารักษาโรคจิต ผลข้างเคียงที่ไม่พึงประสงค์ของยา anticholinergic อาจเพิ่มขึ้นโดยการใช้ Tinset ร่วมกัน ไม่แนะนำให้ใช้สารยับยั้ง MAO และ Tinset ร่วมกัน
คำเตือน สิ่งสำคัญคือต้องรู้ว่า:
TINSET ไม่ได้ระบุไว้ในการรักษาภาวะภูมิแพ้เฉียบพลัน เช่น โรคหอบหืด เมื่อกำหนด Tinset ให้กับผู้ป่วยที่เป็นโรคหอบหืด ไม่ควรหยุดการรักษาด้วยยาในปัจจุบันอย่างกะทันหัน แต่จะค่อยๆ ลดขนาดยาลง โดยเฉพาะอย่างยิ่งสำหรับผู้ป่วยที่ได้รับการรักษาด้วยคอร์ติโคสเตียรอยด์ มีรายงานกรณีของโรคตับอักเสบ อาการบาดเจ็บที่ตับ โรคดีซ่าน และการทำงานของตับผิดปกติ (เอนไซม์ตับเพิ่มขึ้นปานกลางถึงมาก) รวมถึงกรณีที่ตับวายถึงแก่ชีวิตได้น้อยมาก
ผู้ป่วยควรได้รับการสังเกตอย่างระมัดระวังสำหรับผลข้างเคียงของตับ ในกรณีที่ตับทำงานผิดปกติ ควรใช้มาตรการที่เหมาะสม เช่น การหยุดการรักษา และไม่ควรให้การรักษาด้วย Tinset กลับมาอีกครั้ง
เนื่องจากการกำจัดตับ ควรใช้ความระมัดระวังเมื่อกำหนดให้ออกซาโตไมด์แก่ผู้ป่วยที่มีความผิดปกติของตับที่ทราบ หากจำเป็น การรักษาผู้ป่วยเหล่านี้ควรเริ่มต้นที่ครึ่งหนึ่งของขนาดยาปกติ ช่วงเวลาระหว่างการบริหารให้สามารถคงไว้ไม่เปลี่ยนแปลง
มีอาการ Dyskinesia และ extrapyramidal ทั้งในผู้ใหญ่และเด็ก อาการ Extrapyramidal พบได้บ่อยในเด็ก
ในประชากรสูงอายุ การเปลี่ยนแปลงทางสรีรวิทยาที่เกี่ยวข้องกับอายุ (เช่น การซึมผ่านที่เพิ่มขึ้นของอุปสรรคในเลือดและสมองและการเผาผลาญของตับที่ลดลง) อาจส่งผลต่อการทำงานของตัวรับ H1 ในผู้สูงอายุ ความเสี่ยงที่เพิ่มขึ้นของยาระงับประสาทจะต้องนำมาพิจารณาด้วย .
การตั้งครรภ์ ให้นมบุตร และภาวะเจริญพันธุ์
ปรึกษาแพทย์หรือเภสัชกรเพื่อขอคำแนะนำก่อนรับประทานยาใดๆ
ความปลอดภัยของ Tinset ในหญิงตั้งครรภ์ยังไม่ได้รับการจัดตั้งขึ้น หากจำเป็นต้องให้ยา Tinset ในระหว่างตั้งครรภ์ ควรชั่งน้ำหนักความเสี่ยงที่อาจเกิดขึ้นอย่างรอบคอบกับผลการรักษาที่คาดหวังไว้
มีข้อมูลไม่เพียงพอเกี่ยวกับการขับออกซาโตไมด์ในน้ำนมแม่ ดังนั้น ในกรณีของการรักษาด้วย Tinset ควรหยุดให้นมบุตร
ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
ไม่แนะนำให้ขับรถหรือใช้เครื่องจักรขณะใช้ Tinset เนื่องจากอาจเกิดอาการง่วงนอนและลดความตื่นตัวได้ การดื่มแอลกอฮอล์พร้อมๆ กันอาจส่งผลต่อผลกระทบเหล่านี้
ข้อมูลสำคัญเกี่ยวกับส่วนผสมบางอย่าง
ยามีแลคโตส ในกรณีที่ไม่สามารถทนต่อน้ำตาลได้ โปรดติดต่อแพทย์ก่อนรับประทานยา
ปริมาณและวิธีการใช้ วิธีใช้ Tinset: Dosage
ผู้ใหญ่
สำหรับแต่ละข้อบ่งชี้ 1 เม็ดวันละสองครั้ง หลังอาหารเช้าและหลังอาหารเย็น
ความสนใจ
เพื่อหลีกเลี่ยงการใช้ยาเกินขนาดโดยไม่ได้ตั้งใจ ให้ปฏิบัติตามปริมาณที่แนะนำอย่างเคร่งครัด
ยาเกินขนาด จะทำอย่างไรถ้าคุณทาน Tinset มากเกินไป
อาการที่รายงานบ่อยที่สุดหลังการให้ยาเกินขนาด ได้แก่ อาการง่วงซึม อาการมึนงง และอาการผิดปกติของกล้ามเนื้อ เช่น ดายสกิน คอเคล็ด การเคลื่อนไหวของดวงตาโดยไม่ได้ตั้งใจ ดีสโทเนีย และภาวะไขมันในเลือดสูง
พบได้น้อยกว่าคือความตื่นตัวและความตื่นตระหนก ไม่ค่อยมีรายงานเกี่ยวกับ mydriasis และกล้ามเนื้อกระตุกทั่วไปและโคม่า หลังจากให้ยาเกินขนาดแล้วจะมีรายงานการสูญเสียสติและการยืด QT
ไม่มียาแก้พิษเฉพาะ การรักษาประกอบด้วยการติดตามสัญญาณชีพและมาตรการสนับสนุนอย่างใกล้ชิด ควรทำ ECG เพื่อประเมินส่วน QT หากเห็นว่าเหมาะสม อาจให้ถ่านกัมมันต์ อาการ extrapyramidal ได้รับการรักษาด้วยยา anticholinergic เรียบร้อยแล้ว
ในกรณีที่กลืนกิน / รับประทานยา Tinset ในปริมาณที่มากเกินไปโดยไม่ได้ตั้งใจ ให้แจ้งแพทย์ทันทีหรือไปโรงพยาบาลที่ใกล้ที่สุด
หากคุณมีข้อสงสัยเกี่ยวกับการใช้ TINSET โปรดติดต่อแพทย์หรือเภสัชกรของคุณ
ผลข้างเคียง ผลข้างเคียงของ Tinset คืออะไร
เช่นเดียวกับยาทั้งหมด TINSET สามารถทำให้เกิดผลข้างเคียงได้แม้ว่าจะไม่ใช่ทุกคนที่ได้รับก็ตาม
ผลกระทบที่ไม่พึงประสงค์ที่ได้รับรายงานจากการใช้ Tinset ทั้งในการทดลองทางคลินิกและระหว่างการทำการตลาดมีการระบุไว้ด้านล่าง
ในกรณีทั่วไป มีรายงานดังต่อไปนี้: น้ำหนักเพิ่มขึ้น, ง่วงซึม, เหนื่อยล้า, มีความอยากอาหารเพิ่มขึ้น
พบบ่อยมาก (อาจส่งผลกระทบมากกว่า 1 ใน 10 คน): อาการง่วงนอน
ร่วมกัน (อาจส่งผลกระทบมากถึง 1 ใน 10 คน): ความอยากอาหารเพิ่มขึ้น เหนื่อยล้า ปวดหัว ใจเย็น ปากแห้ง น้ำหนักขึ้น)
ผิดปกติ (อาจส่งผลกระทบมากถึง 1 ใน 100 คน): เบื่ออาหาร, หงุดหงิด, กระสับกระส่าย, หงุดหงิด, นอนไม่หลับ, รบกวนสมาธิ, เวียนศีรษะ, หายใจถี่, คลื่นไส้, อาเจียน, ปวดท้อง, ปวดท้องตอนบน , อาการอาหารไม่ย่อย, ท้องผูก, ไม่สบายหน้าอก, การเก็บปัสสาวะ, ผื่น, ลมพิษ
หายากมาก (อาจส่งผลกระทบมากถึง 1 ใน 1,000 คน): ภาวะโลหิตจางจากเม็ดเลือดแดง, ภาวะเกล็ดเลือดต่ำ, เม็ดเลือดขาว, เม็ดเลือดขาว, ภาวะช็อกจากภูมิแพ้, ปฏิกิริยาภูมิแพ้, ปฏิกิริยา anaphylactoid, ภูมิไวเกิน, ความอยากอาหารลดลง, อาการประสาทหลอน, ความปั่นป่วน, ความไม่แยแส, ความสับสน, อาการเวียนศีรษะ, ฝันร้าย , รบกวนการนอนหลับ , ความก้าวร้าว, อาการชัก, ระดับสติลดลง, หมดสติ, อาการมึนงง, ความง่วง, ความพิการทางสมอง, อาชา, ความผิดปกติของ extrapyramidal, การประสานงานผิดปกติ, ดายสกิน, dysarthria, dysgeusia, hypertonia, hypotonia, opisthotonus, แรงสั่นสะเทือน, myoclonus, ataxiad , dystonia, วิกฤตตา, ตาพร่ามัว, การมองเห็นสองครั้ง, การขยายรูม่านตาผิดปกติ, อัมพาตจากการจ้องมอง, หูอื้อ, การสูญเสียการได้ยิน, torsade de pointes, ภาวะมีกระเป๋าหน้าท้อง, ภาวะหัวใจเต้นผิดจังหวะ, กระเป๋าหน้าท้อง extrasystole, จังหวะ, หัวใจเต้นเร็ว, หัวใจเต้นช้า, ใจสั่น , ตกตะลึง, ตกใจ, ความดันโลหิตต่ำ เลือดกำเดาไหล หลอดลมหดเกร็ง เยื่อเมือกแห้ง na เกลือ, คอหอยบวมน้ำ, กรดไหลย้อน gastroesophageal, ท้องร่วง, ตับวาย (ร้ายแรง), ตับอักเสบเฉียบพลัน, โรคตับอักเสบจากน้ำดี, ตับอักเสบ, ตับอักเสบเฉียบพลัน, ความเสียหายต่อเซลล์ตับ, พิษต่อตับ, การบาดเจ็บที่ตับ, โรคดีซ่าน cholestatic, โรคดีซ่าน, cholestasis, การทำงานของตับผิดปกติ, ไขมันพอกตับ , ตับ ความผิดปกติ, การตายของเนื้อร้ายที่ผิวหนังที่เป็นพิษ, กลุ่มอาการสตีเวนส์ - จอห์นสัน, ผื่นที่เป็นพิษ, erythema multiforme, ผื่นแดง, angioedema, อาการคัน, ผื่นแดง, ปฏิกิริยาไวแสง, การปะทุของยา, กลาก, เหงื่อออกมากเกินไป, ความตึงของกล้ามเนื้อ, กล้ามเนื้ออ่อนแรง, ปวดกล้ามเนื้อ , คอเคล็ด, trismus, dysuria, ปัสสาวะ, chromaturia, gynaecomastia, galactorrhea, รบกวนการเดิน, วิงเวียน, hyperpyrexia, pyrexia, ความรู้สึกเย็น, บวมน้ำ, ความรู้สึกผิดปกติ, การยืดตัวของทางเดิน QT ของคลื่นไฟฟ้าหัวใจ, ความผิดปกติของคลื่นไฟฟ้าหัวใจ, ความผิดปกติของการทดสอบการทำงานของตับ, ตับ เอนไซม์เพิ่มขึ้น, อะลานีนอะมิโนทรานสเฟอเรสเพิ่มขึ้น, เพิ่มขึ้น แอสพาเทตอะมิโนทรานสเฟอเรสเพิ่มขึ้น, แกมมากลูตามิลทรานสเฟอเรสเพิ่มขึ้น, บิลิรูบินในเลือดเพิ่มขึ้น, อัลคาไลน์ฟอสฟาเตสในเลือดเพิ่มขึ้น, creatinine ฟอสโฟไคเนสในเลือดเพิ่มขึ้น, แลคเตทดีไฮโดรจีเนสในเลือดเพิ่มขึ้น, ความดันโลหิตลดลง, อัตราการเต้นของหัวใจเพิ่มขึ้น
ผู้ป่วยเด็ก
เหตุการณ์ไม่พึงประสงค์ที่ระบุไว้ในส่วน "ผลที่ไม่พึงประสงค์" นี้อาจเกิดขึ้นในประชากรเด็ก
การปฏิบัติตามคำแนะนำในเอกสารบรรจุภัณฑ์ช่วยลดความเสี่ยงของผลกระทบที่ไม่พึงประสงค์
การรายงานผลข้างเคียง
หากคุณได้รับผลข้างเคียงใดๆ ให้ปรึกษาแพทย์หรือเภสัชกร ซึ่งรวมถึงผลข้างเคียงที่อาจเกิดขึ้นซึ่งไม่ได้ระบุไว้ในเอกสารฉบับนี้ คุณยังสามารถรายงานผลข้างเคียงได้โดยตรงผ่านระบบการรายงานระดับประเทศที่ https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse ในการรายงานผลข้างเคียง คุณสามารถช่วยให้ข้อมูลเพิ่มเติมเกี่ยวกับความปลอดภัยของยานี้ได้
การหมดอายุและการเก็บรักษา
วันหมดอายุ: ดูวันหมดอายุที่พิมพ์บนบรรจุภัณฑ์
วันหมดอายุหมายถึงผลิตภัณฑ์ในบรรจุภัณฑ์ที่ไม่เสียหาย จัดเก็บไว้อย่างถูกต้อง
คำเตือน: ห้ามใช้ยาหลังจากวันหมดอายุที่แสดงบนบรรจุภัณฑ์
ยาไม่ควรทิ้งทางน้ำเสียหรือของเสียในครัวเรือน ถามเภสัชกรว่าจะทิ้งยาที่คุณไม่ได้ใช้แล้วทิ้งอย่างไร ซึ่งจะช่วยปกป้องสิ่งแวดล้อม
เก็บผลิตภัณฑ์ยาให้พ้นสายตาและมือเด็ก
องค์ประกอบและรูปแบบยา
องค์ประกอบ
หนึ่งเม็ดประกอบด้วย:
สารออกฤทธิ์: ออกซาโตไมด์ 30 มก.; สารเพิ่มปริมาณ: แลคโตส, แป้งข้าวโพด, เซลลูโลส microcrystalline, โพวิโดน, ซิลิกาตกตะกอน, แมกนีเซียมสเตียเรต
รูปแบบและเนื้อหาทางเภสัชกรรม
30 เม็ด 30 มก.
เอกสารแพ็คเกจที่มา: AIFA (หน่วยงานยาอิตาลี) เนื้อหาที่เผยแพร่ในเดือนมกราคม 2016 ข้อมูลที่แสดงอาจไม่ทันสมัย
หากต้องการเข้าถึงเวอร์ชันล่าสุด ขอแนะนำให้เข้าถึงเว็บไซต์ AIFA (Italian Medicines Agency) ข้อจำกัดความรับผิดชอบและข้อมูลที่เป็นประโยชน์
01.0 ชื่อผลิตภัณฑ์ยา
TINSET
02.0 องค์ประกอบเชิงคุณภาพและเชิงปริมาณ
TINSET ผู้ใหญ่ 30 มก. เม็ด
หนึ่งเม็ดประกอบด้วย: สารออกฤทธิ์ออกซาโตไมด์ 30 มก.
สารเพิ่มปริมาณ: แลคโตส 120.09 mg
TINSET 25 มก. / มล ยาหยอดปากระงับ
สารแขวนลอย 100 มล. ประกอบด้วย: สารออกฤทธิ์ Oxatomide ไฮเดรต 2.6 กรัม (เท่ากับ 2.5 กรัมของออกซาโตไมด์)
สารเพิ่มปริมาณ: เมทิล p-ไฮดรอกซีเบนโซเอต 180 มก., โพรพิล p-ไฮดรอกซีเบนโซเอต 20 มก.
สำหรับรายการสารปรุงแต่งทั้งหมด ดูหัวข้อ 6.1
03.0 รูปแบบเภสัชกรรม
แท็บเล็ต:
สีขาว กลม แบน สลัก "30" ด้านหนึ่งและเส้นบอกคะแนนอีกด้านหนึ่ง
ยาหยอดปากระงับ:
ระงับสีขาว
04.0 ข้อมูลทางคลินิก
04.1 ข้อบ่งชี้การรักษา
การป้องกันและการรักษาพื้นฐานของโรคภูมิแพ้ ส่วนใหญ่ในกรณีของโรคจมูกอักเสบ โรคหอบหืดภายนอก (ไม่รวมการโจมตีของโรคหอบหืด) เยื่อบุตาอักเสบจากรูขุมขน ลมพิษเรื้อรัง โรคผิวหนังภูมิแพ้ การแพ้อาหาร หากจำเป็น TINSET สามารถใช้ร่วมกับยาอื่น ๆ ที่สอดคล้องกับข้อบ่งชี้เหล่านี้ โดยมีเงื่อนไขว่ากลไกการออกฤทธิ์แตกต่างจาก TINSET
TINSET ไม่ได้ระบุไว้สำหรับการรักษาภาวะภูมิแพ้เฉียบพลัน เช่น โรคหอบหืด
04.2 วิทยาและวิธีการบริหาร
TINSET ผู้ใหญ่ 30 มก. เม็ด,
ผู้ใหญ่: สำหรับแต่ละข้อบ่งชี้ 1 เม็ดเท่ากับ 30 มก. วันละสองครั้ง: หลังอาหารเช้าและหลังอาหารเย็น
TINSET 25 มก. / มล ยาหยอดปากระงับ ผู้ใหญ่: สำหรับแต่ละข้อบ่งชี้ 30 หยดเท่ากับ 30 มก. วันละสองครั้ง: หลังอาหารเช้าและหลังอาหารเย็น
เด็กที่มีอายุตั้งแต่ 1 ปีขึ้นไป: สำหรับแต่ละข้อบ่งชี้:
1 หยดต่อน้ำหนักตัวทุกๆ 2 กก. วันละสองครั้ง
สำหรับเด็กอายุ 1 ปีขึ้นไปและมีน้ำหนักตัวน้อยกว่า 12 กก. เช่นสำหรับเด็กที่มีน้ำหนักตัวมากกว่า 48 กก. ควรปรึกษาแพทย์
จำนวนหยดที่จะให้กับเด็กควรคำนวณตามน้ำหนักตัวของเด็ก
คำเตือน: การใช้ยาเกินขนาดสามารถนำไปสู่ผลที่ไม่พึงประสงค์อย่างร้ายแรง โดยเฉพาะอย่างยิ่งในเด็ก ดังนั้นจึงต้องปฏิบัติตามปริมาณที่แนะนำอย่างเคร่งครัด (ดูหัวข้อ 4.9) โดยเฉพาะอย่างยิ่ง เกี่ยวกับการใช้สารแขวนลอยในเด็ก เพื่อหลีกเลี่ยงการใช้ยาเกินขนาดโดยไม่ได้ตั้งใจ ปริมาณที่จะให้ควรคำนวณเป็นหยด
ผลิตภัณฑ์มีลักษณะคล้ายกับนม ดังนั้นจึงอาจดึงดูดความสนใจของเด็ก ซึ่งอาจเพิ่มความเสี่ยงที่จะให้ยาเกินขนาดในเด็ก
04.3 ข้อห้าม
ภูมิไวเกินต่อสารออกฤทธิ์ ซินนาริซีน หรือสารเพิ่มปริมาณใด ๆ ที่ระบุไว้ในหัวข้อ 6.1
ห้ามใช้ในเด็กอายุต่ำกว่า 1 ปี ผู้ป่วยที่มีภาวะตับไม่เพียงพอ
04.4 คำเตือนพิเศษและข้อควรระวังที่เหมาะสมสำหรับการใช้งาน
TINSET ไม่ได้ระบุไว้สำหรับการรักษาภาวะภูมิแพ้เฉียบพลัน เช่น โรคหอบหืด
เมื่อกำหนด Tinset ให้กับผู้ป่วยที่เป็นโรคหอบหืด ไม่ควรหยุดการรักษาด้วยยาอย่างต่อเนื่องอย่างกะทันหัน แต่ค่อยๆ ลดลง โดยเฉพาะอย่างยิ่งสำหรับผู้ป่วยที่ได้รับการรักษาด้วยคอร์ติโคสเตียรอยด์
จากประสบการณ์หลังการขายพบว่ามีรายงานเกี่ยวกับตับอักเสบ อาการบาดเจ็บที่ตับ โรคดีซ่าน และการเปลี่ยนแปลงในการทำงานของตับ (เอนไซม์ตับเพิ่มขึ้นปานกลางถึงมาก) รวมถึงกรณีของตับวายที่เสียชีวิตได้น้อยมาก ควรติดตามผู้ป่วยอย่างระมัดระวัง ผลข้างเคียง ในกรณีที่ค่าตับผิดปกติควรใช้มาตรการที่เหมาะสม เช่น การหยุดการรักษาและการรักษาด้วย Tinset ไม่ควรกลับมาดำเนินการอีก
เนื่องจากการกำจัดตับ ควรใช้ความระมัดระวังในการสั่งจ่ายออกซาโทไมด์ให้กับผู้ป่วยที่มีความผิดปกติของตับที่ทราบ หากจำเป็น การรักษาผู้ป่วยเหล่านี้ควรเริ่มต้นด้วยขนาดยาที่น้อยกว่าขนาดปกติ ช่วงเวลาระหว่างการให้ยาสามารถคงไว้ได้ไม่เปลี่ยนแปลง
มีอาการ Dyskinesia และ extrapyramidal ทั้งในผู้ใหญ่และเด็ก อาการ Extrapyramidal พบได้บ่อยในเด็ก เด็กอาจอ่อนไหวต่อผลกระทบของระบบประสาทส่วนกลางมากขึ้นเนื่องจากอุปสรรคเลือดและสมองยังไม่บรรลุนิติภาวะ ดังนั้น ควรให้ความระมัดระวังในเด็กอายุระหว่าง 1 ถึง 6 ปี และโดยเฉพาะอย่างยิ่งผู้ที่มีอายุระหว่าง 12 ถึง 24 เดือน Tinset ห้ามใช้ในเด็กอายุต่ำกว่า 1 ปี
ในประชากรสูงอายุ การเปลี่ยนแปลงทางสรีรวิทยาที่เกี่ยวข้องกับอายุ (เช่น การซึมผ่านที่เพิ่มขึ้นของอุปสรรคในเลือดและสมองและการเผาผลาญของตับที่ลดลง) อาจส่งผลต่อการทำงานของคู่อริของตัวรับ H1
ปฏิบัติตามปริมาณที่แนะนำ โดยเฉพาะอย่างยิ่งในเด็ก การใช้ยาแก้แพ้ยาแก้แพ้บางครั้งอาจทำให้เกิดผลร้ายแรงได้
ยาเม็ดประกอบด้วยแลคโตส ดังนั้น ผู้ป่วยที่มีปัญหาทางพันธุกรรมที่หายากของการแพ้กาแลคโต, การขาด Lapp lactase หรือการดูดซึมน้ำตาลกลูโคส-กาแลคโตส malabsorption ไม่ควรรับประทานยานี้
ยาหยอดปากแขวนลอยประกอบด้วยพารา-ไฮดรอกซีเบนโซเอตซึ่งอาจทำให้เกิดอาการแพ้ได้ (รวมทั้งยาที่ออกฤทธิ์ช้า)
ควรให้ Tinset ด้วยความระมัดระวังสำหรับผู้ป่วยสูงอายุเนื่องจากมีความเสี่ยงที่จะเกิดความใจเย็นมากขึ้น
ห้ามดื่มเครื่องดื่มแอลกอฮอล์และห้ามรับประทานยาที่มีแอลกอฮอล์ในขณะที่ใช้ยา Tinset (ดูหัวข้อ 4.5)
04.5 ปฏิกิริยากับผลิตภัณฑ์ยาอื่น ๆ และรูปแบบอื่น ๆ ของการโต้ตอบ
Oxatomide ถูกเผาผลาญโดย cytochrome P450 โดยเฉพาะอย่างยิ่งกับ iso 3A4 และ 2D6 ที่อาจเกิดขึ้นตามการศึกษาในหลอดทดลองเกี่ยวกับไมโครโซมในตับของมนุษย์จากการศึกษาในหลอดทดลอง อาจมีปฏิกิริยาระหว่างยา oxatomide และ CYP 450 inhibitor เช่น itraconazole, ketoconazole และ cimetidine
ผู้ป่วยควรทราบว่า Tinset อาจเพิ่มผลกดประสาทของยากล่อมประสาทส่วนกลาง ซึ่งรวมถึง แอลกอฮอล์ บาร์บิทูเรต ยาสะกดจิต ยาแก้ปวดที่เป็นยาเสพติด ยากล่อมประสาท ยาลดความวิตกกังวล และยารักษาโรคจิต (ดูหัวข้อ 4.7) ผลที่ไม่พึงประสงค์ของยาลดกรดในเลือดอาจเพิ่มขึ้นได้หากใช้ควบคู่ไปกับ Tinset ไม่แนะนำให้ใช้สารยับยั้ง MAO และ Tinset ร่วมกัน
ออกซาโตไมด์เช่นเดียวกับยาต้านฮีสตามีนอื่นๆ อาจรบกวนการทดสอบสารก่อภูมิแพ้ที่ผิวหนัง ดังนั้นควรหยุดการรักษาอย่างน้อย 3 วันก่อนการทดสอบผิวหนัง
04.6 การตั้งครรภ์และให้นมบุตร
การตั้งครรภ์
ไม่พบผลกระทบที่เป็นพิษต่อตัวอ่อนโดยตรง peri และหลังคลอดในสัตว์ ไม่มีผลเสียโดยตรงต่อภาวะเจริญพันธุ์ในขณะที่บันทึกผลกระทบรองในปริมาณที่เป็นพิษต่อมารดาเท่านั้น ข้อมูลการทดสอบในสัตว์ทดลองแสดงให้เห็นว่ามีการผ่านของออกซาโทไมด์อย่างจำกัดผ่านอุปสรรคของรก แต่ยังไม่มีการสร้างความปลอดภัยของ Tinset ในสตรีมีครรภ์ หากจำเป็นต้องให้ยา Tinset ในระหว่างตั้งครรภ์ ควรชั่งน้ำหนักความเสี่ยงที่อาจเกิดขึ้นอย่างรอบคอบกับผลการรักษาที่คาดหวังไว้
เวลาให้อาหาร
มีข้อมูลไม่เพียงพอเกี่ยวกับการขับออกซาโทไมด์ / เมแทบอไลต์ในนมแม่ ดังนั้น ในกรณีของการรักษาด้วย Tinset ควรหยุดให้นมลูก
04.7 ผลกระทบต่อความสามารถในการขับขี่และการใช้เครื่องจักร
เนื่องจากผลิตภัณฑ์อาจทำให้เกิดอาการง่วงนอนและเสียสมาธิได้ จึงควร เตือนผู้ที่ต้องขับรถหรือปฏิบัติงานที่ต้องเฝ้าระวังอย่างครบถ้วน การดื่มแอลกอฮอล์พร้อม ๆ กันอาจทำให้เกิดผลกระทบเหล่านี้ได้
04.8 ผลกระทบที่ไม่พึงประสงค์
ข้อมูลจากการศึกษาทางคลินิก
ความปลอดภัยของ Tinset ได้รับการประเมินในผู้ป่วย 1188 คน (ผู้ใหญ่ 674 คนและเด็ก 514 คน) ที่เข้าร่วมการศึกษาทางคลินิก 17 ครั้งกับ Tinset (การศึกษา 9 เรื่องเกี่ยวข้องกับผู้ใหญ่เท่านั้น เด็ก 5 คนเท่านั้น และ 3 คนทั้งคู่) ที่เป็นโรคหอบหืด ภูมิแพ้ตลอดกาล หรือตามฤดูกาล รวมทั้งโรคจมูกอักเสบ เยื่อบุตาอักเสบ, กลาก, โรคผิวหนังภูมิแพ้และผิวหนังติดต่อ, เบาหวาน, ลมพิษเรื้อรัง, แพ้ยา, แพ้อาหาร, หลอดลมอักเสบหรือ mastocytosis ที่ผิวหนัง
ผู้ป่วยเหล่านี้ได้รับ Tinset อย่างน้อยหนึ่งครั้งและได้รับข้อมูลด้านความปลอดภัย
ผู้ป่วยได้รับการรักษาด้วย Tinset เป็นระยะเวลา 1 สัปดาห์ถึง 15 เดือน
ความถี่ของอาการไม่พึงประสงค์ถูกกำหนดโดยใช้แบบแผนต่อไปนี้:
พบบ่อยมาก (≥1 / 10)
สามัญ (≥1 / 100,
ผิดปกติ (≥1 / 1,000 ถึง
หายาก (≥1 / 10,000,
หายากมาก (≤1 / 10,000)
ไม่ทราบ: ไม่สามารถประมาณความถี่ได้จากข้อมูลที่มีอยู่
อาการไม่พึงประสงค์ที่รายงานสำหรับ≥ 1% ของผู้ป่วยที่ได้รับการรักษาด้วย Tinset แสดงอยู่ในตารางที่ 1
อาการไม่พึงประสงค์น้อยกว่าที่รายงานโดย
ข้อมูลหลังการขาย
นอกจากอาการข้างเคียงที่รายงานในการทดลองทางคลินิกและที่ระบุไว้ข้างต้นแล้ว ยังมีการรายงานอาการข้างเคียงดังต่อไปนี้ระหว่างประสบการณ์หลังการขาย (ตารางที่ 3)
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัย
การรายงานอาการไม่พึงประสงค์ที่น่าสงสัยซึ่งเกิดขึ้นหลังจากการอนุมัติผลิตภัณฑ์ยามีความสำคัญเนื่องจากช่วยให้สามารถตรวจสอบความสมดุลของผลประโยชน์/ความเสี่ยงของผลิตภัณฑ์ยาได้อย่างต่อเนื่อง ขอให้ผู้เชี่ยวชาญด้านสุขภาพรายงานอาการไม่พึงประสงค์ที่น่าสงสัยผ่านระบบการรายงานระดับประเทศ "สำนักงานยาอิตาลี เว็บไซต์: www.agenziafarmaco.gov.it/it/responsabili
04.9 ใช้ยาเกินขนาด
อาการ: อาการที่รายงานบ่อยที่สุดหลังการให้ยาเกินขนาด ได้แก่ อาการง่วงซึม อาการมึนงง และอาการผิดปกติทางร่างกาย เช่น ดายสกิน คอเคล็ด การเคลื่อนไหวของดวงตาโดยไม่ได้ตั้งใจ ดีสโทเนีย และภาวะไขมันในเลือดสูง พบได้น้อยกว่าคือความตื่นตัวและความตื่นตระหนก Mydriasis มีอาการกระตุกของกล้ามเนื้อและโคม่าโดยทั่วไปมีรายงานน้อยมาก มีรายงานกรณีการหมดสติและการยืดระยะเวลา QT ที่เกิดขึ้นน้อยมากหลังจากให้ยาเกินขนาด
การรักษา: ไม่มียาแก้พิษเฉพาะ การรักษาประกอบด้วยการติดตามสัญญาณชีพและมาตรการสนับสนุนอย่างใกล้ชิด ควรทำ ECG เพื่อประเมินช่วง QT หากพิจารณาว่าเหมาะสม อาจให้ Activated Charcoal ได้ อาการ Extrapyramidal ได้รับการรักษาด้วยยา anticholinergic เรียบร้อยแล้ว
05.0 คุณสมบัติทางเภสัชวิทยา
05.1 คุณสมบัติทางเภสัชพลศาสตร์
กลุ่มยารักษาโรค: ยาแก้แพ้สำหรับการใช้ทั้งระบบและเฉพาะที่
รหัส ATC: R06AE06 (เม็ดและหยด) Oxatomide
Oxatomide เป็นยาต่อต้านการแพ้ที่ทำงานโดยยับยั้งการปลดปล่อยและผลกระทบของตัวกลางต่างๆ
เป็นที่ทราบกันดีว่าการบล็อกหรือการลดผลกระทบของตัวรับสื่อกลางสำหรับความแข็งแกร่ง (H1), serotonin (5-HT1), leukotrienes (LTC3, LTC4) และปัจจัยการรวมตัวของเกล็ดเลือด (PAF) เป็นที่ทราบกันดีว่าการโจมตีและความรุนแรงของปฏิกิริยาการแพ้จะถูกต่อต้านเพิ่มเติมด้วย oxatomide ผ่านทาง การลดการปล่อยตัวไกล่เกลี่ย: ผ่านการระดมแคลเซียมตัวกลางไกล่เกลี่ยของปฏิกิริยาการแพ้ที่ผลิตและจัดเก็บโดยแมสต์เซลล์จะถูกหลั่งออกมา กระบวนการนี้ถูกยับยั้งโดยออกซาโตไมด์
ในปริมาณทางคลินิก oxatomide จะไม่ออกแรงทางเภสัชวิทยานอกเหนือจากการต่อต้านการแพ้
05.2 คุณสมบัติทางเภสัชจลนศาสตร์
ในมนุษย์ผลิตภัณฑ์จะถูกดูดซึมได้ดีหลังการบริหารช่องปากและถึงจุดสูงสุดของเลือดภายใน 2 ชั่วโมง ครึ่งชีวิตประมาณ 14 ชั่วโมงและถึงค่าพลาสม่าในสภาวะคงที่ (ประมาณ 35 ng / ml ด้วยปริมาณ 30 มก. วันละสองครั้ง ) หลังจาก 3 วัน การจับโปรตีนในพลาสมาจะอยู่ที่ประมาณ 98% ยาในช่องปากส่วนใหญ่จะถูกขับออกและเผาผลาญด้วยอุจจาระ (60%) โดยเฉพาะทางน้ำดีรวมทั้งทาง "ปัสสาวะและน้อยกว่า 0.5% ของขนาดยาจะถูกขับออกมาไม่เปลี่ยนแปลง . วิถีการเผาผลาญหลักดำเนินการโดยตับผ่านปฏิกิริยาออกซิเดชัน N-dealkylation, conjugation และอะโรมาติกไฮดรอกซิเลชัน
05.3 ข้อมูลความปลอดภัยพรีคลินิก
ศักยภาพความเป็นพิษของออกซาโตไมด์ได้รับการประเมินในชุดการศึกษาทางพิษวิทยาพรีคลินิก ซึ่งรวมถึงความเป็นพิษเฉียบพลันและเรื้อรัง ความเป็นพิษต่อระบบสืบพันธุ์ ความเป็นพิษต่อพันธุกรรม การเกิดมะเร็ง และการศึกษาความทนทาน (ทางผิวหนังและตา) ในท้องถิ่น
ออกซาโตไมด์ไม่ได้แสดงให้เห็นถึงศักยภาพของยีนหรือสารก่อมะเร็งในหนูหรือหนู
ยานี้ไม่มีผลต่อภาวะเจริญพันธุ์ในหนูและไม่ได้แสดงให้เห็นถึงศักยภาพในการทำให้ทารกอวัยวะพิการในหนูและกระต่าย เมื่อให้หนูในปริมาณที่เป็นพิษต่อมารดา oxatomide แสดงให้เห็นถึงผลกระทบต่อตัวอ่อนและทารกในครรภ์
06.0 ข้อมูลทางเภสัชกรรม
06.1 สารเพิ่มปริมาณ
30 มก. เม็ด: แลคโตส แป้งข้าวโพด ไมโครคริสตัลลีน เซลลูโลส โพวิโดน ซิลิกาตกตะกอน แมกนีเซียมสเตียเรต
25 มก. / มล ยาหยอดปากระงับ: ไมโครแกรนูลและเซลลูโลสคาร์เมลโลส, โพวิโดน, โพลีซอร์เบต 20, เมทิลพารา-ไฮดรอกซีเบนโซเอต, โพรพิลพารา-ไฮดรอกซีเบนโซเอต, โซเดียมซัคคาริน, น้ำบริสุทธิ์
06.2 ความเข้ากันไม่ได้
ไม่มีความไม่ลงรอยกันทางเคมีและกายภาพของสารออกซาโตไมด์กับสารประกอบอื่นๆ
06.3 ระยะเวลาที่มีผลบังคับใช้
TINSET ผู้ใหญ่ 30 มก. เม็ด TINSET 25 มก. / มล หยดในช่องปากระงับ: 5 ปี.
TINSET 25 มก. / มล หยดในช่องปากระงับ ยาต้องใช้ภายในสามเดือนหลังจากเปิดขวดครั้งแรก หลังจากช่วงเวลานี้ต้องทิ้งผลิตภัณฑ์ยาที่เหลือ
06.4 ข้อควรระวังพิเศษสำหรับการจัดเก็บ
ยานี้ไม่ต้องการเงื่อนไขการจัดเก็บพิเศษใด ๆ
06.5 ลักษณะการบรรจุทันทีและเนื้อหาของบรรจุภัณฑ์
TINSET ผู้ใหญ่ 30 มก. เม็ด
ตุ่มพีวีซีและอลูมิเนียม
บรรจุ 30 เม็ด
TINSET 25 มก. / มล หยดในช่องปากระงับ:
ขวดแก้วสีเหลืองพร้อมหลอดหยดโพรพิลีนและตัวปิดกันเด็ก
บรรจุภัณฑ์: ขวด 30 มล.
06.6 คำแนะนำในการใช้งานและการจัดการ
เพื่อหลีกเลี่ยงการใช้ยาเกินขนาดโดยไม่ได้ตั้งใจให้ปฏิบัติตามปริมาณที่แนะนำอย่างเคร่งครัด โดยเฉพาะอย่างยิ่งในเรื่องการใช้ยาแขวนลอยในช่องปากในเด็ก ปริมาณที่จะให้ต้องคำนวณเป็นหยดและขวดที่มีสารแขวนลอยจะต้องเขย่าอย่างแรงและทั่วถึงก่อนการใช้งานแต่ละครั้ง
TINSET 25 มก. / มล ยาหยอดปาก กันกระเทือน: น้ำยาปิดปากเด็ก:
ฝาปิดประเภทนี้ออกแบบมาเพื่อให้เด็กเปิดขวดได้ยาก โปรดจำไว้ว่า หากผู้ใหญ่ไม่ปิดขวดอย่างถูกต้องตามคำแนะนำด้านล่าง ฝาปิดจะไม่ทนต่อเด็กอีกต่อไป
• ในการเปิด ให้ดันฝาพลาสติกโดยให้หลอดหยดลงให้แน่น แล้วคลายเกลียว
• หลังจากการสุ่มตัวอย่าง ในการปิดอีกครั้ง ให้กดฝาพลาสติกโดยให้หยดลงไปอย่างแน่นหนา และในขณะเดียวกันก็ขันกลับเข้าไปใหม่
• เพื่อให้แน่ใจว่ากลไกด้านความปลอดภัยทำงานอย่างถูกต้อง ให้หมุนฝาทวนเข็มนาฬิกาโดยไม่ต้องกด และตรวจสอบว่าไม่สามารถเปิดขวดได้
เก็บยานี้ให้พ้นมือเด็ก
07.0 ผู้ทรงอำนาจการตลาด
GRUNENTHAL ITALIA S.r.l. - Via Carlo Bo, 11 - 20143 มิลาน
08.0 หมายเลขอนุญาตการตลาด
TINSET ผู้ใหญ่ 30 มก. เม็ด, 30 เม็ด - เอ.ไอ.ซี. NS. 025293010
TINSET 25 มก. / มล. ระงับช่องปาก, ขวด 30 มล. - เอ.ไอ.ซี. NS. 025293034
09.0 วันที่อนุญาตครั้งแรกหรือต่ออายุการอนุญาต
กุมภาพันธ์ 2555
10.0 วันที่แก้ไขข้อความ
3 กุมภาพันธ์ 2558